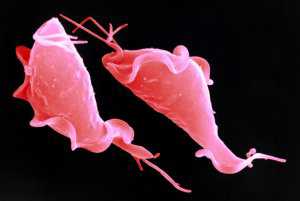
В клеточный хронический лимфолейкоз
Хронический в-клеточный лимфолейкоз (в-хлл)
Хронический В-клеточный лимфолейкоз (В-ХЛЛ) – это лимфопролиферативная опухоль преимущественно из CD5+-позитивных морфологически зрелых В-лимфоцитов с первичным поражением костного мозга.
Классификация хронического в-клеточного лимфолейкоза
Доброкачественная
Прогрессирующая (классическая)
Опухолевая
Абдоминальная
Селезеночная (спленомегалическая)
Пролимфоцитарная
Костномозговая
Стадии
0 – только лимфоцитоз (клинических проявлений нет)
I– присоединяется лимфаденопатия (верхней половины туловища) (ст. А)
II– присоединяется спленомегалия (ст. В)
III– возникновение аутоиммунной гемолитической анемии (ст. С)
IV– аутоиммунная тромбоцитопения (ст. С)
Диагностика хронического лимфолейкоза
Абсолютный лимфоцитоз (за счет зрелых клеток) в периферической крови (5-600*109/л) и в костном мозге (более 30%)
При увеличении л/у, селезенки или печени – диффузная пролиферация лимфоцитов в них
Нормохромная нормоцитарная анемия (в далеко зашедших стадиях – аутоиммунная гемолитическая анемия), тени Боткина-Гумпрехта
Гипогаммаглобулинемия, возможно выявление моноклонального IgM, в моче – белка Бенс-Джонса
Иммунофенотипирование: экспрессия антигенов CD5 иCD23, возможно выявление поверхностногоIgM
Цитогенетический анализ: трисомия 12, реже др.
Возможна положительная проба Кумбса , антитромбоцитарные АТ
Лечение хронического лимфолейкоза
Наблюдение – в нулевую стадию
Специфическая химиотерапия (Циклофосфамид, Хлорбутин, при устойчивости – комбинированные схемы (с включением ГКС), моноклональные антитела): подавляющими дозами и затем интермиттирующая терапия поддерживающими дозами
Лучевая терапия (часто сочетают с последующей трансплантацией стволовых клеток крови или костного мозга)
Спленэктомия (при аутоиммунных осложнениях)
Сопроводительная терапия (санитарно-дезинфекционный режим, антибиотикотерапия, препараты гранулоцитарного или гранулоцитарно-макрофагального колониестимулирующих факторов (Филграстим, Ленограстим, Молграмостим)
Лимфогранулематоз и миеломная болезнь Определение
Лимфогранулематоз – первичное опухолевое заболевание, характеризующееся злокачественной гиперплазией лимфоидной ткани с образованием в лимфатических узлах и внутренних органах лимфогранулём.
Классификация лимфогранулематоза (гистологическая)
Гистологические варианты (могут соответствовать фазам заболевания)
Лимфогистиоцитарный вариант (с преобладанием лимфоидной ткани);
Нодулярный склероз;
Смешанно-клеточный вариант;
Вариант с лимфоидным истощением
(Окончательный диагноз лимфогранулематоза должен быть всегда подтвержден гистологически!)
Классификация лгм по стадиям (клиническая) по Энн Арбор
| I | Вовлечение одной группы л/узлов (N) с любой стороны диафрагмы или одного внелимфатического очага (IЕ), являющегося единственным проявлением заболевания. |
| II | Вовлечение двух или более групп л/узлов по одну сторону диафрагмы (в диагнозе количество указывается арабской цифрой); может вовлекаться селезенка, если группы поражённых лимфатических узлов расположены ниже диафрагмы или один внелимфатический орган по ту же сторону диафрагмы. |
| III | Вовлечение групп лимфатических узлов по обе стороны диафрагмы или одного внелимфатического органа или локализации; может поражаться селезенка (IIIS). |
| IV | Диффузное вовлечение одного или более внелимфатических областей и органов (костный мозг (M), печень (H), лёгкое (L), плевра (Р), кости (О), кожа и п/к клетчатка (D) и т.п.) с ( или без) поражением л/узлов |
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
Хронический лимфоцитарный лейкоз
Лейкоз – злокачественное образование клеток крови, белокровие. Для того чтобы развился лейкоз много не надо. Хватает одной клетки, которая стала злокачественной, за счет своего быстрого роста она делится и таких клеток уже становится очень много. Причинами такого страшного заболевания являются канцерогены (они действуют на костный мозг, который вырабатывает кровяные тела, вследствие этого нормальные клетки не вырабатываются), радиационное облучение, наследственный фактор. Начинается лейкоз очень скрытно. Пациент долгое время может не чувствовать болезни, а когда уже вся кроветворная система заражена этими злокачественными клетками, появляются симптомы. Изначально симптоматика может напоминать инфекционные заболевания, а по мере заражения развивается гемофилия. Общее состояние больного ухудшается, появляется слабость, тахикардия, одышка, анемия. На коже появляются синяки. К смерти пациента приводит кровоизлияния в мозг, в желудочно-кишечный тракт.
Течение заболевания делят на:
- стрый лейкоз – выявить на ранних стадиях легко, в крови находится много несозревших клеток;
- хронический лейкоз отличается от острого своим скрытым течением, происходит это, потому что в крови есть еще нормальные клетки, и процесс течения болезни может маскироваться под симптоматикой других заболеваний. Выявить его непросто.
Хронический лимфоцитарный лейкоз – заболевание, которое возникает из существующих в одной форме В — лимфоцитов, которые присутствуют в периферийной крови. Больше половины пациенты мужского пола, которым за 60.
Хронический лимфоцитарный лейкоз часто встречается у мужчин, связывают появление заболевания также с возрастным изменением, генетикой. Те люди, которые поражены ревматическим заболеванием сердца, не входят в ряды заболевших.
Причины болезни
К появлению заболевания ведет увеличение количества лимфоцитов. Сначала злокачественные лимфоциты увеличиваются в лимфатических узлах. После этого попадая в кровь, они разносятся к печени и селезенке, увеличивая и их. Затем они попадают в костный мозг и убивают нормальные клетки. А костный мозг начинает вырабатывать «неправильные» клетки, которые приводят к анемиям. За счет этого снижается иммунная система и начинает работать неправильно. Нормальные клетки она распознает как чужие и уничтожает их. Это приводит к сбою работы всего организма. Есть В — клеточный (В — лимфоцитарный лейкоз) он встречается гораздо чаще и Т – клеточный – этот редкое заболевание.
Симптомы заболевания
Хронический лимфоцитарный лейкоз, в начале появления не проявляет практически себя, не считая увеличенных лимфоузлов. Может также ощущаться одышка, потеря аппетита, слабость. Некоторые пациенты могут отмечать чувство полного живота, происходит это из-за увеличения селезенки и печени. На ранних стадиях возможно бледность кожных покровов и кровоизлияние под кожу. На поздних стадиях присоединяются грибковые инфекции, бактериальные и вирусные. Бывают случаи, что болезнь находят совершенно случайно. В формуле крови повышенное количество лимфоцитов.
Диагностика лейкоза
 Диагностика лейкоза
Диагностика лейкоза Диагноз устанавливают по анализу крови. При исследовании общего анализа крови видно, что уровень тромбоцитов и эритроцитов сниженный, а лимфоцитов, наоборот, много. Для постановки диагноза исследуют костный мозг. С помощью такого исследования можно поставить диагноз и выбрать эффективное лечение.
Взятие спинномозговой жидкости позволит увидеть лейкозные клетки и начать лечение с помощью введения химических препаратов.
Рентгенологическое исследование дадут возможность врачу увидеть пораженные лимфоузлы средостенья, кости и суставы.
КТ проводят для осмотра лимфатических узлов грудной полости.
МРТ применяют для осмотра спинного и головного мозга.
Лимфолейкоз понятие и виды
Лимфолейкоз (лимфоидный) – злокачественное поражение лимфатической ткани. Заболеванию характерно накапливание патологических лимфоцитов в лимфоузлах, костном мозге и периферической крови. Лимфоидный вид считался раньше детским заболеванием потому как поражал в основном их, на сегодняшний день болезнь чаще встречается у взрослых.
Лимфолейкоз имеет две формы по течению:
- острый (лимфобластный) лейкоз;
- хронический (лимфоцитарный лейкоз).
Острый лимфолейкоз (лимфобластный) ставится диагноз на основе анализа периферийной крови. В ней находят бласты, которые, и указывают на заболевание. В мазке крови имеются «провалы» то есть, есть только зрелые формы и бласты, промежуточных форм нет. В некоторых случаях заподозрить можно болезнь, но для постановления точного диагноза требуется исследовать костный мозг.
Симптомы лимфолейкоза
Острый лимфобластный лейкоз проявляется в виде общего недомогания, за счет снижения аппетита. Больной теряет в весе, повышается температура, кожные покровы бледные за счет развития анемии. Появляется одышка, кашель без выделения мокроты. Возникает боль в животе, рвота. Пациент теряет жидкость и наступает интоксикация организма. Нарушаются жизненно важные функции организма из-за появления в нем токсинов от опухоли. Больной начинает страдать диареей, аритмией, нарушается функция центральной нервной системы. Боль в позвоночнике, конечностях. Пациент становится нервозным, раздражительным. Периферические лимфатические узлы увеличиваются, увеличение происходит и в брюшной полости и грудной. Появляются мелкие кровоизлияние под кожу – петехии.
Причины и стадии лимфолейкоза
Острый лимфобластный лейкоз возникает из-за того что хромосомы начинают менять свою структуру.
Хронический лимфолейкоз заболевание, при котором характерным является накапливание патологических лимфоцитов у крови, которая находится на периферии. По названию можно определить, что хроническая форма, протекает медленнее, чем острая. Успех на выздоровления зависит от того, насколько поражен костный мозг и насколько далеко распространилось злокачественное заболевание.
По течению болезни, онкологи разделяют хронический лимфолейкоз на три стадии:
- Начальная стадия (А), увеличиваются лишь некоторые группы лимфатических узлов, изменений в крови нет. Пациент под присмотром врача. Анемии и тромбоцитопении нет.
- Развернутая (В) – начинаются изменения в крови в виде лейкоцитоза, увеличение лимфатических узлов усиливается, образуются рецидивы инфекции. В этой стадии надо активное и эффективное лечение. Анемии и тромбоцитопении нет.
- Терминальная (С) стадия. Происходит превращение злокачественно образования в хроническую форму. Тромбоцитопения и анемия присутствуют.
Лечение лимфолейкоза
Лечения проводится с помощью:
- Лечение лимфолейкоза
Химиотерапии. Этот метод состоит в ведении в организм сильнодействующих химических препаратов, которые останавливают рост онкоклеток и убивают их. При таком лечении можно использовать препараты, как в инъекционном виде, так и в виде таблетированных форм.
- Хирургическое вмешательство проводят с удалением пораженной части селезенки. Таким способом можно добиться уменьшение опухоли и улучшить содержание нормальных кровяных тел.
- Лечение с помощью моноклональных тел помогает иммунитету бороться с раковыми клетками. Эти лекарственные препараты вводят в вену или подкожно.
- Облучение проводится перед операцией или после ее проведения. Лучевая терапия уменьшает размеры опухоли.
Если костный мозг пораженный, то делают его трансплантацию, переливают кровь, назначают антибиотики и проводят симптоматическое лечение. Кстати трансплантация является единственным способом вылечить больного от хронической формы заболевания.
Если опухоль развивается очень быстро, то врач назначает препараты, которые некротизируют опухоль – цитостатики и гормоны.
Диагностика лимфолейкоза
Для постановления диагноза также понадобится:
- Цитогенетический анализ. Анализируют хромосомы, смотрят на их изменения. Некоторые хромосомы, которые имеют важное значения, могут отсутствовать. Видя это, врач подбирает наиболее эффективный метод лечения.
- Поточная цитометрия. Используют онкомаркеры, которые окрашивают онкоклетки в определенный цвет, таким способом можно узнать из каких именно клеток (Т или В – лимфоцитов) возникла опухоль.
- Проводят также биопсию лимфатических узлов. Врач осматривает кожу, находит воспаленный лимфоузел, обезболивают этот участок и путем надреза извлекают узел для исследования.
- Пункция костного мозга и кости. Берется забор биологических веществ из тазовой или грудной кости. Затем под микроскопом исследуют жидкости на наличие патологических клеток.
Прогноз на выздоровление
Пациентам стоит организовать правильно свой режим сна и отдыха, нельзя использовать процедуры в виде приема грязей, нельзя переутомляться. Надо составить свой день так, чтобы организм не уставал. Запрещается вакцинация таким больным, потому как иммунная система очень ослаблена, а вакцины это живые возбудители болезни. Питание должно быть максимум полезным. Можно кушать мясо, печень. Стоит употреблять продукты, в которых содержится много железа (крыжовник, чеснок, картошку, виноград, лук, гречку). Кушать свежие овощи шпинат, свеклу. Фрукты вишни, землянику, смородину и др.
Так как течение заболевания медленное, то прогноз на выздоровления зависит от злокачественности болезни, ее стадии. Стадия определяется по анализу крови, наличии патологических клеток в костном мозге. Определяется по размеру селезенки, печени, по наличию анемии. Умирает пациент из – за того, что костный мозг не выполняет свою функцию. Клетки, которые необходимы для перенесения кислорода (эритроциты) не вырабатываются, и клетки различных органов начинают отмирать. Иммунная система не в силе бороться с инфекцией.
Как и все остальные болезни, лимфолейкоз лучше поддается лечению когда он обнаружен на начальных стадиях, а для того чтобы его вовремя увидеть, нужно периодически сдавать хотя бы общий анализ крови. Не стоит избегать профилактических медицинских осмотров. Так как точных причин возникновения болезни никто назвать не может, стоит внимательно прислушиваться к своему организму. Потому как считают, что болезнь вызывает специальные вирусы. Они проникают в организм, и находятся в нем. Под воздействием негативных факторов для организма, эти вирусы начинают действовать. Снижают иммунитет, попадают к незрелым клеткам крови и изменяют их ДНК – структуру. Вследствие этого они начинают размножаться и расти. Получается не контролированный их рост. Таким образом, они вытесняют нормальные клетки. И организм дает сбои, потому как иммунитет ослаблен и восприимчив к инфекционным и другим различным болезням.
Хронический лимфолейкоз — кто в группе риска?
Гемобластозы, или лейкозы – опухоли, состоящие из клеток крови, часто ошибочно называют рак крови. Несмотря на, без сомнения, злокачественную природу патологии, лейкемии (еще одно название этой группы болезней), как уже было сказано, происходят от клеток крови в различной стадии созревания. Тогда как рак, в традиционном понимании этого слова — опухоль, происходящая из эпителия: кожи или слизистых оболочек, в том числе выстилающих полости внутренних органов.
Если обычные болезни делят на острые или хронические исходя из продолжительности, то лейкозы различаются по степени зрелости клеток опухоли. Клетки крови в своем развитии проходят несколько стадий созревания. Если опухоль состоит из молодых – бластных клеток, лейкоз называется острым. Если большинство клеток опухоли представляют собой зрелые формы – это хроническая лейкемия.
Классификация хронических лейкозов
Лейкозы подразделяются на группы исходя их того, какой вид клеток крови начал бесконтрольно размножаться. По этому параметру хронические лейкозы делятся на:
- миелолейкоз;
- мегакариоцитарный лейкоз;
- эритромиелоз;
- моноцитарный;
- макрофагальный;
- тучноклеточный;
- лимфолейкоз;
- сублейкемический миелоз;
- эритремия;
- волосатоклеточный лейкоз;
- парапротеинемические гемобластозы.
Хронические лейкозы чаще всего возникают у взрослых и пожилых людей. Самый частый из них — хронический лимфолейкоз.
Хронический лимфоцитарный лейкоз
Он же хронический лимфолейкоз – патология преимущественно пожилых людей: в Европе медиана возраста пациентов составляет 69 лет. В России продолжительность жизни в целом ниже, поэтому возрастная группа, в которой патология встречается, чаще всего определяется как пациенты 40-60 лет. Хронический лимфолейкоз у детей встречается крайне редко, самая частая патология в этом возрасте – острый лимфоидный лейкоз.
Хронический лимфоцитарный лейкоз — это злокачественная патология лимфатической ткани, при которой субстрат опухоли состоит преимущественно из зрелых лимфоцитов и обязательно создает очаги поражения в костном мозге.
По клиническим проявлениям хронический лимфоцитарный лейкоз может быть:
- с преобладанием поражения костного мозга;
- с преобладанием поражения лимфатических узлов;
- с преобладанием поражения селезенки;
- с выраженными атоимунными осложнениями (тромбоцитопения, анемия).
Симптоматика
Хронический лимфолейкоз развивается очень медленно и симптомы могут не проявляться годами и даже десятилетиями, изменяя лишь показатели анализа крови. Процесс начинается с постепенного увеличения количества лимфоцитов в крови, что может быть диагностировано только лабораторно. По мере роста лимфоцитоза начинает снижаться количество других видов клеток крови: развивается анемия, возникает дефицит тромбоцитов (тромбоцитопения). Начальные симптомы анемии могут одновременно стать и первыми клиническими проявлениями лейкоза, но чаще всего они тоже проходят незамеченными. Это такие признаки как:
- слабость;
- бледность кожи и слизистых;
- одышка при физической нагрузке;
- потливость.
Также может подниматься температура, начаться немотивированная потеря веса.
Огромное количество лимфоцитов (в тяжелых случаях может достигать 600 х 109/л при норме до 4,8) не только заполняют кровь. Они инфильтрируют костный мозг и оседают в лимфоузлах, которые начинают увеличиваться, причем равномерно по всем группам тела, в том числе брюшной полости, средостении. Хронический лимфоцитарный лейкоз отличается от большинства других патологий, вызывающих увеличение лимфоузлов тем, что при нем лимфатические узлы остаются совершенно безболезненными. Их консистенция напоминает тесто, а размеры могут достигать 10 – 15 см. Конечно, если такие огромные лимфатические узлы находятся в средостении, то они могут сдавить жизненно важные органы, вызывая дыхательную и сердечно-сосудистую недостаточность.
Вслед за лимфоузлами увеличивается селезенка – тоже из-за инфильтрации лимфоцитами. Потом печень. Эти два органа обычно не разрастаются до гигантских размеров, хотя бывают и исключения.
Хронический лимфолейкоз вызывает иммунные нарушения. Лейкемические B — лимфоциты перестают вырабатывать антитела. А поскольку количество нормальных клеток резко уменьшается, антител становится недостаточно для того, чтобы сопротивляться бактериальным инфекциям, частота которых увеличивается. Чаще всего поражаются дыхательные пути – возникают тяжелые бронхиты, распространенные пневмонии, плевриты. Нередки и инфекции мочевыводящих путей или поражения кожных покровов. Еще одно следствие измененного иммунитета – появление антител к собственным эритроцитам, что вызывает гемолитическую анемию, которая клинически проявляется желтухой. Недостаток тромбоцитов вызывает кровотечения – от точечных кровоизлияний до массивных носовых, желудочно-кишечных, у женщин – маточных.
Как долго будет протекать хронический лимфоцитарный лейкоз, заранее предсказать невозможно – темпы развития варьируются в широких пределах. Основные причины смерти:
- кровотечения;
- кровоизлияния в головной мозг;
- инфекционные осложнения;
- анемии;
- сдавление жизненно важных органов увеличенными лимфатическими узлами.
Лабораторная диагностика
Как уже упоминалось, при хроническом лимфолейкозе первые симптомы – изменение показателей крови. Зачастую диагноз ставится именно на этой стадии. Картина крови при хроническом лимфолейкозе характеризуется такими изменениями как:
- лейкоцитоз от 10-15х109/л;
- преобладание лимфоцитов (85-90%);
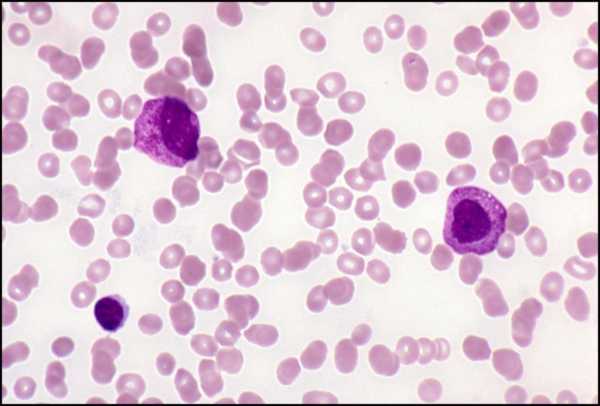
- появление пролимфоцитов и теней Гумпрехта – Боткина, разрушенных при приготовлении мазка ядер лимфоцитов;
- анемия;
- тромбоцитопения.
Стадии хронического лимфолейкоза определяются согласно классификации Binet.
- A. Гемоглобин выше 100 г/л, тромбоцитов больше 100 х 109/л, лимфоузлы увеличены в 1-2 областях.
- B. Показатели крови аналогичны предыдущей стадии, лимфатические узлы увеличены в 3 и более областях.
- C. Гемоглобина меньше 100 г/л, тромбоцитов меньше 100 х 109/л.
Медиана выживаемости при стадии А – более 120 месяцев, B – 61 месяц, С – 32 месяца.
Лечение хронического лейкоза
Если при большинстве онкологических заболеваний упущенное время может в буквальном смысле означать упущенную жизнь, то лечение хронического лимфолейкоза назначается далеко не всегда. Примерно у 40% пациентов эта форма лейкоза развивается медленно, и при обнаруженной на стадии А патологии прогнозируемая продолжительность жизни ничем не отличается от прогноза для среднестатистического человека того же пола и возраста. В этом случае предпочтительней выжидательная тактика. Препараты, используемые для лечения рака крови, имеют тяжелые побочные действия. Поэтому В-клеточный хронический лимфолейкоз имеет строгие показания к лечению:
- Беспричинное похудание на 10% и более за последние 6 месяцев;
- Потеря способности работать, и, тем более, обслуживать себя самостоятельно;
- Беспричинный субфебрилитет (температура около 37-37.5);
- Рост анемии или дефицита тромбоцитов;
- Появление аутоимунной анемии или тромбоцитопении;
- Селезенка выступает из-под реберной дуги на 6 и более см. (в норме она не прощупывается);
- Массивное увеличение лимфоузлов, усиление процесса;
- Количество лимфоцитов удвоилось менее чем за 6 месяцев.
В основном лечение направлено на устранение осложнений. Сам по себе рак крови этой разновидности пока считается неизлечимым. А с учетом того, что пациенты, как правило, весьма почтенного возраста, лечение подбирается исходя из общего состояния больного. Химиопрепараты используются в минимально токсичных дозировках, чаще всего с паллиативной целью (продление жизни и избавление от страданий). Активно комбинированную химиотерапию, направленную на достижение ремиссии используют для лечения относительно молодых и физически активных пациентов.
Хронический лимфолейкоз - классификация, диагноз, лечение
11 Марта в 13:47 1107
Хронический лимфолейкоз (ХЛЛ) является наиболее частым видом лейкоза у лиц пожилого возраста в странах Европы и Северной Америки. Ежегодная заболеваемость ХЛЛ в этих странах составляет 3-3,5 на 100000 населения, причем мужчины болеют чаще женщин. В странах Азии и Африке В-ХЛЛ является редким заболеванием, в странах Азии преобладает Т-клеточный хронический лимфолейкоз; отмечено повышение его частоты среди евреев. Средний возраст к началу заболевания составляет 55 лет, около 70% пациентов заболевают в возрасте 50-70 лет. Роль наследственного фактора подтверждается повышенной частотой заболеваемости ХЛЛ у кровных родственников как по горизонтальной, так и по вертикальной линиям.Не удалось установить роль каких-либо мутагенных факторов в развитии ХЛЛ - химических агентов, ионизирующего излучения, вирусов, алкилирующих препаратов. Согласно классификации ВОЗ (2001 г.) В-клеточный хронический лимфолейкоз относится к опухолям периферических органов иммунной системы и в целом составляет около 20% всех неходжинских лимфом (НХЛ). ХЛЛ в 95% случаев в Европе и США имеет В-клеточный и в 5% случаев - Т-клеточный фенотип.
Иммунофенотипическая характеристика В-клеточного хронического лимфолейкоза позволяет рассматривать его как опухоль, морфологическим субстратом которой являются первично активированные В-лимфоциты, прошедшие первичную активацию в паракортикаль-ной зоне лимфоузла. При В-клеточном ХЛЛ опухолевые лимфоциты имеют фенотип CD3-,CD10-, CD5+, CD19+, CD20+, CD23.Экспрессия CD5+ является обязательным маркером В-клеточного ХЛЛ, а экспрессия CD23+ позволяет отличить хронический лимфолейкоз от лейкемизации лимфомы зоны мантии (ЛЗМ). Для лимфоцитов при ХЛЛ, как и при других формах НХЛ, характерна слабая экспрессия легких цепей поверхностных иммуноглобулинов. При цитогенетическом анализе во многих случаях ХЛЛ можно обнаружить хромосомные аберрации.
Наиболее частыми маркерами являются трисомия Хр12 (16%), а также делеции Xp11q и Хр17р (локализация гена тумор-супрессора опухолевого роста р53). Наличие двух последних изменений относится к НФП в связи с отсутствием клинического эффекта от проводимой полихимиотерапии (ПХТ). В 55% случаев хронический лимфолейкоз определяется делеция 13q, которая не влияет на прогноз.
Предположение о том, что ХЛЛ является болезнью накопления длительно живущих иммунонекомпетентных малых лимфоцитов получило подтверждение и объяснение. Обнаружено, что у большинства больных ХЛЛ имеется гиперэкспрессия гена BCL-2, играющего главную роль в предотвращении апоптоза, причем уровень экспрессии нарастает по мере прогрессирования заболевания. Другим важным фактором риска является мутация генов, ответственных за синтез тяжелых цепей иммуноглобулинов.
ХЛЛ развивается медленно, в ранних стадиях у пациентов нет специфической симптоматики. Предположение о наличии ХЛЛ может быть высказано на основании изменений в анализе крови - наличие лейкоцитоза с абсолютным лимфоцитозом. Иногда первым клиническим симптомом является лимфоаденопатия; лимфоузлы имеют тестоватую консистенцию, безболезненные.При рентгенисследовании можно выявить увеличение лимфоузлов средостения, при ультразвуковом исследовании (УЗИ) - увеличение абдоминальных и забрюшинных лимфоузлов. Увеличение селезенки у большинства больных появляется позже, чем увеличение лимфоузлов, еще позднее увеличивается печень. Не отмечается корреляции степени лимфоидной инфильтрации костного мозга, уровня лейкоцитов и размеров лимфоузлов, селезенки и печени.
Гематологические изменения характеризуются постепенно нарастающим лейкоцитозом, иногда до 1000,0х109/л и повышением количества лимфоцитов в лейкограмме до 85-99%, обычно с наличием единичных пролимфоцитов. Характерно для хронического лимфолейкоза наличие в мазке крови клеток Боткина-Гумпрехта - полуразрушенных при приготовлении мазка ядер лимфоцитов.
При исследовании костномозгового пунктата выявляется лимфоцитоз с уменьшением числа гранулоцитов и эритрокариоцитов; уже на ранних стадиях болезни в миелограмме обнаруживается повышение уровня лимфоцитов более 40% с постепенным (без лечения) их нарастанием. Биопсия костного мозга показывает нодулярную, диффузную или смешанную инфильтрацию.Число эритроцитов, тромбоцитов и уровень Нв в ранних стадиях заболевания обычно в пределах нормы. Эти показатели в поздних стадиях ХЛЛ обычно снижены либо за счет уменьшения плацдарма нормального кроветворения в костном мозге вследствие вытеснения здоровых ростков патологическими лимфоцитами, либо в связи с присоединением аутоиммунных осложнений типа аутоиммунной гемолитической анемии (АИГА) или парциальной красноклеточной аплазии (ПККА). У части пациентов может развиваться гемодермия по типу эритродермы вследствие инфильтрации кожи лимфоцитами.
В Европе принята классификация стадий ХЛЛ по J.Binnet (1981 г.):• стадия А: при наличии лимфоцитоза крови более 15,0х109/л и более 40% лимфоцитов в костном мозге, позволяющего установить диагноз, содержание Нв - более 100,0 г/л, тромбоцитов - более 100,0x10%, имеется увеличение лимфоузлов в 1-2 областях;
• стадия В содержание Нв и тромбоцитов такое же, как в стадии А, но имеется увеличение лимфоузлов в 3 и более областях;• стадия С содержание Нв ниже 100 г/л и тромбоцитов - менее 100,0х109/л при любом количестве зон с увеличенными лимфоузлами и независимо от увеличения органов.
В настоящее время диагноз ХЛЛ можно выставить при наличии лимфоцитоза в крови более 5,0х109/л при доказанной клональности лимфоцитов и при наличии более 30% лимфоцитов в костный мозг (КМ). При ХЛЛ, помимо лейкемической лимфоидной пролиферации, важную роль играют количественные и качественные изменения как патологических, так и нормальных лимфоцитов. Опухолевые В-лимфоциты продуцируют сниженное количество нормальных иммуноглобулинов. Уменьшение количества нормальных В-лимфоцитов обусловливает гипогаммаглобулинемию, что ведет к тяжелому течению инфекций. Эта проблема играет при ХЛЛ особую роль, поскольку инфекционные осложнения остаются главной причиной смерти больных ХЛЛ даже в отсутствие признаков прогрессирования процесса. Наиболее часто возникают инфекции дыхательных путей, бактериальные инфекции мочевыводящих путей, кожных покровов и мягких тканей, herpes zoster (нередко принимает генерализованную форму с развитием сливных поражений кожи и распространением на внутренние органы). Лечение инфекционных осложнений у больных хроническим лимфолейкозом проводится по общим правилам лечения инфекций у больных со снижением иммунитета.Другим важным следствием иммунных нарушений при ХЛЛ являются аутоиммунные осложнения. Наиболее часто развивается АИГА (у 10-25% больных), чаще с обнаружением антител класса IgG, реже - класса IgM. Очень редко развивается иммунная тромбоцитопения, при которой могут возникать опасные для жизни нарушения гемостаза.
Крайне редким осложнением является ПККА с полным отсутствием эритрокариоцитов в костном мозге и ретикулоцитов в периферической крови. Хороший эффект в лечении ПККА у ряда больных оказывает циклоспорин А в суточной дозе 150-200 мг или пульс-терапия (высокие дозы ГКС+циклофосфамид).Аутоиммунные процессы чаще возникают у больных с развернутой клинико-гематологической картиной ХЛЛ. Ведущим в их терапии является применение высоких доз глюкокортикостероидов (ГКС), предупреждение развития синдрома диссеминированного внутрисосудистого свертывания крови (ДВС-синдрома) при АИГА и, при необходимости, трансфузии тромбоконцентрата при тромбоцитопении.
В терапии ХЛЛ важнейшим вопросом является определение времени начала терапии. В стадии А по J.Binnet, т.е. при минимальных проявлениях болезни сохраняется тактика «наблюдай и жди».
Лечение больного хронического лимфолейкоза начинают при признаках стадии В по J.Binnet, не дожидаясь появления симптомов декомпенсации процесса.Наличие следующих признаков является необходимым для незамедлительного начала цитостатической терапии:
- наличие общих симптомов интоксикации: усталость, потливость, снижение массы тела, - анемия или тромбоцитопения вследствие лейкемической инфильтрации КМ, - аутоиммунная анемия или тромбоцитопения, - массивная лимфоаденопатия или спленомегалия с компрессионным синдромом, - число лимфоцитов периферической крови выше 150,0x10%, - удвоение абсолютного числа лимфоцитов в крови менее, чем за 12 месяцев, - лимфоцитарная инфильтрация КМ - более 80%, - наличие комплексных хромосомных аберраций, - стадия С по J.Binnet. С 60-х годов XX века при ХЛЛ начала применяться методика первично-сдерживающей терапии, задачей которой являлось сдерживание роста патологического клеточного клона и предупреждение прогрессирования болезни. Ее назначали при умеренных клинико-гематологических проявлениях заболевания: лейкоцитоз до 30,0-50,0x10%, незначительной лимфоаденопатии и/или спленомегалии и при тенденции к прогрессированию заболевания. Обычно назначался хлорбутин (лейкеран) в дозе 10-20 мг в неделю или циклофосфамид в дозе 150-200 мг/сутки с коррекцией дозы в дальнейшем в зависимости от уровня лейкоцитов. Однако такая терапия (монотерапия или в сочетании с ГКС - хлорбутин 10-20 мг в сутки + преднизолон 30-70 мг в сутки курсами по 7-14 дней с интервалами 2-1 недели) позволяла получить лишь частичные ремиссии, в основном снижалось количество лейкоцитов без особого уменьшения величины лимфоузлов и селезенки. Поэтому с 70-х гг. XX века были разработаны комбинированные лечебные схемы. Длительное время «золотым стандартом» в лечении являлась ПХТ по протоколам СОР, CHOP и САР. В настоящее время они применяются в качестве терапии второй линии или терапии у пациентов с агрессивными формами ХЛЛ. Однако рандомизированные исследования показали, что длительная безрецидивная и общая выживаемость при применении вышеуказанных протоколов ПХТ не изменилась достоверно в сравнении с таковыми при лечении хлорбутином и преднизолоном. Ситуация в терапии ХЛЛ изменилась в конце 80-х гг. XX века в связи с синтезом и внедрением в клиническую практику аналогов пуриновых нуклеозидов - флюдарабина, кладрибина и пентостатина. Эти препараты воздействуют как на делящиеся, так и на покоящиеся лимфоидные клетки, чем и обусловлена их эффективность при лечении медленно текущих лимфом, к которым относится и хронический лимфолейкоз. Препараты ингибируют ряд важнейших клеточных ферментов, нужных для синтеза РНК и ДНК: ДНК-примазу, ДНК-полимеразу, ДНК-лигазу, рибонуклеотидредуктазу. Это ведет к прекращению синтеза и нарушению построения цепи ДНК, а также к нарушению синтеза РНК. В настоящее время применение аналогов пуриновых нуклеозидов рекомендуется в качестве терапии первой линии у пациентов с ХЛЛ: терапия по протоколам FC, FCM, FMD.Бендамустин применятся для лечения как ХЛЛ, так и при рецидиве вяло текущих неходжинских лимфом, не отвечающих на обычную терапию или прогрессирущих в течение 6 месяцев после терапии с использованием ритуксимаба. В настоящее время он применяется для лечения НХЛ, лимфомы Ходжкина, хронического лимфолейкоза и множественной миеломы.
Химическая структура бендамустина обуславливает двойное воздействие, сходное как с действием алкилирующих агентов, так и аналогов пуриновых нуклеозидов. Препарат активирует зависимый от р53 стрессовый путь, приводящий к апоптозу и ингибированию механизмов контроля митоза. Бендамустин назначают в дозе 120 мг/м в 1-2 дни каждые три недели и проводят всего 6 циклов терапии. Для быстрого снижения количества лейкоцитов можно применять лейкоцитаферез. В последние годы в клинической практике применяются моноклональные антитела против антигенов В- и Т-клеток (ритуксимаб, алемтузумаб). В связи с тем, что эффект ритуксимаба лимитирован степенью экспрессии CD20 на клетках ХЛЛ, при рефрактерном или при рецидивирующем течении ХЛЛ рекомендуется терапия по протоколу FCR, особенно в случаях первично диагностированного хронического лимфолейкоза. Специально в рефрактерных случаях (часто ассоциированных с делецией р53) высокоэффективен алемтузумаб (Campath) - антитела к CD52. Его применяют 3 раза в неделю, начиная с минимальной дозы 3 мг/день с постепенным повышением дозы при каждом введении до достижения дозы 30 мг с частотой введения подкожно 3 раза в неделю. Применение протокола FluCam (флюдарабин 25 мг/кв.м. в/венно 1-3 дни + Campath 30 мг 3 раза в неделю на протяжении 6 недель) оказывается более эффективным, но чревато проявлениями тяжелой иммуносупрессии. Для лечения пациентов с рецидивами ХЛЛ может применяться люмиликсимаб, который является моноклональным aнти-CD23-aнтигеном. Его применяют в сочетании с ритуксимабом, циклофосфамидом и флюдарабином (протокол L-FCR). Лечение по этому протоколу эффективно снижает количество опухолевых клеток в периферической крови независимо от уровня экспрессии CD23 и CD38. Эффективным в терапии ХЛЛ является применение маломолекулярных ингибиторов антиапоптотических протеинов семейства BCL-2, одним из которых является абатоклакс.Для пациентов с большой массой селезенки и гиперспленизмом может быть рекомендована спленэктомия. Пациентам молодого возраста с агрессивным течением заболевания можно рекомендовать ауто- трансплантация гемопоэтических стволовых клеток (ТГСК); при наличии совместимого по HLA-системе донора - алло-ТГСК или алло- трансплонтация костного мозга (ТКМ).
А.Т. Фиясь Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе