Скт сердца у ребенка
Скт сердца у ребенка - Все про гипертонию
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день...
Читать далее »
У новорожденных малышей могут быть диагностированы самые разные врожденные пороки и аномалии развития сердца. Часть из них не совместимы с жизнью, другие требуют хирургической коррекции, иначе тяжелого нарушения гемодинамики не избежать, третьи — относительно безопасны и протекают бессимптомно.
Аневризму МПП (межпредсердной перегородки) относят к так называемым малым аномалиям сердца, не вызывающим существенных расстройств кровообращения и изменения работы сердца. Это редкий порок новорожденных детей, встречающийся не более чем в 1% случаев и протекающий обычно бессимптомно.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
Молодые мамы, столкнувшиеся с такой аномалией у своего ребенка, не должны впадать в панику — аневризма МПП не представляет угрозы для жизни, дети развиваются правильно, а по мере роста аневризма самопроизвольно может исчезнуть. Беспокойство должны вызывать случаи, когда аневризма сочетается с более серьезным пороком, который и определит симптоматику и тактику ведения малыша.
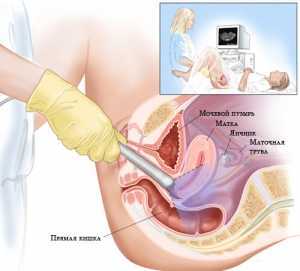
Аневризма МПП бывает изолированной, но значительно чаще она сочетается с другими пороками сердца и открытым овальным окном, поэтому симптоматика может быть разнообразной, но не всегда связана именно с аневризмой. Заподозрить патологию у новорожденного позволяет ультразвуковое исследование, которое может быть проведено в первые дни и недели жизни.
Причины и разновидности аневризмы МПП
Аневризма межпредсердной перегородки с точки зрения анатомии — это выпячивание стенки миокарда между предсердиями в ту или иную сторону. Обычно пролабирует стенка в области так называемой овальной ямки, которая осталась после зарастания овального окна, так как там сердечная мышца недостаточно прочна и при неблагоприятных условиях способна выпячиваться.
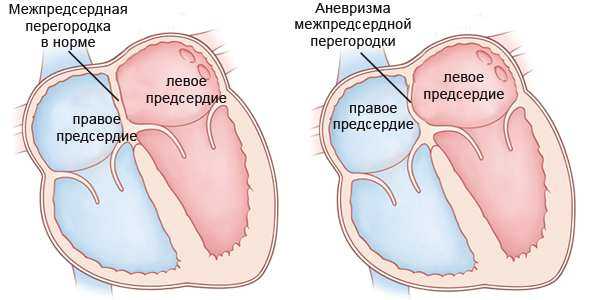
У плода легочный круг кровообращения не функционирует, ведь освоение процесса дыхания возможно только после рождения малыша. Газообмен внутриутробно поддерживается за счет функционирующей плаценты, а овальное окно, расположенное в перегородке между предсердиями, необходимо для перенаправления крови из правого предсердия в левое и далее большой круг. После рождения отверстие практически сразу закрывается, новорожденный дышит собственными легкими, а кровь из одного предсердия в другое уже не попадает.
Нередко специалисты-неонатологи наблюдают несвоевременное закрытие овального окна, которое может функционировать довольно долго — до года и более. В таких случаях недостаточно прочный миокард имеет больше шансов выпятиться в ту или иную сторону под действием давления кровяных потоков. Сочетание аневризмы с дефектом перегородки более типично, нежели изолированная аневризма МПП, хотя и последний вариант возможен.
Причины аневризмы МПП точно не установлены, а масштабные исследования в этой области не проводились. Предполагается роль и внешних, и внутренних факторов. Это могут быть перенесенная в течение беременности инфекция, неблагоприятные экологические условия. Не исключается роль стрессов, недостатка витаминов у будущей мамы, внутриутробной гипоксии.
Несмотря на отсутствие достоверных данных об этиологии аневризмы МПП, большинство ученых все же склоняются к единому мнению, что в основе появления аномалии ключевое значение имеет развитие соединительной ткани во внутриутробном периоде.
Соединительнотканная основа сердца может быть незрелой, недостаточно прочной, коллагеновых волокон может быть недостаточно либо изменено их соотношение. Если эти явления не носят наследственного характера, а спровоцированы индивидуальными особенностями развития, то, скорее всего, по мере роста ребенка сердце придет в норму. При наследственных дисплазиях соединительной ткани дело обстоит значительно хуже: в сердце обнаруживается три и более аномалии или более тяжелые пороки, в других органах также есть признаки соединительнотканной дисплазии.
У детей дошкольного возраста с функционирующим овальным окном можно обнаружить внезапно появившуюся аневризму. После рождения у таких пациентов диагностируют наличие дефекта, но аневризмы у них нет. При быстром зарастании отверстия фиброзно-мышечной тканью происходит провисание тонкой стенки в ту или иную сторону — возникает аневризма МПП.
У взрослых аневризма МПП может быть следствием обширного инфаркта, но такое состояние встречается крайне редко. Инфаркты больше свойственны миокарду желудочков, предсердия же страдают исключительно редко.
Условно аневризмой считается такое выпячивание стенки межпредсердной перегородки в одно из предсердий, когда по данным УЗИ оно более 1 см, но и меньшие по величине выбухания тоже будут условно считаться аневризмами.
В зависимости от направления прогиба межпредсердной перегородки, выделяют три типа аневризм МПП:
- С прогибанием в правое предсердие (встречается наиболее часто);
- Прогиб в левое предсердие;
- S-образная аневризма, когда одна часть перегородки пролабирует в одну сторону, а другая — в противоположную.
Направление провисания межпредсердной стенки не оказывает влияния на симптоматику и течение порока, но чаще обнаруживают правостороннее направление, так как давление в левом предсердии выше, чем в правом, и стенка сердца отклоняется под его действием в противоположную сторону.
С точки зрения клиники гораздо большее значение имеет не направление аневризмы, а ее сочетание с другими дефектами — открытым овальным окном, дефектом стенок сердца и другими врожденными пороками, которые могут вызвать нарушение внутрисердечной и органной гемодинамики с соответствующей симптоматикой.
Кровоток в сердце при аневризме меняется не всегда. Если она не сопровождается наличием дефекта в перегородке, а пролабирование не достигает критических значений, то циркуляция крови по камерам будет нормальной.
Сильно выраженное выбухание может способствовать деформации и сдавлению клапанных створок, а аневризма большой площади, выпячивающаяся в правое предсердие, затрудняет опорожнение этой камеры сердца и, соответственно, нормальное заполнение правого желудочка, что влечет расстройства кровотока.
Аневризма, сформированная при целостной стенке между предсердиями, протекает без сброса крови из одной камеры в другую, прогноз при этом благоприятный, а симптоматика чаще всего отсутствует. Если есть дефект, не закрытое вовремя овальное окно либо произошел разрыв аневризматического выпячивания, то кровь будет поступать в правое предсердие из левого, и в правой половине сердца и легочном стволе начнет возрастать давление — легочная гипертензия.
Проявления аневризмы межпредсердной перегородки
Как и большинство других малых аномалий, не сопровождающихся наличием иных пороков сердца, аневризма межжелудочковой перегородки протекает бессимптомно. О ней становится известно после планового ультразвукового исследования сердца малыша первого года жизни.
Бессимптомная аневризма никак не сказывается на развитии ребенка — в физическом и психоэмоциональном плане он ничем не будет отличаться от сверстников. Об этом обязательно должен сказать педиатр родителям малыша, чтобы избежать излишних волнений и ненужных обследований.
Дети с аневризмой, пролабирующей слева направо, больше подвержены аритмиям. Это связано с тем, что выпячивание способствует более сильным колебаниям миокарда правого предсердия, где находятся элементы проводящей системы. Раздражение водителей ритма и вызывает расстройства ритмичности сокращений сердца.
Если аневризма большая, а, тем более, сочетается с другими анатомическими дефектами в сердце, то клинические проявления появятся уже у новорожденного малыша. В других случаях аномалия может манифестировать при повышении физической нагрузки, при усилении роста в подростковом периоде, гормональных перестройках.

Симптомами аневризмы МПП у ребенка могут быть:
- Тахикардия, синюшность носогубного треугольника, одышка при грудном кормлении у новорожденных и детей первых месяцев жизни, быстрая утомляемость и одышка при физических занятиях, активной игре, купании;
- В подростковом периоде в связи с ускорившимся ростом, гормональными колебаниями, интенсивными нагрузками в школе, спортивных секциях возможны тахикардия, утомляемость, головокружения, нарушения ритма сердца, чувство дискомфорта и замирания в груди, возможны и боли в сердце;
- При сочетании аневризмы и открытого отверстия в перегородке на первый план выходят признаки застоя и повышения давления в малом круге — одышка, частые воспалительные заболевания бронхолегочной системы, не исключены нарушения ритма сердца из-за гипертрофии и растяжения стенок правой половины сердца.
В подростковом возрасте наличие аневризмы МПП может сопровождаться симптомами вегетативной дисфункции — появляется потливость, тошнота, головокружения, обмороки, субфебрильная лихорадка. Дети старшего возраста могут жаловаться на боли в животе, нарушения пищеварения, головные боли, частую усталость и сонливость. Малыши, у которых повышается тонус вегетативной нервной системы, могут стать беспокойными, плаксивыми, вялыми или чрезмерно возбужденными, часто нарушается сон и снижается аппетит.
Крупные аневризмы без сброса крови, выпячивания на фоне дефектов перегородки, вызывающие застой крови в легочном круге, провоцируют частые воспалительные процессы в дыхательных путях, что проявляется у детей первых лет жизни бронхитами, пневмониями, рецидивирующими респираторными вирусными заболеваниями.
Аневризма МПП может сопровождаться некоторыми осложнениями, наиболее опасными считаются ее разрыв и внутрисердечный тромбоз, который может стать причиной эмболии с закупоркой других сосудов (головного мозга, например).
Случаи разрыва встречаются не так уж часто, но если это произошло, то врачи предпочитают наблюдение и тщательный контроль кровообращения, нежели операцию, которая сопряжена с большим риском. При разрыве в области аневризмы последствия вряд ли будут фатальными, поэтому риск не оправдан.
Диагностика и лечение аневризмы МПП
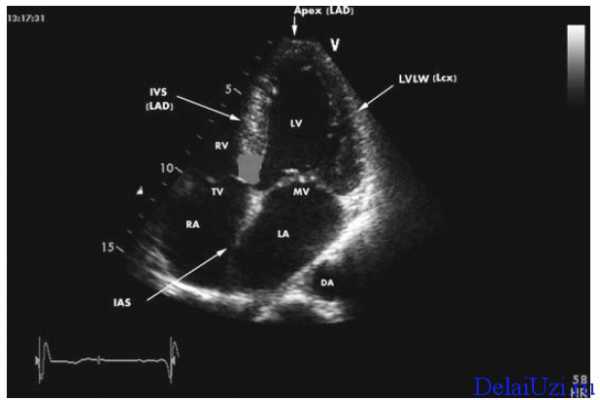
Для выявления аневризмы МПП используется ультразвуковое исследование сердца. Оно безболезненно и безопасно даже самым маленьким пациентам, поэтому проводится уже в роддоме или поликлинике при наблюдении в течение первого года жизни малыша. Для оценки внутрисердечного кровотока УЗИ дополняется допплерографией. Показанием к обследованию новорожденного или ребенка раннего возраста может стать выслушивание шума в сердце при аускультации, который чаще всего связан с наличием дефекта в перегородке или открытым овальным окном.
При подозрении на наличие более тяжелых структурных аномалий сердца показаны дополнительные исследования — чреспищеводное УЗИ, КТ, катетеризация полостей сердца.
Видео: аневризма МПП на ЭхоКГ (УЗИ сердца)
Большинство малых аномалий сердца не требуют специфического лечения, но наблюдение у кардиолога считается обязательным. При бессимптомном течении аневризмы МПП без сброса крови лечение не назначается, а ребенка раз в год осматривает кардиолог после проведения плановой эхокардиографии.
Детям с аневризмой межпредсердной перегородки очень важно организовать общеоздоровительные мероприятия. Следует наладить режим труда и отдыха, исключающий сильные физические и психоэмоциональные нагрузки, особенно — в периоды интенсивного роста, обеспечить условия для достаточно продолжительного сна, показаны прогулки на свежем воздухе и питание с высоким уровнем витаминов, белка, микроэлементов.
Полезными считаются водные процедуры, массаж, при сочетании аневризмы с вегетативной дисфункцией целесообразны работа с психотерапевтом, аутотренинги, электросон. Для нормализации метаболизма в миокарде назначается электрофорез с магнезией.

Вопрос занятий физкультурой и конкретными видами спорта очень волнует многих родителей, столкнувшихся с аневризмой МПП у своего ребенка. Особенно остро он может стать для детей, желающих посещать различные спортивные секции. Решить, безопасны ли такие тренировки для конкретного ребенка, может только кардиолог исходя из размеров аневризмы и наличия или отсутствия сопутствующих изменений в сердце.
При аневризме МПП не рекомендуются очень активные спортивные занятия с высоким уровнем травматизма, но обычная физкультура и, тем более, ЛФК будут только полезны, ведь они нормализуют общий тонус, улучшают кровообращение и способствуют правильному формированию сердечно-сосудистой системы у детей.
Противопоказаниями к занятиям физкультурой могут стать аритмии, жалобы на боли в области сердца, сердцебиения, которые часто беспокоят растущих подростков.
Некоторые родители, наоборот, склонны чрезмерно ограничивать ребенка от всяческих занятий, что в корне неверно и вредно. Во-первых, при этом тормозится общее физическое развитие, а во-вторых — ограничение или исключение физкультуры из жизни ребенка может повлечь изменение в его характере, привычках, дисциплинированности, способствовать формированию комплекса неполноценности или неуверенности в себе. При аневризме МПП родителям важно создать такие условия, чтобы ребенок не считал себя больным, слабым или хуже остальных детей в коллективе.
Медикаментозное лечение показано при наличии симптомов дисфункции сердечно-сосудистой системы, врожденных нарушениях развития соединительной ткани, наличии открытого овального окна. Оно включает:
- Применение препаратов магния;
- Назначение средств, улучшающих трофику сердечной мышцы (при нарушении реполяризации в миокарде);
- Антибиотикотерапию при частых воспалительных процессах;
- Антиаритмическое лечение при аритмиях.
Магний — важный компонент соединительной ткани, необходимый для образования коллагеновых волокон. Кроме того, он обладает антиаритмическим действием, способствует сохранению калия внутри кардиомиоцитов, поэтому препараты магния составляют основу патогенетического лечения при аневризме МПП и других малых аномалиях сердца.
Терапия препаратами магния состоит в назначении магнерота по 0,5 г три раза в день на протяжении одной недели, далее 5 недель по 250 мг препарата. Магне В6 назначается курсом на полтора-два месяца, дозировка рассчитывается исходя из массы тела ребенка. Помимо магния, показаны средства с калием — калия оротат в течение месяца. Курсы лечения микроэлементами повторяют несколько раз в год.
Для улучшения трофики миокарда, антиоксидантной защиты, мембраностабилизирующего эффекта применяются L-карнитин, коэнзим Q10 (кудесан), цито-мак. Курсы метаболической терапии могут занимать до 1-1,5 месяцев и повторяются 2-3 раза в год.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
Витаминотерапия проводится на протяжении полутора-двух месяцев повторяющимися курсами до трех раз в год. Целесообразно применение витаминов группы В, никотинамида, биотина.
При внутрисердечном тромбообразовании с риском эмболических осложнений назначаются антиагреганты и антикоагулянты. Крупные аневризмы у взрослых пациентов с риском тромбозов тоже могут требовать кроверазжижающей терапии.
Операция при аневризме МПП показана редко. Необходимость ее проведения может быть обусловлена наличием других пороков со стороны сердца и выходящих из него сосудистых магистралей, крупным дефектом межпредсердной перегородки, при котором нарушается внутрисердечная гемодинамика и происходит сброс крови слева направо, создающие предпосылки для сердечной недостаточности.
Обоснована операция при аневризме со сбросом крови и нарастанием необратимой гипертензии в легочной артерии. В таких случаях ушивают дефект или применяют пластику синтетическими «заплатами», препятствующими попаданию крови из левого предсердия в правое.
Специфических профилактических мер для предупреждения аневризмы не существует, а при ее наличии важно соблюдать щадящий режим, избегать физического и эмоционального перенапряжения. Раз в год детей с диагностированной аневризмой положено показывать кардиологу для оценки общего состояния ребенка и изменений перегородки между предсердиями. В абсолютном большинстве случаев аномалия протекает с хорошим прогнозом, никак не сказывается на развитии ребенка и не влияет на общую продолжительность жизни и ее качество.
Каким должно быть артериальное давление у детей разного возраста
- Артериальное давление – общее понятие
- Способы контроля давления
- Как правильно измерять АД у детей
- Норма АД у ребенка и особенности его изменения
- Осложнения перепадов давления у детей
- Как нормализовать АД детям
Перепады артериального давления (АД) у взрослых никого не удивляют, подобные проблемы у детей волнуют всех. Тем более, что отклонения от нормы бывают не только у подростков, но и у грудничков. Молодой организм имеет эластичные стенки сосудов, потому и кровяное давление у младенцев ниже. У новорожденного систолическое давление – около 75 мм рт.ст. С ростом малыша оно постепенно увеличивается.
Возраст ребенка определяет степень эластичности сосудистой стенки, ширину просвета артерий и вен, общую площадь капиллярной сети, от которых зависит норма артериального давления у детей.
Медицинская практика отмечает существенный перепад АД у младенцев до года. Каждый месяц у малышей оно растет на 1 мм рт. ст.
С года до 6 лет, давление повышается мало. Где-то к пяти годам его показатели выравниваются для обоих полов, в дальнейшем у мальчиков наблюдают АД чуть выше, чем у девочек. С 6 лет и до подросткового возраста систолическое АД снова растет: у мальчиков – на 2 мм. рт. ст., у девочек – на 1 мм рт. ст. Если ребенок жалуется на слабость, повышенную утомляемость, не спешите давать ему таблетку от головной боли. Измерьте для начала давление.
Артериальное давление – общее понятие
Система кровотока в организме – это сердце и сосуды. Они заполнены кровью, обеспечивающей питательными веществами и кислородом органы и ткани. Главная роль в этой системе отведена сердцу – природному насосу, перекачивающему кровь. При сокращении оно выбрасывает кровь в артерии. Давление крови в них называют артериальным.
Под АД медики понимают силу, с которой кровь воздействует на сосуды. Чем больше их Ø, тем выше АД. Проталкивая порциями кровь в кровеносную систему, сердце и создает соответствующий напор. Нормальное давление важно для обменных процессов, так как с кровью транспортируются к органам все питательные вещества, выводятся шлаки, токсины.
Способы контроля давления
Используют прямой и непрямой способы контроля АД. Инвазивный способ, необходим при оперативном вмешательстве, когда в артерию вводится зонд и датчик. Неинвазивные способы – это компрессионные варианты:
- Пальпаторный – самый сложный метод, требующий определенных навыков. Прижимая пальцами артерию, важно поймать в области, которая находится ниже сдавливаемого участка, момент максимального и минимального пульса.
- Аускультативный метод хирурга Короткова – эталонный с 1905 года и по сегодняшний день прием. Он предусматривает применение тонометра, манометра и стетоскопа.
- Осциллометрический способ лежит в основе принципа работы большинства автоматических тонометров. Он дает возможность проверить АД на плече, колене, запястье.
- Допплерография определяет с помощью ультразвука лишь систолическое АД. Используют ее чаще для новорожденных и грудничков.
Современные тонометры позволяют измерять давление детям в домашних условиях без специальной медицинской подготовки. И все же элементарные правила измерения АД детям надо знать.
Как правильно измерять АД у детей
Лучше всего измерять ребенку АД утром. Важно, чтобы он был в спокойном состоянии, перед процедурой у него не должно быть никаких нагрузок. Измерять лучше спустя час после еды или прогулки, если малыш не замерз. Стоит перед процедурой сводить его и в туалет.
Если измерения проводят впервые, надо проверить две руки, чтобы впоследствии проводить измерения там, где результат был выше. Измерение АД у детей имеет свои особенности. Детям до 2-х лет обычно меряют давление в положении лежа. Малыш постарше может сидеть. Рука, приготовленная для измерений, не висит, а лежит на приставном столике параллельно туловищу ладошкой вверх. Ножки также должны быть на подставке, если стул не по росту. Обязательное условие – угол между плечом и кистью должен быть прямой (около 90º).
Особенности техники измерений подробно описаны в инструкции к тонометру и заключаются, в основном, в подборе точной манжетки. Если пользоваться манжетами для взрослых, результат будет неточный. Особенно это касается малышей раннего возраста. Правильные результаты можно получить лишь в том случае, если манжета соответствует ¾ расстояния от локтевого сгиба до подмышки. Одевают ее на предплечье и закрепляют при помощи липучек. Зазор должен быть таким, чтобы между манжетой и кожей проходил палец взрослого. После фиксации манжеты по всем правилам с помощью груши нагнетают воздух. Потом этот воздух спускают, нажимая на клапан.
Чтобы рассчитать норму систолического давления, надо удвоить возраст и к произведению добавить 80. Диастолическое АД должно быть от ½ до ⅔ от значения верхнего АД. Для точных расчетов можно использовать специальную формулу. К примеру, для пятилетнего малыша надо произвести такие расчеты: 5 * 2 + 80 = 90 мм рт. ст. норма нижнего давления определяется как половина или ⅔ от этого параметра – от 45 до 60 мм рт. ст. Нормальное для конкретного ребенка давление будет зависеть не только от возраста, но и от ряда других факторов:
- Комплекции;
- Активности обменных процессов;
- Настроения;
- Переедания;
- Усталости;
- Качества сна;
- Генетической предрасположенности;
- Неблагоприятной погоды.
Норма АД у ребенка и особенности его изменения
Значения артериального давления у детей – таблица по возрасту:
| Возраст | Артериальное давление, мм рт. ст | |||
| Систолическое | Диастолическое | |||
| минимум | максимум | минимум | максимум | |
| 0-2 недели | 60 | 96 | 40 | 50 |
| 2-4 недели | 80 | 112 | 40 | 74 |
| 2-12 месяцев | 90 | 112 | 50 | 74 |
| 2-3 года | 100 | 112 | 60 | 74 |
| 3-5 лет | 100 | 116 | 60 | 76 |
| 6-9 лет | 100 | 122 | 60 | 78 |
| 10-12 лет | 110 | 126 | 70 | 82 |
| 13-15 лет | 110 | 136 | 70 | 86 |
Таблица с нормой пульса у детей:
| Возраст ребенка | Среднее значение пульса, уд./мин. | Пределы нормы, уд./мин. |
| 0-1 мес. | 140 | 110-170 |
| 1-12 мес. | 130 | 102-162 |
| 1-2 года | 124 | 94-154 |
| 2-4 года | 115 | 90-140 |
| 4-6 лет | 106 | 86-126 |
| 6-8 лет | 98 | 78-118 |
| 8-10 лет | 88 | 68-108 |
| 10-12 лет | 80 | 60-100 |
| 12-15 лет | 75 | 55-95 |
Норма АД: грудничок до года
Эластичное сосудистое русло и густая сетка капилляров – главные предпосылки того, что у младенцев АД намного ниже, чем у их родителей. У новорожденного показатели давления – 60-96/40-50 мм рт. ст. С укреплением тонуса стенок растет и АД, к концу первого года оно колеблется в пределах от 80/40 до 112/74 мм рт. ст., с учетом веса малютки.
Если нет под рукой данных АД у детей (норма – в таблице), для ориентации можно пользоваться расчетами: 76 + 2 n, где n – возраст грудничка в месяцах. Для новорожденных ширина камеры детской манжетки – 3 см, для младенцев постарше – 5 см. Процедуру повторяют 3 раза, ориентируясь на минимальный результат. У младенцев проверяют только систолическое АД, определяя его пальпацией.
Норма АД: малыш 2-3 лет
После года рост АД замедляется. К 2-3 годам средние показатели верхнего давления находятся на уровне100-112 мм рт. ст., нижнего – 60-74 мм рт.ст. АД можно считать выше границ нормы, если тревожный результат сохраняется в течение 3-х недель. Формула для уточнения нормы: систолическое АД – (90 + 2n), диастолическое – (60 + n), где n – количество полных лет.
Норма АД: ребенок 3-5 лет
Изучая параметры таблицы, нетрудно заметить, что с 3-х до 5-ти лет динамика роста АД замедляется. Систолическое АД у таких детей – 100-116 мм рт. ст, диастолическое – 60-76 мм рт. ст. Надо учитывать, что данные тонометра на протяжении дня не совпадают: в светлое время суток они достигают максимума, к ночи падают и после полуночи, до 5 часов, они минимальны.
Норма АД: школьник 6-9 лет
Из табличных данных понятно, что минимальные показатели давления сохраняются на прежних позициях, немного увеличены только самые высокие параметры. Норма возраста – 100-122/60-78 мм рт. ст.
Начало школьной жизни характеризуется отклонениями, так как образ жизни ребенка меняется. После непривычных эмоциональных нагрузок, сокращения физической активности дети жалуются на усталость, головную боль, капризничают. Важно быть внимательным состоянию ребенка в этот период.
Норма АД: подросток 10-12 лет
Начальный период полового созревания характерен изменениями АД. В большей степени это относится к девочкам, опережающим сильный пол в темпах физического развития.
Несмотря на средние значения АД от 110/70 до 126/82 мм рт. ст., медики считают нормой верхний предел – 120 мм. рт. ст. Зависит этот показатель и от типа телосложения: высокие и худощавые астеники обычно имеют более низкое давление по сравнению с ровесниками атлетического типа.
Норма АД у юношей и девушек 12-15 лет
Переходный возраст преподносит подросткам и их родителям немало сюрпризов. Высокие нагрузки в школе, часы, проведенные за компьютером, стрессы, нестабильный гормональный фон могут провоцировать как гипертензию, так и гипотонию.
В норме давление у детей таблица демонстрирует ближе к взрослым значениям: 110-70/136-86 мм рт. ст., так как к 12 годам сосудистая система уже заканчивает свое формирование. При перепадах возможна тахикардия, обмороки, изменение частоты сердечных сокращений, головные боли и головокружения.
Консультация детского кардиолога Тодоровой О.В. из научного цента «Здоровье детей» по вопросу измерения давления у детей – на этом ролике https://www.youtube.com/watch?v=jWzaMjRakck.
Осложнения перепадов давления у детей
Есть у медиков понятие – органы-мишени. Так называют органы, которые страдают в первую очередь. Обычно возникают проблемы со стороны сердца (ишемическая болезнь, инфаркт миокарда), проблемы центральной нервной системы, мозга (инсульты), поражение органов зрения вплоть до слепоты, почечная недостаточность. Опасность заключается в том, что артериальная гипертензия у детей, как правило бессимптомна.
Ребенок, особенно маленький, на самочувствие не жалуется. Проявляются отдельные признаки, на которые родители обязательно должны обращать внимание. Многие из них сходны с предпосылками гипертонии у взрослых.
- Головная боль;
- Носовые кровотечения;
- Тошнота, рвота;
- Слабость, усталость;
- Неврологические проявления: судороги, парезы, параличи;
- Нарушения зрения;Р
- Изменение походки.
Если ребенок упал в обморок, надо обязательно показать его педиатру. Доктор направит вас к специалисту для дальнейшего обследования.
Артериальная гипертензия имеет наследственную компоненту: если в семье есть гипертоники, АД у ребенка надо периодически контролировать, так как 45-60% из них имеют отягощенную наследственность. Чтобы ребенок стал гипертоником, необходимо воздействие и модифицирующих факторов: стрессы, нездоровое питание, гиподинамия, спортивные перегрузки.
Если у родных встречается вариант гипотонии, то пониженное давление может быть для ребенка индивидуальным вариантом нормы. Пониженное давление может носить адаптивный характер, например, у спортсменов или тех, кто выезжает на высокогорье. Этот вариант скорее исключение, потому что симптомы низкого давления могут говорить и о пороках сердца, миокардитах, эндокринных расстройствах (проблемы щитовидной железы, недостаточность коры надпочечников связаны с низким давлением).
Как нормализовать АД детям
Повышенное АД отмечают у 13% детей. Это связано с неадекватной нагрузкой на сердечную мышцу, высоким тонусом артерий, спазмами сосудов. Различают первичную и вторичную гипертонию. Первая форма обусловлена изменениями гормонального фона, непосильными для детской психики стрессами, недосыпанием, перегрузками за компьютером или в спортивной секции, конфликтами с ровесниками. Кроме внешних причин, есть еще и скрытые факторы: сердечная и почечная недостаточность, проблемы с эндокринной системой.
Вторичную гипертонию провоцируют тяжелые заболевания почек, сердца, эндокринной и нервной системы, интоксикации, травмы головы. В контексте таких расстройств кроются грозные патологии: опухоль гипофиза, сужение почечной артерии, новообразования надпочечников, остеопороз, пороки сердца, энцефалит.
Гипотония у детей бывает физиологическая и патологическая. От низкого давления страдают 10% детей. Физиологические предпосылки могут быть наследственными (конституция тела, генетическая предрасположенность к гипотонии), так и внешними (избыток кислорода, неблагоприятные погодные условия, неадекватные физические нагрузки) причинами. Патологическую гипотензию провоцируют:
- Респираторные инфекции;
- Бронхиты, тонзиллиты с осложнениями;
- Стрессы и расстройства психики;
- Физические перегрузки или их полное отсутствие;
- Авитаминоз, анемия;
- Родовая травма, аллергии;
- Сахарный диабет;
- Проблемы щитовидной железы;
- Сердечная недостаточность.
Чтобы нормализовать АД детям при гипотонии, надо контролировать количество употребляемой жидкости, скорректировать норму соли, можно использовать чай, кофе, эхинацею, китайский лимонник, пантокрин, экстракт элеутерококка. Наладить режим отдыха и учебы.
Нормы АД у детей – понятие относительное. Если ребенок волнуется, тонометр может показывать завышенный результат. В таком случае надо измерить давление еще раз. Объективным будет результат 3-4 измерений с интервалом в 5 минут. Для здорового ребенка нет необходимости в частом измерении АД, но если малыш заболел, попал в больницу, давление надо контролировать обязательно, желательно завести специальный дневник.
Регулярные физические нагрузки улучшают кровоток и нормализуют давление. Придумайте с детьми веселую зарядку, проводите ее в игровой форме, и море положительных эмоций гарантировано.
Давление – важный параметр здоровья ребенка, но не самый главный. Так что относитесь к нему без звериной серьезности. АД – вещь вариабельная, способная колебаться в течение суток, в зависимости от настроения и физических нагрузок. Главное – чтобы ребенок был здоров и не давал повода для постоянного контроля АД.
Синусовая аритмия у детей и подростков: диагностика и лечение заболевания
Что это такое
По результатам электрокардиографии ставят нарушение синусового ритма – синусовую аритмию. Но сразу отметим, что чаще всего это состояние связано с бурным ростом и гормональными изменениями в организме и только изредка указывает на серьезные патологии сердца.
В любом случае, малыша должен осмотреть врач, который после проведения дополнительных исследований, определит причину заболевания и выберет подходящую тактику лечения.
Общее описание заболевания
Сердце представляет собой насос для перекачивания крови. Пульсация происходит за счет электрических импульсов, которые распространяются по мышечным волокнам, вызывая их сокращение. Осуществляется это автоматически. Если по каким-либо причинам импульс образуется с задержкой или опережением, в сердечном ритме происходит сбой.
По частоте сердцебиения аритмии бывают трех видов:
- С сохранением нормального количества ударов в минуту.
- С увеличение числа сокращений – тахиаритмия.
- Со снижением частоты сердцебиения – брадиаритмия.
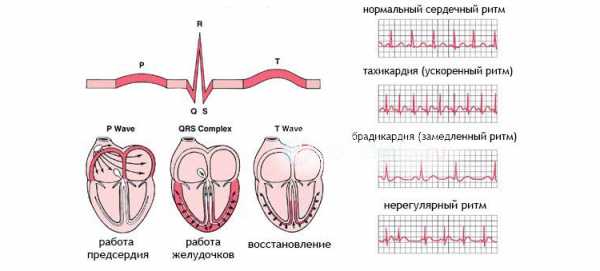
Синусовая аритмия возникает в результате изменения проводимости сердечных волокон, повышенной или сниженной возбудимости, сбоя автоматизма сердечных сокращений.
По происхождению заболевание может быть врожденным, приобретенным или наследственным.
Выделяют две степени тяжести:
- Умеренная синусовая аритмия у ребенка. Характерна для неопасных форм аритмии. Слабо выраженные симптомы или их отсутствие. Выявляется, как правило, случайно при проведении плановых ЭКГ.
- Выраженная синусовая аритмия у ребенка. Имеет явные симптомы. Сопровождает заболевания сердца и сосудов.
Распространенность
Нарушение сердечного ритма не является самостоятельным заболеванием, скорее проявлением или осложнением болезни или возникает как временное явление при возрастных перестройках организма.
Опасные и неопасные формы
В зависимости от причины различают сбой сердечного ритма дыхательного, функционального или органического типа.
Дыхательная
Дыхательная форма считается самой неопасной разновидностью заболевания. Выражается в усиленном сердцебиении на вдохе и сниженном при выдохе.
Частой причиной является незрелость нервной системы малыша. Нарушение сердечного ритма с возрастом проходит, но наблюдаться у врача нужно, чтобы не упустить возможных осложнений.
К патологическим причинам дыхательной синусовой аритмии можно отнести:
- повышение внутричерепного давления;
- поражение головного мозга невоспалительной природы у грудных детей, которое вызвано кислородным голоданием плода в период внутриутробного развития;
- незрелость детского организма в результате преждевременного рождения;
- нарушения обменных процессов в организме, рахит.
Функциональная
Функциональная форма встречается реже, чем дыхательная, но также редко бывает опасна. Причиной могут быть нарушения работы нервной, иммунной, эндокринной систем. Возникает как последствие перенесенной инфекционной или вирусной болезни или как проявление заболевания щитовидной железы.
Органическая
Органическая форма – наиболее опасная. Указывает на патологические сбои в системе проводящей импульс и другие нарушения в работе сердца.
Такой форме присущи ярко выраженные симптомы аритмии. Состояние требует немедленного обследования и длительного лечения.
Причины и факторы риска
Аритмию вызывают нарушения работы сердца:
- Сбои в работе системы, которая проводит импульсы. Нарушения могут касаться скорости образования и проведения импульса.
- Неправильное строение сердца. Если аномалии препятствуют нормальному сокращению сердечной мышцы.
- Нарушения вегетативной нервной системы.

Также сбой сердечного ритма может быть одним из проявлений заболевания:
- врожденный или приобретенный порок сердца;
- воспалительные заболевания сердца;
- сильная интоксикация организма (в том числе лекарственная);
- новообразования (доброкачественные или злокачественные опухоли);
- тяжелые случаи инфекционных или вирусных заболеваний;
- нервные перенапряжения и стрессы;
- сбои в период эмбрионального развития;
- наследственные заболевания;
- обезвоживание организма;
- чрезмерные физические нагрузки, особенно на фоне авитаминоза или общей ослабленности.
В детском и подростковом возрасте выделяют несколько периодов, когда опасность возникновения аритмии повышена из-за физиологических особенностей:
- Грудные дети от 4 до 8 месяцев;
- дети дошкольного возраста от 4 до 5 лет;
- младшие школьники от 6 до 8 лет;
- подростки от 12 лет.
В эти периоды лучше провести ЭКГ (электрокардиографию) и посетить кардиолога. О расшифровке ЭКГ у детей вы можете прочесть в отдельной статье.
Основная симптоматика
При нетяжелых случаях аритмии нет выраженных проявлений. Ситуация осложняется тем, что дети младшего возраста не могут сформулировать, что их беспокоит. Нарушение ритма выявляется врачом-кардиологом при осмотре или при проведении ЭКГ.
Симптомы, которые должны насторожить родителей:

- Повторяющиеся потери сознания.
- Плохой сон на протяжении длительного времени. Малыш часто просыпается с плачем.
- На фоне любой физической активности (ползание, ходьба, подъем и так далее) возникает отдышка.
- Ребенок часто плачет без явных причин.
- Усиленное потоотделение.
- Ухудшение аппетита или полный отказ от еды.
- Синюшность носогубного треугольника, ногтевых пластин, стоп на фоне общей бледности кожи.
- Нарушение поведения. Беспокойство или вялость.
Дети старшего возраста могут жаловаться на:
- ощущение слабости, вялости, упадка сил;
- дискомфорт в области сердца (перебои);
- ощущения сжатия в районе сердца, боль в груди;
- головокружения;
- учащенное сердцебиение;
- ухудшение состояния после физической активности.
Диагностические мероприятия
Самым первым методом диагностики сердечных нарушения является электрокардиография.
Для получения достоверных результатов ЭКГ важно правильно провести процедуру. Если маленькому пациенту неудобно, страшно или он побегал перед исследованием, то кардиограмма покажет нарушение сердечного ритма. Но в таком случае аритмия вызвана естественными сбоями в дыхании на нервной почве.
Кроме того, применяются дополнительные методы исследования:
- Эхокардиограмма. Исследование проводят при помощи ультразвука.
- Суточное холтеровское мониторирование ЭКГ. Длительная непрерывная запись кардиограммы на протяжении суток или большего периода времени.
- Стресс-тест. Запись ЭКГ на фоне нагрузок.
- Ортостатическая проба. Определение некоторых показателей (давление, частота пульса и другие) при переходе из лежачего положения в стоячее и наоборот.
- Электрофизиологическое исследование. Метод, при котором отделы сердца стимулируются и регистрируются результаты. При этом электроды вводятся непосредственно в сердце.
- Анализы. Проводится общий анализ крови у детей и исследуются гормональные показатели.
Чаще всего проводят ЭКГ с разными вариантами нагрузок. Пример, как выглядит синусовая аритмия на ЭКГ у ребенка:
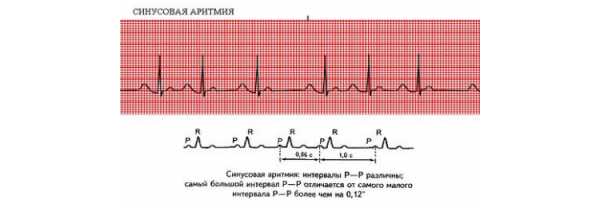
Кроме основной применяют дифференциальную диагностику. Это метод исследования, при котором исключаются заболевания, которые не подходят по каким-то параметрам, пока не выявится единственно верный диагноз.
Существуют компьютерные программы, которые по ряду данных могут составить список возможных заболеваний пациента. А врач уже определяется с диагнозом.
Тактика терапии
Если по результатам кардиограммы выявлено нарушение, нужно посетить кардиолога. Будут назначены дополнительные обследования, которые помогут выяснить причину, форму и степень тяжести патологии. Только после этого назначается лечение.

Аритмии дыхательного типа в большинстве случаев в лечении не нуждаются – проходят самостоятельно. Но требуют врачебного контроля.
Функциональные нарушения сердечного ритма проходят после устранения причины заболевания.
Органическая аритмия нуждается в длительном комплексном лечении, так как вызывается сердечной патологией. Лечебная тактика подбирается индивидуально.
Лечение любого вида аритмии включает организацию правильного режима дня, здоровое разнообразное питание (преимущественно растительная и молочная пища), щадящий режим, массажи (особенно массаж шеи).
Интенсивность допустимых физических нагрузок определяется в каждом случае индивидуально. Обычно полезно заниматься плаванием, гимнастикой, совершать пешие прогулки. Детям с аритмией нельзя нервничать и переутомляться.
Общая схема лечения:
- В основе терапии – противоаритмические препараты, которые нормализуют сердечный ритм и снимают неприятные симптомы. Например, Аймалин, Анаприлин, Верапамил и другие.
- Обезболивающие препараты.
- Успокоительные средства.
- Комплексы витаминов и минералов.
В тяжелых случаях ребенок должен находиться под контролем медиков. Возможно потребуется хирургическая операция по установке кардиостимулятора.
Прогноз и возможные осложнения
В большинстве случаев аритмия проходит самостоятельно, в дальнейшем не возникает последствий. В тяжелых случаях может развиться сердечная недостаточность. Ребенку присваивается инвалидность.
Самыми страшными осложнениями являются асистолия (прекращение сокращений сердца) и фибрилляция (состояние при котором разные части сердечных волокон сокращаются по-разному – трепетание). В результате наступает летальный исход.
Узнайте больше о нарушениях ритма сердца у детей, а также о синдроме, симптомом которого это может быть, из видео:
Профилактика
Лучшей профилактической мерой является здоровый образ жизни. У малыша должен быть режим дня, достаточное количество сна, полноценное сбалансированное питание, отсутствие стрессовых ситуаций и чрезмерных нагрузок.
Не нужно пропускать плановые осмотры у врачей. При малейших подозрениях – обратиться к кардиологу. Если есть заболевания, которые могут вызвать аритмию, или наследственная предрасположенность – контролировать состояние, наблюдаться у врача.
Чтобы исключить сердечные патологии или серьезные заболевания, симптомом которых может быть аритмия. Тактика лечения и прогноз зависят от вида нарушения сердечного ритма и от причин, вызывавших сбой.
МСКТ сердца – быстрый, точный и комфортный метод диагностики
Коронарные артерии в организме человека выполняют особую функцию – доставляют к сердечной мышце наполненную кислородом кровь, тем самым питая миокард. Наличие патологий, неправильного строения и работу сердца исследуют при помощи мультиспиральной компьютерной томографии. МСКТ сердца является новейшим методом в медицинской диагностике.
Метод исследования сердца
МСКТ сердца помогает увидеть расположение сосудов в трехмерном изображении
МСКТ – мультиспиральная компьютерная томография сердца. Сканирование сердечной мышцы рентгеновским излучением. С помощью чувствительных детекторов сквозь сердце проходит пучок излучений, который сканирует орган.
Процедура помогает увидеть сердце в трехмерном изображении и выявить патологии и поражения сердечных клапанов, миокарда, перикарда.
Диагностика сопровождается небольшим лучевым влиянием на организм, верно и точно определяет заболевания, выводит изображения необходимых участков и срезов на монитор.
В отличие от этого метода, прочие кардиодиагностические исследования не показывают все участки поражения артерий. Поэтому для диагностики заболеваний структур сердца и коронарных артерий используют МСКТ.
Показания к проведению
Различные патологии клапанов сердца являются показанием к проведению МСКТ
Врачи определили несколько областей применения метода, где он показывает наиболее точные результаты обследования. МСКТ назначают при:
- патологии сердечных клапанов
- сердечном кальцинозе
- атеросклерозе
- нехватке фактов после эхокардиографии, других исследований
- подозрении на новообразования
- проверке работы шунта
- появлении тромбов
- определении заболеваний, сопутствующих сердечным
- обнаружении порока сердца
- сильной боли в груди, связанной с ИБС
- аномальном состоянии артерий
Возможности метода помогают выявить сложные, редкие пороки вен, артерий, бронхов.
Противопоказания
При беременности проводить МСКТ запрещено
Важно учитывать, что есть ряд противопоказаний нового метода. Это:
- высокий уровень креатинина
- нарушение сердцебиения, больше 100 сокращений в минуту
- сбои в работе щитовидной железы
- астма, одышка
- психические расстройства
- беременность
- общее тяжелое состояние пациента
- избыточный вес, более 170 килограмм
- заболевание почек
МСКТ проводят после тщательного выявления противопоказаний для больного. Это необходимое условие безопасности и точности результатов процедуры.
Мультиспиральная компьютерная кардиография легко переносится больными. Для проведения процедуры требуется минимум подготовки:
- Перед исследованием нельзя есть. После приема пищи должно пройти три – пять часов.
- В день процедуры запрещено пить лекарства, учащающие сердцебиение. Это кофеин, теофиллин, атропин, цитрамон.
- Во время кардиографии нужная частота сокращений сердца должна быть меньше 65 ударов в минуту. Если сердце бьется чаще, больному вводят препарат, уменьшающий частоту сокращений.
- Советуют не волноваться людям, имеющим аллергию на йод и нуждающимся в МСКТ. Их подготавливают, прокалывают антигистаминные лекарства.
Процедура практически не имеет побочных эффектов и помогает быстро оценить состояние сердца и артерий.
Проведение процедуры
При МСКТ проводят катетеризацию для вода в организм контрастирующего вещества
Перед началом процедуры больной переодевается в стерильную больничную пижаму. Снимает предметы из металла: очки, украшения, часы, протезы. Они могут помешать, исказить показания исследования.
Читайте также: Тредмил-тест в кардиологии - что это такое?
Пациента укладывают на стол, на спину с поднятыми руками. Вводят в вену небольшой катетер, подающий контрастирующую жидкость.
К катетеру присоединяется трубочка от томографа. Она дозирует содержащее йод вещество. Процедуру сканирования начинают на вдохе, после непродолжительной задержки дыхания.
Для получения более четких изображений двигаться во время диагностики нельзя! Детям и тревожным больным дают успокаивающие препараты.
Во время диагностики, из-за поступления в вену контраста, больные чувствуют привкус металла во рту, ощущают сильный жар во всем теле. Но так как кардиография длится 10 – 15 минут, эти побочные эффекты не причиняют неудобств.
После завершения сканирования результат обрабатывают на компьютере, и появляется трехмерная картинка исследуемой области. Затем больной получает все анализы в распечатанном виде. Каждый снимок снабжен расшифровкой врача лучевой диагностики. С результатами пациент идет к кардиологу для назначения лечения.
Результат исследования
Результат МСКТ выглядит как трехмерная модель сердца и его сосудов
Томография выявляет патологию самых мизерных размеров. Для постановки верного диагноза важно грамотно расшифровать снимки. Это зависит от практики и опыта врача.
Результат исследования определяют не количеством снимков. Важно не только найти патологию и определить ее точное расположение. Необходимо правильно «прочитать» МСКТ и описать очаги заболевания.
Современные аппараты для коронарографии создают трехмерную модель сердца и его сосудов. Это дает возможность увидеть самые мелкие коронарные артерии.
Читайте также: Что это такое велоэргометрия и о чем она может рассказать?
Исследования помогают обнаружить:
- тромб
- спазм
- атеросклероз
- эмболию легких
- инфаркт миокарда
- стенокардию
- ишемию миокарда
- гипертрофию сердца
- патологию клапанов
- склероз миокарда
- аортальную диссекцию
- коронарный синдром
Использование контраста
МСКТ сердца делают с использованием контрастирующей жидкости. Она помогает точно увидеть обследуемую область.
Контраст позволяет четче рассмотреть очертания и форму сердца, выявить опухоли. Это удается благодаря возможности лучей более точно отражать от бариевой или йодсодержащей среды, чем и является контрастная жидкость.
Метод внутривенного контраста дает возможность увидеть характер патологии органов. Это актуально при обнаружении опухоли. Кроме того, контрастирование выявляет изменения и патологии, которые не удается обнаружить при процедуре МСКТ без контраста.
В крупных, оснащенных медицинских центрах процедура выполняется болюсным способом: введение контраста полностью автоматизировано, жидкость поступает посредством специального прибора.
Во время процедуры рядом с больным всегда находится врач – анестезиолог.
Преимущества метода
Метод МСКТ позволяет определить местонахождение холестериновых бляшек в сосудах сердца
МСКТ сочетает два вида диагностики: УЗИ, МРТ. При этом практически не имеет недостатков. Помогает врачу — кардиологу понять состояние сердца и кровеносного русла.
Процедура МСКТ безопаснее и точнее компьютерной томографии сердца. Ее преимущества:
- Быстрое исследование, что удобно при большом количестве больных. Кроме этого, процедуру выполняют амбулаторно, не помещая человека в стационар.
- Невысокое ионизирующее излучение – до 65%.
- Изображение артерий на 3D картинке, помогающее увидеть и понять отклонения.
- Верная оценка состояния сосудов, сердца, перикарда. Выявление патологии клапанов, месторасположения холестериновых и фиброзных бляшек.
- Возможность увидеть расположение шунтов после операции.
- Эффективность метода при лечении больных 50 – 60 лет с ишемической болезнью сердца.
- Применение МСКТ для пациентов с сердечными болями неизвестного характера.
В результате медицинской статистики установлено преимущество МСКТ сердца перед коронарной томографией. Кардиологи подтверждают, что новый метод дает почти 100% правдивую информацию.
Потенциальные риски
МСКТ считают безопасным исследованием, при котором происходит небольшое излучение. Но, как и при любой томографии, имеются некоторые риски:
- Частое использование этой диагностики вызывает появление злокачественных опухолей.
- Женщинам желательно сказать врачу о беременности или ее возможности. Беременным запрещено проходить диагностику. Рекомендуют сделать томографию без использования облучения.
- Случается, что при вводе контраста у пациента возникает аллергия на йод. Важно выявить склонность к аллергической реакции до проведения МСКТ, сделать пробу на используемый препарат.
Альтернативы
МРТ является одним из альтернатив МСКТ
МСКТ сосудов и сердца имеют недостатки:
- катетеризация процесса
- желательная госпитализация пациента
- ощущения дискомфорта
- возможность осложнений
- высокая цена исследования
Врачи предлагают, как альтернативу, следующие процедуры:
- Магнитно — резонансная томография. Проводится быстро, безболезненно, комфортно. Не представляет для пациента опасности, точно показывает артерии при применении контраста.
- ЭКГ – диагностическое исследование на электрокардиографе. Показывает регулярность и частоту сокращений сердца. Недостатки: невозможность увидеть порок сердца, новообразования, измерить давление крови.
- Сцинтиграфия сердца — рассматривают кровоток к сердцу во время нагрузки и в состоянии покоя. Это помогает оценить кровообращение в сердечной мышце. Сцинтиграфию миокарда считают щадящим и безопасным методом диагностики без применения катетера.
- УЗИ – недостаток заключается в невозможности рассмотреть длину сосудов сердца, медикам видно лишь начало сосудов. Поэтому точным диагностическим методом УЗИ назвать нельзя.
- Спиральная КТ – ангиография: метод, дающий полную информацию о сосудах сердца. Сканирует артерии, сердце, аорту, периферические сосуды.
Кардиолог учитывает индивидуальные анализы и определяет подходящий метод диагностики. Самым информативным и полным считают МСКТ и МРТ.
Смотрите видео про МСКТ:
Применение мультиспирального компьютерного томографа помогает оценить коронарные артерии больного, увидеть патологию грудной аорты и легких. Это дает возможность выявить болезнь в ранней стадии и назначить правильное лечение.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
Мультиспиральная компьютерная томография в диагностике врожденных пороков сердца у детей первых лет жизни
Комплексные проблемы сердечно-сосудистых заболеваний. 2013. № 4
УДК: 616-007-053.1
МУЛЬТИСПИРАЛЬНАЯ КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ В ДИАГНОСТИКЕ ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА У ДЕТЕЙ ПЕРВЫХ ЛЕТ ЖИЗНИ
А. Н. КОКОВ, С. Е. СЕМЕНОВ, В. Л. МАСЕНКО, А. А. ХРОМОВ, Ю. М. ПОРТНОВ Федеральное государственное бюджетное учреждение «Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний» Сибирского отделения Российской академии наук, Кемерово, Россия
Цель. Анализ собственного опыта использования мультиспиральной компьютерной томографии (МСКТ) в диагностике врожденных пороков сердца (ВПС) у детей первых лет жизни, определение эффективности данной методики.
Материалы и методы. Проанализированы данные МСКТ пациентов с ВПС (п = 156, средний возраст 3,5 (2; 9,7) мес). Обследование проводили на 64-срезовом компьютерном томографе с болюсным введением рентгеноконтрастного препарата.
Результаты. Отмечена высокая диагностическая информативность МСКТ в отношении морфометрии коарктации аорты, открытого артериального протока до и после оперативного вмешательства. Определены возможности метода в отношении больных с тетрадой Фалло и аномальным дренажем легочных вен. С использованием МСКТ у 55 больных с ВПС выявлены также патологические изменения со стороны бронхолегочной системы.
Заключение. Использование МСКТ в диагностике ВПС у детей первых лет жизни позволяет получить точные морфометрические данные, касающиеся ВПС, оценить сопутствующую некардиальную патологию, определить дальнейшую тактику лечения, провести планирование оперативной коррекции порока и оценить результаты хирургического вмешательства.
Ключевые слова: врожденные пороки сердца, мультиспиральная компьютерная томография.
MULTYSLICE COMPUTED TOMOGRAPHY IN THE DIAGNOSIS OF CONGENITAL HEART DISEASE IN CHILDREN EARLY YEARS
A. N. KOKOV, S. E. SEMENOV, V. L. MASENKO, A. A. KHROMOV, YU. M. PORTNOV Federal State Budgetary Institution Research Institute for Complex Issues of Cardiovascular Diseases under the Siberian Branch of the Russian Academy of Medical Sciences, Kemerovo, Russia
Purpose. Analysis of the own experience with multislice computed tomography (MSCT) in the diagnosis of congenital heart disease (CHD) in children in the first years of life and determine the effectiveness of this technique.
Materials and methods. We analyzed MSCT data of patients with CHD (n = 156, mean age 3,5 (2; 9,7 mo), which was conducted on a 64-slice CT scanner with a bolus of X-ray contrast.
Results. We found excellent information content of MSCT in morphometry of coarctation of the aorta, ductus arteriosus in patients before and after surgical intervention. Possibilities of the method have been presented for patients with tetralogy of Fallot and anomalous pulmonary venous drainage. Pathological changes in the bronchopulmonary system were revealed in 55 patients with CHD by MSCT.
Conclusion. The use of MSCT in the diagnosis of CHD in children during the first years of life to get accurate morphometric data of the anatomy of CHD and assessment of concomitant noncardial pathology for determining treatment strategy, planning, operational correction and control of the results of surgery.
Keywords', congenital heart disease, multislice computed tomography.
Введение
Врожденные пороки сердца (ВПС) представляют собой серьезную медицинскую и социальную проблему для всех стран мира [6]. Высокие затраты на лечение, уход и реабилитацию детей с данной патологией обусловливают приоритетные задачи здравоохранения по разработке и совершенствованию методов диагностики. На протяжении последних десятилетий диагностика врожденных пороков развития сердечно-сосудистой системы претерпела значительные изменения, обуслов-
ленные развитием матерально-технической базы, совершенствованием техники хирургической коррекции и развитием реанимационной перинатальной поддержки. Совершенствование ультразвуковой диагностики дало возможность определять нарушения формирования сердца и магистральных сосудов уже на этапе внутриутробного развития. Если еще недавно для прижизненной визуализации анатомии пороков в арсенале лучевых диагностов, помимо ультразвуковых методов, имелось лишь инвазивное зондирование камер сердца, то в настоящее время активно использу-
ются контрастные и бесконтрастные методики магнитно-резонансной (МРТ) и мультиспираль-ной компьютерной томографии (МСКТ).
МРТ при отсутствии лучевой и контрастной нагрузки уступает МСКТ в пространственном и временном разрешении [8]. Чувствительность МРТ к двигательным артефактам и необходимость длительного пребывания пациента в поле сканера для получения диагностических данных ограничивает использование этого метода для визуализации и диагностики анатомии врожденного порока, состояния органов грудной клетки у детей первых лет жизни, в том числе новорожденных. Необходимость ранней диагностики требует проведения МСКТ у больных этой категории как можно раньше, в том числе на первом месяце жизни [5, 6]. Использование МСКТ в определении тактики и стратегии коррекции врожденных пороков сердца в ФГБУ «НИИ КПССЗ» СО РАМН получило начало в 2009 г.
Нами проведен анализ результатов обследования пациентов с данной патологией с целью обобщения опыта использования МСКТ в диагностике ВПС у детей первых лет жизни, определения эффективности данной методики.
Материалы и методы
В течение 2009-2012 гг. на базе кабинета рентгеновской компьютерной томографии ФГБУ «НИИ КПССЗ» СО РАМН обследованы 156 пациентов в возрасте от 6 часов до 3 лет (средний возраст 3,5 (2; 9,7) мес). Исследование проводилось на фоне анестезиологического пособия. В 8 случаях иммобилизацию пациентов выполняли путем тугого пеленания. Сканирование выполняли на мультиспиральных компьютерных томографах Somatom Sensation 64 (Siemens, ФРГ) и LightSpeed 64 (GE, США) по протоколу с синхронизацией по сигналу ЭКГ Использовали толщину реконструируемых срезов 0,6 и 1,5 мм. Внутривенное болюсное введение неионного изоосмолярного контрастного препарата (йодиксанол, концентрация йода 320 мл/мг) в объеме 1,5-2 мл/кг осуществляли с помощью автоматического двухколбового шприца-инжектора. Скорость введения рентгеноконтрастного препарата варьировалась в пределах 0,5-1,0 мл/с. Суммарная эффективная доза облучения при проведении МСКТ колебалась от 3,3 до 4,8 мЗв. Полученные изображения в дальнейшем подвергались постпроцессорной обработке на мультимодальных рабочих станциях Advanced Workstation и Leonardo с построением трехмерных и четырехмерных реконструкций, использованием методов проекции максимальной интенсивно-
сти (англ. maximum intensity projection, сокращенно MIP) и мультипланарной реконструкции (англ. multiplanar reconstruction, сокращенно MPR). Все данные сопоставляли с данными эхокардиогра-фии и интраоперационными данными.
Для количественных признаков результаты представлены в виде медианы (Me) с межквар-тильным интервалом (25 %; 75 % процентили). Расчет эффективности метода производили с использованием критериев, предложенных научной группой ВОЗ для визуализирующих методов диагностики (Женева, 1992): чувствительности, специфичности, диагностической точности. Под чувствительностью понимали способность методики выявлять больных из числа лиц, к которым она применялась; под специфичностью - способность методики выявлять пациентов, не имеющих патологии, среди тех, к кому эта методика применялась; под диагностической точностью - соотношение числа правильных заключений (положительных и отрицательных) к общему числу окончательных диагнозов.
Результаты и обсуждение
В основе детальной оценки анатомии и мор-фометрии врожденного порока сердца лежит изучение тонких поперечных срезов зоны интереса. Последовательный анализ изображений позволяет понять пространственное расположение основных структур, их взаимосвязь и отношение к органам средостения, бронхолегочной системе. Особенностями визуализации структур сердца у детей в раннем возрасте на МСКТ является наличие артефактов дыхания, которых невозможно избежать, так как ребенок не выполняет команды по задержке дыхания во время сканирования. Кроме того, высокая частота сердечных сокращений - 120-140 ударов в минуту и изменение самой структуры сердечного цикла в сторону укорочения диастолы приводит к диссинхронии сканирования с ЭКГ и появлению так называемых степ-артефактов, «рвущих» изображение в аксиальной плоскости. Имеющиеся данные литературы указывают на возможность использования бета-адре-ноблокаторов (пропранолол) у детей младшего возраста для урежения ритма, чтобы достичь качественного изображения [3]. Мы не использовали такой подход из-за риска дестабилизации состояния пациентов. С целью получения наиболее приемлемых изображений при постпроцессорной обработке мы выполняли реконструкции в различные фазы сердечного цикла. Таким образом, оценка структур на интересуемом уровне у одного пациента может осуществляться по данным серии
изображений, полученных на протяжении сердечного цикла с шагом в 10 % от интервала Я-Я. При последующей мультипланарной реконструкции, которая обязательно входит в протокол изучения массива данных, мы получали фактически четырехмерное изображение. Наиболее информативно использование данного этапа в оценке анатомии клапанного аппарата и состояния сократительной функции миокарда.
В определении анатомических особенностей структур сердца и магистральных сосудов нами традиционно используется сегментный подход с последовательной оценкой предсердного, желудочкового сегментов, предсердно-желудочкового сообщения, желудочково-артериального сообщения и состояния аорты, легочной артерии и их клапанов [11]. Дополнительному изучению подвергаются анатомия венозных структур, наличие коллатерального кровообращения.
Структура врожденных пороков сердца, диагностированных в кабинете МСКТ, отличается от данных статистики ВПС на территории Кемеровской области [2]. Это обусловлено дифференциальным подходом к выбору данного метода обследования в случаях неудовлетворительных или неполных данных эхокардиографии, а также при определении тактики хирургической коррекции (табл. 1).
Таблица 1
Структура
диагностированных в рожденных пороков по данным МСКТ (2009-2012 гг.)
Показатель п % Возраст, мес
Коарктация аорты 58 37,2 7,1 (1,5; 13)
Тетрада Фалло 33 21,2 3 (1; 5,5)
Аномальный дренаж легочных вен 19 12,2 19 (8; 29)
Транспозиция магистральных сосудов 14 8,9 4,5 (1,75; 5,75)
Стеноз легочной артерии 10 6,4 3,25 (1; 4)
ДМПП (без прочих ВПС) 7 4,5 5 (3; 9)
Двойное отхождение магистральных сосудов 5 3,2 2(1; 5)
дмжп (без прочих ВПС) 4 2,6 4(1; 7,25)
Атрезия трикуспидально-го клапана 3 1,9 2 (2; 5)
Атриовентрикулярная коммуникация 3 1,9 1,2 (0,85; 1,6)
Всего 156 100 3,5 (2; 9,7)
Именно в связи с предоперационным планированием, выбором метода хирургической коррекции
наибольшее количество диагностических процедур выполнено у больных с коарктацией аорты. Исходные изображения в аксиальной плоскости не позволяют достоверно оценить эту патологию. Поэтому основной анализ данных должен осуществляться на основании кососагиттальных плоскостных МІР реформаций, построенных вдоль осей восходящего и нисходящего отделов грудной аорты, и трехмерных реконструкций (рис. 1).
Рис. 1. Коарктация аорты.
Данные МСКТ с внутривенным болюсным контрастированием у ребенка 1,5 мес.: а - М1Рреконструкция по продольной оси аорты;
б - трехмерная УК I реконструкция.
Белой стрелкой отмечена коарктация, дуга аорты гипоплазирована, визуализирован открытый артериальный проток (тонкая стрелка)
Мы проводили морфометрию аорты, коаркта-ции, расстояния ее до ветвей дуги, определяли пространственное положение всех отделов восходящей аорты относительно других сосудистых структур, трахеи, пищевода. В 56 случаях (97 %) было отмечено сужение просвета аорты в области перешейка по предуктальному типу, дистально от устья левой подключичной артерии на 1,2 (5; 1,75) мм, на протяжении 0,75 (0,3; 1,1) мм. Полный перерыв аорты с развитием коллатерального кровотока через спинальные и костальные ветви отмечали у двух пациентов (3 %). Также при полном перерыве аорты визуализировался открытый артериальный проток. У остальных пациентов с коарктацией аорты открытый артериальный проток присутствовал в 73 % случаев. Диаметр его варьировался от 1 до 8,5 мм. Коарктация аорты зачастую сопровождалась гипоплазией дуги (22 больных, 37,9 %) в виде тубулярного уменьшения ее диаметра более чем на 5 % относительно восходящего отдела. Ассоциация коарктации с дефектом межжелудочковой перегородки (ДМЖП) в 27,6 % (16 пациентов) и формированием двухстворчатого аортального клапана в 15,5 % (9 пациентов) может свидетельствовать в пользу теории о влиянии вну-трисердечных дефектов на снижение артериального кровотока в левых отделах и, как следствие, развитие гипоплазии и коарктации аорты [1]. Дистальный кровоток аорты в большинстве случаев не имел каких-либо особенностей, за исключением 4 больных, у которых отмечали протяженное сужение просвета брюшной аорты до 3 мм. В последующем у этих детей после хирургической коррекции коарктации произошло наполнение дистального русла и нормализация морфометрических параметров аорты. Оценка коллатерального кровообращения при коарктации не вызывала затруднений в случае визуализации расширенных (более 1 мм) костальных артерий, ход которых четко прослеживался до перетоков в систему брахиоцефальных артерий. Но в большинстве случаев (67,2 %) нам не удалось однозначно проследить систему коллатералей из-за субмиллиметрового калибра артерий. В 11 случаях МСКТ была проведена в сроки 8-15 месяцев после хирургической коррекции с целью определения состояния анастомоза аорты, для исключения рекоарктации, визуализации Боталлова протока. Было отмечено полное восстановление проходимости аорты, четко визуалированы анастомозы. Коллатеральное кровообращение в постоперационном периоде значимо редуцировалось. С учетом изменения пространственной анатомии области перешейка и дуги в постоперационном периоде заслуживает
внимания состояние трахеи, легочных артерий, вен (рис. 2). Данные МСКТ сравнивали с интра-операционными данными, в результате чего отметили полное соответствие морфометрических показателей аорты (чувствительность - 100 %, специфичность - 100 %, диагностическая точность - 100 %). В отношении визуализации коллатеральных сосудов и открытого артериального протока данные несколько разошлись. Функционирующий Боталлов проток не удалось убедительно визуализировать в 3 случаях из-за артефактов (чувствительность - 92 %). Но при этом не было отмечено ни одного ложноположительного результата. Таким образом, специфичность МСКТ в определении открытого артериального протока составила 100 %. Чувствительность и специфичность метода в отношении коллатералей составила 86 и 90 % соответственно, что вполне соответствует данным литературы [7, 10].
Рис. 2. Экстравазальная компрессия единственной левой легочной вены нисходящей аортой.
Данные МСКТ с внутривенным болюсным контрастированием у ребенка 9 мес. в послеоперационном периоде через 6 мес после пластики дуги аорты, аксиальный срез
Исследование пациентов с тетрадой Фалло (ТФ) составило пятую часть объема МСКТ, выполненного у больных с ВПС. Как и в случае остальных врожденных пороков, у детей с ТФ можно выделить две цели направления на МСКТ: первичную предоперационную диагностику и пост-операционный контроль. Оба диагностических алгоритма при этом имеют свои особенности. Из-за того что выраженные формы ТФ сопровождаются ранней манифестацией клиники, возраст детей, проходивших МСКТ при подготовке к операции, варьировался от недели до 4 месяцев, в среднем 1,5 (0,5; 2,5) месяца. Основной диагностической задачей в такой ситуации является определение степени стеноза легочной артерии, степени декстрапозиции аорты, наличия больших
аорто-легочных коллатералей, пространственной анатомии структур сердца и магистральных артерий. В 80 % случаев выявленной декстрапо-зиции аорты отмечали симметричное расположение фиброзного кольца аортального клапана над межжелудочковой перегородкой. Смещение аорты в сторону левого или правого желудочка более 50 % было выявлено в равном количестве случаев. Более вариабельно у больных с ТФ представляется анатомия выводного пути правого желудочка. Атрезия клапана легочного ствола была выявлена у 3 пациентов, что было подтверждено данными селективной ангиографии и интраопера-ционно. Эффективно подтвердить подклапанный стеноз, обусловленный гипертрофией правого желудочка, с помощью МСКТ не удалось. Стеноз на уровне клапана в большинстве случаев удалось визуализировать (чувствительность - 83 %), но определить степень стеноза по данным МСКТ было сложно (специфичность - 65 %). Причинами неудач явились наложение артефактов высокой ЧСС и резкая динамическая подвижность структур малого размера (фиброзное кольцо, створки клапана). Чтобы получить представление об изменениях надклапанных отделов легочного ствола и легочных артерий, зачастую достаточно изучения аксиальных изображений (рис. За). Однако мы всегда использовали кососагиттальные М1Р реконструкции вдоль продольной оси легочного ствола для детальной оценки просвета. Из-за расположения этих сосудистых образований крани-
ально относительно активно движущихся структур сердца наложение на них артефактов высокой ЧСС практически отсутствует. Это позволило с высокой диагностической точностью определить состояние проходимости легочного ствола и легочных артерий (чувствительность - 98 %, специфичность - 96 %). Стенотические изменения легочных артерий зачастую сопровождаются формированием патологической коллатеральной сети, так называемых больших аорто-легочных коллатеральных артерий (БАЛК), посредством которых осуществляется дополнительный приток крови к легким (рис. 36). Выявление БАЛК, определение точной локализации устья и дальнейшего хода артерии имеет значение для планирования операции и формирования гемодинамики малого круга в постоперационном периоде [10]. Учитывая конечную разрешающую способность метода МСКТ, имеет значение диаметр БАЛК. По нашим данным, достоверное определение аорто-легочных коллатералей возможно при диаметре более
1,3 мм (табл. 2).
Таблица 2
Диагностика больших аорто-легочных коллатералей по данным МСКТ
Диаметр БАЛК (мм) Чувствительность, % Специфичность, % Точность, %
Более 1,3 100 100 100
1,0-1,3 93 88 91
Менее 1,0 75 93 81
Рис. 3. Стеноз правой легочной артерии, БАЛК. Данные МСКТ с внутривенным болюсным контрастированием у ребенка 5 мес.: а - М1Р реконструкция в аксиальной проекции; б - трехмерная УКГ реконструкция. Большой стрелкой отмечен стеноз правой легочной артерии, визуализируется расширение легочного ствола и левой легочной артерии. Имеется выраженный коллатеральный кровоток от аорты к ветвям правой легочной артерии (маленькие стрелки)
Рис. 4. Тотальный аномальный дренаж легочных вен, супракардиальная форма.
Данные МСКТ с внутривенным болюсным контрастированием у ребенка 6 мес.: а - МІР реконструкция во фронтальной проекции; б - трехмерная УКТ реконструкция (вид сзади)
В послеоперационном периоде МСКТ проводилась через 12 (9; 16) месяцев. Дополнительно к стандартному объему исследования у таких пациентов выполняли оценку пластики легочного клапана, легочного ствола. При закрытии дефекта межжелудочковой перегородки определяли наличие перетока между желудочками в раннюю фазу прохождения болюса контраста. У 5 больных визуализирован подключично-легочной анастомоз, который был наложен на первом этапе хирургического лечения; проходимость шунта во всех случаях не была нарушена.
Одним из отличий МСКТ от селективной ангиографии является возможность одномоментного получения данных как об артериальном, так и венозном русле. Определение нарушения анатомии венозных коллекторов малого круга кровообращения послужило основанием для проведения МСКТ в нашем исследовании у 19 пациентов. Наиболее тяжелой формой данной патологии является тотальный аномальный дренаж легочных вен. Этот порок на МСКТ отмечали у 6 детей, из них в 5 случаях дренаж осуществлялся в систему верхней полой вены (супракардиальная форма ТАДЛВ). У одного пациента отмечена инфракардиальная форма порока. При формировании оттока из легочных вен в верхнюю полую вену отмечали два типа анатомии. По нашим наблюдениям, наиболее часто (80 %) вены обоих легких формировали единый коллектор, располагающийся в средостении параверте-брально слева и впадающий в безымянную вену (рис. 4). Единичное наблюдение касалось перехода единой вены левого легкого в правую половину
грудной клетки, соединения ее с правыми легочными венами и впадение в верхнюю полую вену. У пациентов с ТАДВЛ при проведении обследования очень важно верифицировать наличие септального дефекта между предсердиями и состояние Ботал-лова протока для решения вопроса об атриосепто-томии [4]. Визуализация дефекта межпредсердной перегородки на МСКТ отмечена у всех больных с ТАДЛВ. Оценивать диагностическую эффективность метода в отношении размеров септального дефекта на столь малом количестве наблюдений было бы неправомерно, но можно отметить тенденцию высокой отрицательной прогностической значимости МСКТ в отношении крупных, более 1 см, дефектов. Наличие при ТАДЛВ функционирующего открытого артериального протока является спасительным механизмом оксигенации крови большого круга кровообращения в первые дни жизни пациента [9]. Достоверно определить наличие кровотока через Боталлов проток по данным МСКТ нам удалось у всех 6 пациентов с ТАДЛВ. При этом у 4 (66,7 %) детей отмечали закрытие протока или его субмиллиметровый просвет, что определило активную хирургическую тактику в их отношении.
До настоящего времени отсутствуют убедительные эхокардиографические критерии, позволяющие диагностировать частичный аномальный дренаж легочных вен (ЧАДЛВ) [4]. С использованием МСКТ нам удалось визуализировать непосредственно сам аномальный венозный сосуд, проследить его ход и локализовать устье дренажа. У всех 13 больных патологический сброс из мало-
го круга осуществлялся через правые легочные вены. В 9 случаях (69 %) отмечали супракарди-альную форму дренажа в систему верхней полой вены, интракардиальную форму диагностировали у 4 пациентов (31 %). Такое соотношение соответствовало распространенности данных форм ЧАДВЛ [4, 7]. Инфракардиальный тип ЧАДЛВ и сброс крови из левых легочных вен в нашей практике не встречались. Среди всех пациентов с ЧАДЛВ изолированный порок отмечали лишь в единичном случае. У остальных детей аномальный дренаж сочетался с дефектами межпред-сердной (92,3 %), межжелудочковой перегородок (38,5 %), транспозицией магистральных сосудов (23 %), тетрадой Фалло (15,4 %) и единственным желудочком (8 %).
При сравнительном анализе интраоперацион-ных данных, а также данных дополнительного зондирования камер сердца можно отметить высокую значимость МСКТ в диагностике транспозиции магистральных сосудов, двойного отхожде-ния магистральных сосудов от правого желудочка, атриовентрикулярной коммуникации и патологии клапанного аппарата. Ни в одном из этих случаев не выявлено расхождения данных об анатомии порока. Однако малое количество наших наблюдений таких ВПС не позволяет достоверно оценить диагностическую точность методики. Дальнейший набор материала даст возможность статистически подтвердить эффективность МСКТ при данных пороках развития.
Необходимо отметить диагностические возможности МСКТ в отношении сопутствующей некардиальной патологии у больных с ВПС. Мы расширили стандартный протокол обследования дополнительной постпроцессорной реконструкцией с изучением легочных полей в «мягкотканном» и «легочном» окнах. Изменения со стороны легких у обследованных пациентов в основном были представлены застойными явлениями, но в ряде случаев были отмечены сегментарная гиповентиляция одного из легких (5 пациентов), лобарная секвестрация (2 пациента), стенотические изменения бронхиального дерева (3 пациента). В 45 случаях дополнительно диагностированы инфильтратив-ные изменения, характерные для пневмонии.
Использование МСКТ, безусловно, сопряжено с контрастной и лучевой нагрузкой на пациента. Но необходимо отметить, что использование дифференцированного подхода к выбору рентгенкон-трастного препарата, подбору дозировки и скорости введения позволило снизить риск развития контраст-индуцированной нефропатии у наших пациентов. Оптимизация протокола сканирования
с подбором минимальных параметров дала возможность снизить суммарную эффективную дозу облучения при проведении МСКТ до 3,3-4,8 мЗв. Кроме того, выполнение данной диагностической процедуры позволило в большинстве случаев избежать инвазивного зондирования камер сердца.
Заключение
Использование мультиспиральной компьютерной томографии в диагностике врожденных пороков сердца у детей первых лет жизни позволяет получить точную анатомическую картину структур сердца, магистральных сосудов, морфометрические данные, касающиеся ВПС, оценить сопутствующую некардиальную патологию. Полученные данные определяют дальнейшую тактику лечения, планирование оперативной коррекции порока, дают возможность оценить результаты хирургического вмешательства.
ЛИТЕРАТУРА
1. Борисков М. В., Петшаковский П. Ю., Серова Т. В. Коаркгация аорты у новорожденных // Хирургия. 2010. № 10. С. 89-94.
2. Шмулевич С. А. Распространенность и структура врожденных пороков сердца на территории Кемеровской области // Вестник Кузбасского научною центра. Вып. 11: Актуальные вопросы здравоохранения: материалы Восьмой науч.-практ. конф. Кемерово, 2010. С. 221.
3. ALCAPA: the role of myocardial viability stadies in de-terming prognosis / L. Browne [et al.] // Pediatr Radiol. 2010. Vol. 40. P. 163-167.
4. Dillman J., Yarram S., Hernandez R. Imaging of Pulmonary Venous Developmental Anomalies // Am. J. Roentg. 2009. Vol. 192. P. 1272-1285.
5. Dillman J. Role of CT in the evaluation of congenital cardiovascular disease in children // Am. J. Roentg. 2009. Vol. 192. P. 121-1231.
6. Congenital heart disease in the general population : changing prevalence and age distribution / A. J. Marelli [et al.] // Circulation. 2007. Vol. 115. P. 163-172.
7. CT of congenital heart disease: normal anatomy and typical pathologic conditions / H. W. Goo [et al.] // Radiographies. 2003. Vol. 23. P. 147-165.
8. Gutierrez F., Mai-Lan Ho, Siegel M. Practical applications of magnetic resonance in congenital heart disease // Magn. Reson. Imaging. Clin. N. Am. 2008. Vol. 16. P. 403-435.
9. Kim T. H, Kim Y. М., Suh С. H. Helical CT angiography and three-dimensional reconstruction of total anomalous pulmonary venous connections in neonates and infants // Am. J. Roentg. 2000. Vol. 175. P. 1381-1386.
10. Three-dimensional helical computed tomographic angiography in neonates and infants with complex congenital heart disease / T. Kawano [et al.] // Am. Heart. J. 2000. Vol. 139. P. 654-660.
11. Van Praagh R. Terminology of congenital heart disease: glossary and commentary // Circulation. 1977. Vol. 56. P. 139-143.
Статья поступила 05.09.2013
Ответственный автор за переписку: Коков Александр Николаевич -заведующий лабораторией рентгеновской и томографической диагностики ФГБУ «НИИ КПССЗ» СО РАМН
Адрес для переписки: Коков А.Н., 650002, г. Кемерово, Сосновый бульвар, д. 6 Тел: 8(3842) 64-35-19 E-mail: [email protected]
Corresponding author:
Alexander N. Kokov -
head of roentgen and tomography diagnostics
laboratory of FSBI RI for CICVD,
SB RAMS
Correspondence address:
A. N. Kokov, 6, Sosnoviy blvd.,
Kemerovo, 650002 Tel.: +7 (3842) 64-35-19 E-mail: [email protected]
CDG
Быстро развивающая технология и новые клинические применения в сердечно-сосудистой обработке изображений, связанные с терапевтической опцией в сердечно-сосудистых болезнях, привело к быстрому развитию этой сферы.
В последнее время, арсенал диагностических неинвазивных инструментов вырос, одновременно с новостями из сферы контрастных веществ, компютерной томографии (КТ) для коронарной ангиограмы, и оценка кальция, а также и магнетический резонанс сердца, для миокардической структуры, функции и жизнеспособности. Эти прогрессы приносят новые возможности для врачей, дают им возможность использовать неинвазивные технологии для получения важных информаций о состояние их пациентов.Компютерная томография сердца
Исследование сердца лучами Х, также как електрокардиография (ЭКГ), стара как век. От первых сердечных исследований, до сих пор, технология сделала большие прогрессы в этой области. На сегодняшний день один из самых развитых методов диагностики с лучами Х является КТ, который позволяет высокий структурный обзор, васкуларизаций и функций сердца. В общем сложность в обследовании сердца зависит от ряда факторов, как : постоянное движение структур из-за сокращении, движение сердца определенная феноменом пульсации и респираторным движениям. Для получения качественных изображений с диагностической утилитации, систем КТ должен быть датирован современными техническими инновациями. Эти требования изображены через технической характеристики системы Siemens Somatom Sensation с которой оборудован ГДЦ. Трубка сканирования вращается со скоростью 0.28мс, что означает что в одну секунду он проделает 3 вращения. Имея доступ к 64 ряда детекторов получаем за одну секунду- 192 разделов. Это позволяет полностью сканировать сердце за 10- 14 сек., достаточное время чтоб пациент сдержал дыхание, и мы получили комплект изображений в количестве 1200- 5000, толщиной 0.6мм. Объяснение простое и не перечисляет комплексные технологии которые делают обследование возможным. Заслуживает внимание технология Care Dose 4D, которая в сочетание с модулем ЕКГ трубки, позволяет во многом уменьшить дозу радиации.Таким образом доза облучения часто бывает меньше чем у КТ живота.
 |
| Фиг. 1. Виртуальная реконструкция сердца и корональных артерии. |
Главный указатель КТ сердечно- сосудистой системы является оценка сосудов сердца, названных коронарных артерии, откуда и название двух расследований КТ коронарография. Сердечные артерии с возрастом часто бывают поражены атеросклерозом ( скопление жира на стенах сосудов). Атеросклеротические бляшки постепенно закрывают люмен (проход) и приводят к болям в груди, названных стенокардией и в 70% случаев могут причинить смерть сердечной мышцы, названный инфаркт миокарда.
Сегодня инфаркт миокарда является причиной номер 1 в смерть населения. Важен тот факт что в 50% случаев больные не жалуются и стенозы (сужения артерий) являются незначительны. КТ коронарографии позволяет обнаружению атеросклеротических бляшек, локализацию, количество и степень заражения. Диагностический метод рекомендуется больным у которых данный диагноз нестабилен, или имеет атипичную презентацию. Пациенты с таким диагнозом нуждаются в обследовании через Конвенциональную Коронарографию, которая является частичным инвазивным методом.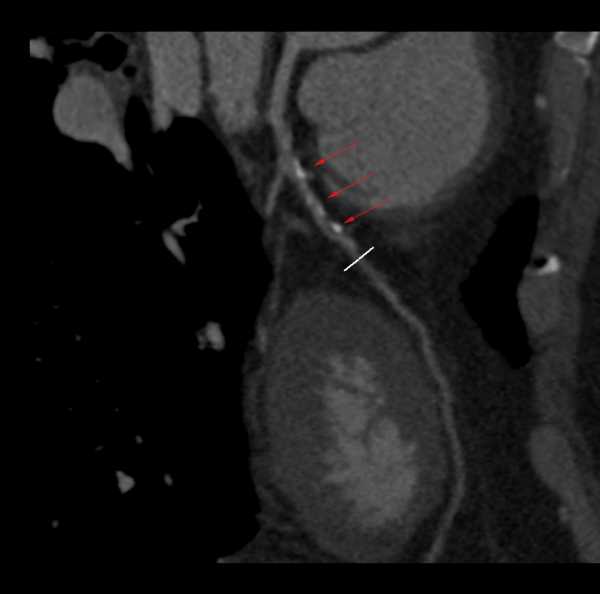 | 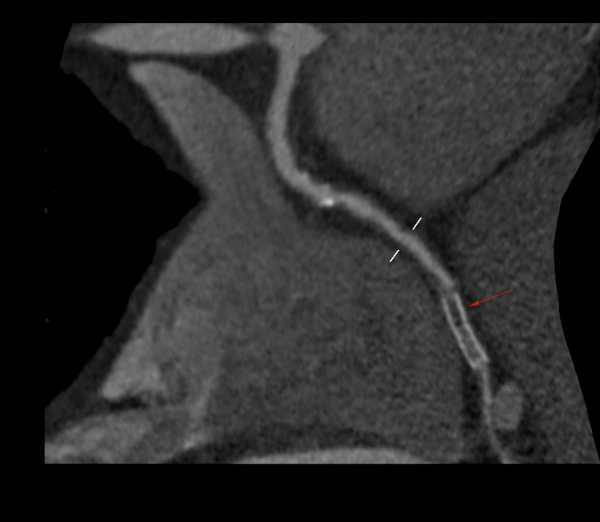 |
| Фиг. 2. Предыдущая левая нисходящая коронарная артерия представляет большинство атеросклеротических бляшек кальцифицированные и некальцифицированные. | Фиг. 3. Стент в среднем сегменте правой коронарной артерии. Проксимальный сегмент окклюзии (закрытия) стента тромбов. |
СКТ позволяет ставить точный диагноз перечисленных патологии и рекомендуется в случае противопоказаний для сердечной МРТ.
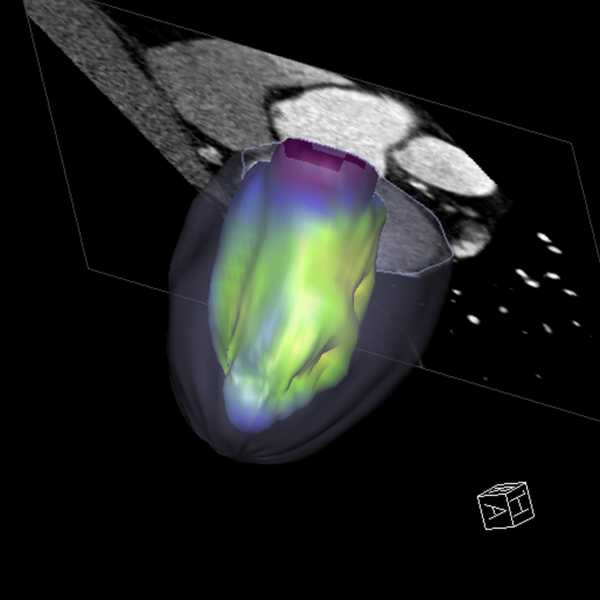 | 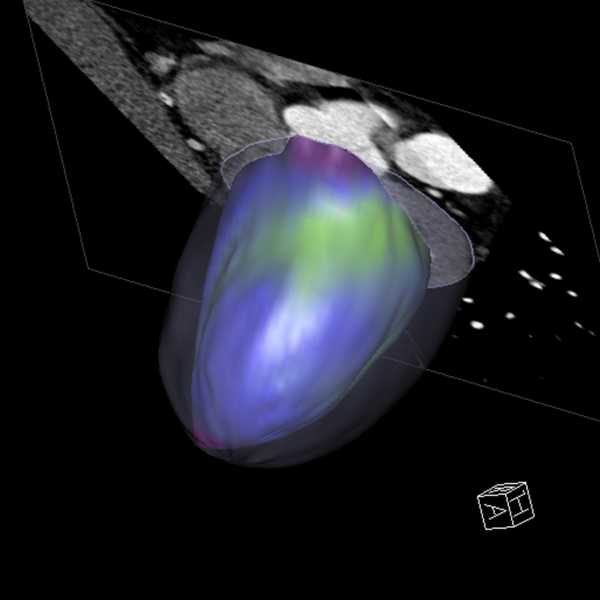 |
| Фиг. 4 – 5. Виртуальная реконструкция объема левого желудочка в систоле и диастоле. |
В заключении СКТ показания являются:
1. КТ коронарографии (КТК) у больных с подозрением на диагноз ишемической болезни сердца или атипичной клинической картины;2. КТК у больных со стентами или коронарными by-passuri;3. КТК при подозрении на аномалии развития коронарных артерии;4. СКТ у пациентов с врожденными сердечными аномалиями, для предоперационной и послеоперационной оценки, в случае противопоказании к МРТ сердца;5. СКТ в болезни сердечной мышце, перикардита, опухолей, и.т.д. в случае противопоказаний к сердечной МРТ (магнитная- резонансная томография);6. Как озвучивание для оценки прогноза у больных с подозрением на инфаркт миокарда с известными факторами риска.Процедура имеет определенную степень сложности и выполняется хорошо обученным персоналом. Пациенту требуется первичная консультация рентгенолога, который из жалоб пациента решает какой тип подготовки необходим, который занимает 30- 60 мин. В некоторых редких случаях пациент может быть перепрограммирован через 3 -4 дня, так как требуется специальное приготовление. Важно чтоб во время обследования пациент мог предоставить амбулаторную карточку, ЭКГ, и знал название принимаемых лекарств.
ВИДЕО:
| На виртуальной реконструкции, в правом нижнем квадрате виден стент коронарной артерии. В плане сердечного стендарта заметен инфаркт миокарда нижней боковой стенки, которая представляет утоньшение стенки и сокращение движении, то что снижает контрактную функцию левого желудочка. | |
| В левый верхний циферблат сердца просматриваются оценки глобальной функции сократимости левого желудочка. В правом нижнем циферблате рассматривается как меняется объем левого желудочка в различных фазах сокращения. | |
| Представлена структура митрального клапана и его функции (открытие и закрытие створок). | |
| Представлен митральный и аортальный клапан и нормальная функция выходного тракта левого желудочка. | |
| Представлена структура аортального клапана и его функции (открытие и закрытие створок). |
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе