Рост организма человека регулируется следующими гормонами
Гормоны регулирующие рост - Про щитовидку
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения щитовидки наши читатели успешно используют Монастырский чай. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
Наука эндокринология изучает железы внутренней секреции, их нарушения, а также выделяемые этими железами гормоны.
Гипоталамо-гипофизарная система — это тесная связь эндокринной и нервной части организма человека, поэтому ее называют нейроэндокринной системой.
Чтобы понять, как работают органы эндокринной системы нужно знать их анатомию и механизм синтеза.
Как работают эндокринные органы:
- эндокринные железы, синтезируют гормоны;
- они транспортируются различными путями;
- их принимают ткани соответствующих органов.
Без нормального функционирования эндокринной системы невозможна здоровая работа органов и систем человеческого организма. 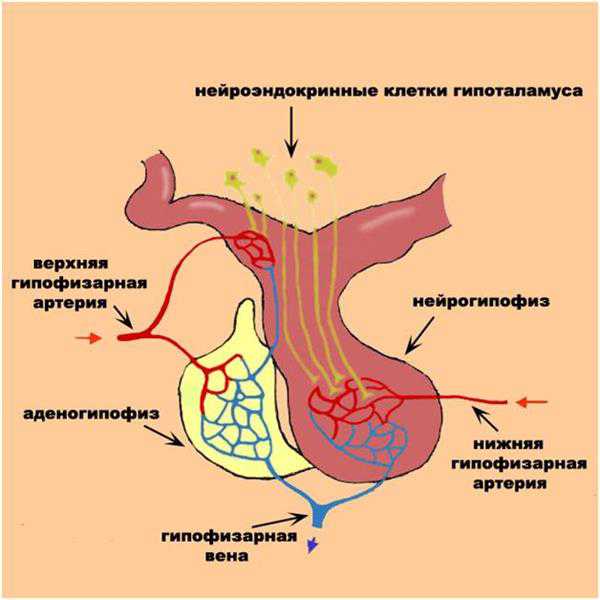
- Железы внутренней секреции и их гормоны
- Гипоталамус
- Гипофиз
- Эндокринный щитовидный орган
- Надпочечники
- Поджелудочная железа
- Половые железы
- Почки, сердце и центральная нервная система как эндокринные железы
Железы внутренней секреции и их гормоны
| Гипофиз | Меланоцитостимулирующий гормон (полипептид) |
| Гипоталамус | Гормон рилизинг – фактор (полипептид) |
| Щитовидная железа | Тиреокальцитонин, тироксин, трийодтиронин (полипептид) |
| Околощитовидныежелезы | Партгормон (белки) |
| Поджелудочная железа | Глюкагон, инсулин, соматостатин (белки, полептиды) |
| Надпочечники, гормоны коркового вещества | Кортизол, эстрогены, андрогены, кортикостерон, альдостерон, прогестерон (стероиды). |
| Надпочечники, гормоны мозгового вещества | Норадреналин, адреналин (катехоламины) |
| яичники | стероиды |
| Семенники, яички | стероиды |
Гормоны – вещества, отличающиеся высокой активностью, их синтезируют железы внутренней секреции.
Эти вещества делят в зависимости от их химического строения. Смотрите таблицу:
| Полипептиды, белковые. |
| Стероидные. |
| Производимые аминокислотами. |
Свойства гормонов представлены в таблице:
| Биологическая активность. |
| Дистанционное воздействие. |
| Избирательность и специфичность. |
Небольшое количество гормонов в крови, оказывает явное действие на органы и системы. Точки их воздействия находятся на расстоянии от эндокринных желез.
Специфичность и избирательность заключается в их воздействии на органы и ткани, называемые мишенями. Гормоны взаимодействуют с ними, благодаря рецепторам, белковым молекулам, способным трансформировать сигнал в действие, вызывающие определенные изменения в органах.
Гипоталамус
Расположен в мозге, обладает свойствами эндокринной и нервной систем. В гипоталамусе синтезируются вазопрессин и окситоцин, транспортируемые в гипофиз, они регулируют работу репродуктивной системы и почек.
Гипофиз
Гипофиз вырабатывает тропные гормоны. Он расположен у основания мозга, в месте, называемом турецкое седло. Вещества, вырабатываемые гипофизом, указаны в таблице.
| Гормон роста | Регулирует рост, образование глюкозы и белка, усвоение жиров. |
| Кортикотропин | Отвечает за выработку глюкокортикоидов |
| Тиреотропин | Стимулирует выработку тиреоидных веществ в щитовидной железе. |
| Гонадотропин | Отвечает за синтез репродуктивных гормонов как женских, так и мужских. |
| Пролактин | Регулирует лактацию. |
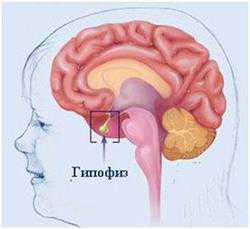
Эндокринный щитовидный орган
Железа синтезирует йодосодержащие: тиреокальцитонин, тироксин, трийодтиронин, вещества, регулирующие обмен фосфора, кальция, уровень энергозатрат, необходимых для всего организма.
Околощитовидные железы продуцируют паратгормон, повышающий содержание кальция и фосфора в крови и поддерживающий его на необходимом уровне.
Нормальная работа щитовидной железы и ее продуктивность обеспечивается постоянным поступлением элемента йод в количестве до 200 мкг. Йод человек получает с пищей, водой и воздухом.
 Йод в кишечнике расщепляется на йодиды и захватывается щитовидной железой. Синтез тиреоидных веществ осуществляется только чистым элементарным йодом, получаемым при помощи ферментов цитохромоксидазы и пероксидазы. Поступление йодидов в щитовидку и их окисление осуществляет гипофизарный тиреотропин.
Йод в кишечнике расщепляется на йодиды и захватывается щитовидной железой. Синтез тиреоидных веществ осуществляется только чистым элементарным йодом, получаемым при помощи ферментов цитохромоксидазы и пероксидазы. Поступление йодидов в щитовидку и их окисление осуществляет гипофизарный тиреотропин.
Недостаток йода – основная причина проблем щитовидной железы и гормональной недостаточности, вызывающих нарушение в работе всех органов, падение иммунитета и снижение интеллектуальной активности.
Функционирование аденогипофиза и щитовидной железы осуществляется гипоталамусом, главным регулятором эндокринной системы. Тиролиберин, вырабатываемый этим органом, стимулирует производство тиреотропина в гипофизе.
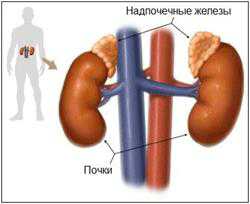 Гормоны в надпочечниках выделяются в мозговом и корковом веществе. В корковом веществе синтезируются кортикостероиды.
Гормоны в надпочечниках выделяются в мозговом и корковом веществе. В корковом веществе синтезируются кортикостероиды.
Корковое вещество делится на три зоны, в которых продуцируются гормоны, указанные в таблице.
| Зона клубочковая | минералокортикоиды | альдостерон, дезоксикортикостерон | Контролируется минеральный обмен |
| Пучковая | глюкокортикоиды | кортикостерон, кортизол | контролируется обмен белков, жиров, углеводов |
| Сетчатая | Половые гормоны | андрогены |
Мозговое вещество поставляет в кровь катехоламины: норадреналин и адреналин. Норадреналин регулирует нервные процессы в симпатической зоне.
 Катехоламины регулируют жировой и углеводный обмен, помогают организму адаптироваться к стрессу, выделяя адреналин в ответ на эмоциональные раздражения (боль, радость, волнение, ужас, злость). Адреналин не зря называют гормоном эмоций.
Катехоламины регулируют жировой и углеводный обмен, помогают организму адаптироваться к стрессу, выделяя адреналин в ответ на эмоциональные раздражения (боль, радость, волнение, ужас, злость). Адреналин не зря называют гормоном эмоций.
Поджелудочная железа
Эндокринная часть железы, называемая островки Лангерганса производит глюкагон, инсулин, соматостатин.
- Инсулин регулирует жировой, белковый и углеводный обмен.
- Глюкагон – стимулятор глюкозной секреции инсулина.
- Соматостатин подавляет синтез гормона роста, инсулина и глюкагона.
Нарушение производства глюкагона и инсулина приводит к диабету. 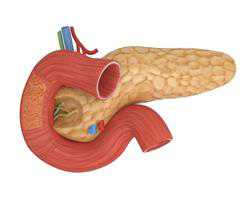
Половые железы
Синтезируют не только гормоны, также яйцеклетки женские и сперматозоиды мужские. Сперматозоиды продуцируются в мужских семенниках. Их выработке способствуют андрогены. Женские яичники вырабатывают эстрогены. Их специализация — женские половые признаки, их развитие. Яичники вырабатывают и прогестерон, необходимый для вынашивания потомства. Контроль над синтезом половых клеток осуществляется аденогипофизом.
Почки, сердце и центральная нервная система как эндокринные железы
Кроме выделительной функции, почки осуществляют и эндокринную. Юкстагломерулярный аппарат синтезирует ренин, регулирующий тонус сосудов. Синтезируют почки и эритропоэтин, отвечающий за эритроциты костного мозга.
Сердце также является частью эндокринной системы, натрийуретический гормон, производимый в предсердии, влияет на производство почками натрия.
Энкефалины и эндорфины — гормоны эндокринной и нервной систем, синтезируются в ЦНС, их задача – обезболивание, поэтому их еще называют «Эндрогенные опиаты». Нейрогормоны действуют по типу морфина.
Гормональный сбой щитовидной железы, симптомы которого могут свидетельствовать о других заболеваниях, может произойти в любом возрасте. Выработка гормонов может повышаться или понижаться под действием определенных факторов. Щитовидная железа является небольшим органом весом всего 25-40 г, напоминающим бабочку из-за своей формы строения (две боковые доли соединяются перешейком).
Основные гормоны, которые она вырабатывает, — это кальцитонин и тироксин. Кальцитонин обладает гипокалиемическим и гипофосфатемическим действием, а также поддерживает необходимый баланс кальция в крови. Тироксин влияет на рост и развитие всех систем организма. Выработка этих двух гормонов важна для энергетического, белкового, жирового, углеродного, кислородного, водно-минерального обменных процессов. Также гормоны регулируют работу сердечно-сосудистой, нервной и репродуктивной систем.
Из этого следует, что работа этого крохотного органа влияет на весь организм в целом. Однако распознать нарушения его функций сразу бывает не просто. Большинство симптомов проявляются таким образом, что человек не подозревает о нарушениях в работе щитовидной железы. В итоге к лечению прибегают уже на поздней стадии того или иного заболевания.
Недостаток и переизбыток гормонов, вырабатываемых щитовидной железой, сказываются негативно на самочувствии человека.
Причины гипертиреоза щитовидной железы
Под гипертиреозом подразумевается патологический процесс, вызванный чрезмерной выработкой гормонов. Существуют 3 вида гипертиреоза. Первичный вид гиперфункции связан с изменением самого органа. Это могут быть увеличение размеров, воспалительные процессы или аутоиммунные реакции. Причина вторичного гипертиреоза связана с нарушением функциональности гипофиза, который регулирует баланс гормонов.
Третичный вид гипертиреоза формируется на фоне патологического функционирования гипоталамуса.
Заболевания, вызывающие гипертиреоз:
- токсический зоб;
- заболевание Пламмера;
- опухолевые образования коры гипофиза;
- тиреоидит (воспаление железы).
Токсический зоб чаще наблюдается у женщин от 20 до 50 лет, чем у мужчин. 75% всех случаев гиперфункции щитовидной железы связаны именно с токсическим зобом. Данное заболевание представляет опасность для жизни и требует немедленного лечения. Переизбыток гормонов оказывает токсическое воздействие на все системы организма.
Заболевание Пламмера, или синдром Пламмера, — это доброкачественная опухоль щитовидной железы. Данное заболевание диагностируется с помощью УЗИ. При обследовании виден узелок округлой формы со специфическим ободком. Опухолевые образования коры гипофиза становятся чаще причиной вторичного гипертиреоза. В этом случае диагностика затруднительна, так как видимых повреждений органа не наблюдается.
Причины уменьшения выработки гормонов
Состояние, когда щитовидная железа вырабатывает недостаточное количество гормонов, называется гипотиреоз. Такой гормональный сбой встречается чаще у женщин. Диагностировать заболевание сложно по причине медленного и плавного развития и отсутствия ярких проявлений. Гипотиреоз, как и гипертиреоз, также имеет свою классификацию.
Различают первичный, вторичный и третичный гипотиреоз. Этот недуг может быть врожденным или приобретенным. Первичный гипотиреоз формируется на фоне различных патологических процессов щитовидной железы. Вторичный вид развивается при поражениях гипофиза, который не вырабатывает ТТГ (тиреотропный гормон). Врожденный гипотиреоз формируется у человека еще при внутриутробном развитии. Третичный вид гипотиреоза развивается при нарушении процессов гипоталамуса.
Причинами первичного гипотиреоза являются:
- избыток йода;
- подострый тиреоидит;
- лечение препаратами лития;
- частичное удаление щитовидной железы;
- аутоиммунный тиреоидит;
- врожденный дефицит ТТГ;
- эндемический зоб;
- патологии щитовидной железы;
- опухоли гипофиза;
- массивная кровопотеря;
- нейроинфекции головного мозга;
- травмы головного мозга с повреждением гипофиза;
- отсутствие лечения заболеваний щитовидной железы.
Прогрессирование гипотиреоза ведет к торможению обменных процессов в организме. Это заболевание считается функциональным расстройством с осложнениями органического характера. Из-за недостатка гормонов происходит нарушение структуры органов, которые зависимы от них. Сама щитовидная железа тоже меняет свою структуру по причине патологии, которая вызвала гипотиреоз.
Как распознать гормональные нарушения?
Учитывая то, какую огромную роль играет щитовидная железа в работе всего организма, дисбаланс гормонов сразу же сказывается не только на физическом состоянии, но и на психоэмоциональном. Однако ситуация такова, что часто люди путают симптомы гипертиреоза и гипотиреоза с другими болезнями и пытаются лечиться самостоятельно. При этом все усилия направлены на устранение симптоматики, а не самой болезни, о которой человек даже не подозревает.
При гипертиреозе процессы в организме происходят в ускоренном темпе из-за быстрого синтеза гормонов. Это сказывается на работе сердечно-сосудистой системы в первую очередь. Меняется внешний вид человека, потому что у пациентов с таким недугом заметно расширены глазные прорези, а само глазное яблоко выпячивается. Создается впечатление, что человек словно удивлен или перепуган. Со временем перенапряжение глазных нервов может привести к частичной или полной слепоте.
Усиленная выработка гормонов сопровождается дополнительными симптомами в виде:
- учащенного сердцебиения;
- аритмии;
- повышенного артериального давления;
- расстройства пищеварения;
- повышения температуры тела;
- частого ощущения жара;
- дрожи конечностей;
- сонливости;
- вялости, быстрой утомляемости;
- флегматичности;
- повышенного аппетита;
- боязни яркого света;
- диареи;
- раздражительности;
- чрезмерной обидчивости;
- страха;
- тревоги и беспокойства;
- бессонницы на фоне нервозности;
- жажды;
- учащенного мочеиспускания.
У беременных женщин ко всем описанным симптомам могут добавиться чрезмерное слезотечение и потоотделение, опухоль век, ухудшение зрения. Диарея свойственна детям при субклиническом гипертиреозе.
Под действием гормонов наблюдается повышенная мозговая активность. Больной может очень быстро говорить, при этом речь его бессвязная и спутанная. При гипертиреозе выпадают волосы, ногти становятся ломкими, а кожа — влажной и тонкой. Происходят нарушения в репродуктивной и половой системах как мужчин, так и женщин.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения щитовидки наши читатели успешно используют Монастырский чай. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
Описание признаков гипотиреоза
Симптомы гипотиреоза напрямую зависят от этиологии заболевания, возраста больного и скорости развития недуга. Проблема заключается в постановке диагноза, так как при дефиците гормонов нет таких проявлений, которые были бы характерны только для этого заболевания. Признаки гипотиреоза очень похожи с другими соматическими и психическими болезнями.
Пациентов с гипотиреозом беспокоят такие симптомы:
- ухудшение интеллекта;
- снижение памяти;
- депрессия;
- сонливость;
- запоры;
- тошнота;
- дискинезия желчных путей;
- бледность и сухость кожи;
- отечность;
- увеличение массы тела;
- одышка;
- боли в области сердца;
- брадикардия;
- постоянное ощущение холода;
- выпадение волос;
- ломкость ногтей;
- анемия;
- частичная потеря слуха;
- снижение либидо;
- нарушение менструального цикла;
- бесплодие;
- ранний атеросклероз;
- гипотония;
- изменения тембра голоса из-за отеков.
При гормональном сбое щитовидной железы симптомы, описанные выше, наблюдаются при множестве других заболеваний. Поэтому вялость, усталость списывают на трудный рабочий день, проблемы с ЖКТ — на плохое питание, а женскую депрессию — на ПМС. Однако при наличии такой симптоматики важно пройти обследование на функциональность щитовидной железы.
При отсутствии лечения гипотиреоз вызывает серьезные осложнения, особенно у детей.
Самым тяжелым последствием гормонального сбоя является гипотиреоидная кома. Развивается она чаще всего у людей преклонного возраста. Дети, которым не проводилась надлежащая терапия этой болезни, имеют задержку физического роста и отклонения в умственном развитии. При врожденном гипотиреозе человеку придется всю жизнь принимать препараты, регулирующие уровень необходимых гормонов.
Важные и незаменимые гормоны щитовидки
Щитовидная железа является важнейшим органом эндокринной системы.
Паренхима щитовидки представлена двумя долями, которые соединены между собой перешейком.
Внешне орган напоминает бабочку с большими симметричными крыльями.
Щитовидка охватывает трахею, рядом проходят крупные кровеносные сосуды шеи.
С диагностической точки зрения важным показателем являются размеры долей:
- ширина каждой доли в норме не превышает 2 см;
- длина –4 см;
- толщина — 1- 1,5 см.
У взрослого человека вес органа находится в диапазоне от 12 до 25г.
У детей первого месяца жизни масса щитовидной железы не превышает 3г.
В норме объем щитовидной железы составляет:
- у мужчин не более 25 мл;
- у женщин не более18 мл.
Важно подчеркнуть, что вес и объем щитовидки индивидуальны и могут изменяться даже при нормальных физиологических процессах.
В частности, у женщин в разные периоды менструального цикла вес и объем органа могут меняться.
Функции гормонов
Щитовидная железа — одна из желез внутренней секреции, гормоны которой чрезвычайно важны для жизнедеятельности человека.
Щитовидка синтезирует:
Основной гормон щитовидной железы, вырабатывается ее фолликулярными клетками.
Воздействует на все ткани тела, проникает в межклеточное вещество, влияет на обмен веществ.
Стимулирует синтез белков РНК, посредством этого активирует метаболизм.
Управляет ростом и развитием организма, сокращениями сердца.
Отвечает за обмен кислорода в тканях.
Способствует формированию ЦНС, росту скелета у детей.
Ускоряет белковый обмен и метаболизм, нормализует обмен веществ в костях.
Снижает уровень холестерина.
Стимулирует выработку витамина А.
Только треть гормона поступает в организм в чистом виде, остальное – продукт распада тироксина, попавшего в кровь и потерявшего атом йода.
Регулирует фосфорно-кальциевый обмен, баланс клеток костной ткани – остеокластов и остеобластов.
Синтезируется парафолликулярными клетками щитовидной железы.
Также производится вилочковой железой и околощитовидными железами.
Эти вещества регулируют обмен веществ и поддерживают гомеостаз.
Под воздействием тиреоидных гормонов происходит рост и дифференциация клеток.
От уровня гормонов щитовидки зависят следующие процессы:
- поддержание нормальной температуры тела;
- кроветворение;
- появление и передача нервного импульса;
- регуляция частоты и силы сокращений сердечной мышцы.
Тиреоидные гормоны регулируют деятельность всей эндокринной системы, в связи с чем в медицинских кругах щитовидку называют «дирижером оркестра».
Изменения функциональной активности железы приводит к серьезным сбоям в организме.
Избыточная активность
Повышенная секреция тиреоидных гормонов носит название гипертиреоз.
Превышающая норму концентрация тироксина и трийодтиронина в крови наносит ущерб всему организму.
Основные болезни, которые появляются при гиперфункции щитовидной железы:
- болезнь Базедова;
- болезнь Пламмера;
- подострый тиреоидит;
- искусственный гипертиреоз.
Болезнь Базедова является аутоиммунным заболеванием, от этой патологии страдают лица с наследственной предрасположенностью.
У женщин Базедова болезнь встречается в 8 раз чаще, чем у мужчин. Факторами, которые влияют на развитие болезни, являются:
- психические травмы;
- инфекционные заболевания;
- травмы головы;
- заболевания носоглотки.
Болезнь Пламмера или аденома щитовидной железы — один из видов доброкачественной опухоли, представляющий собой узел на фоне гипертиреоза.
В эндокринологии описание клинической картины патологии включает неспецифическую симптоматику.
Подострый тиреоидит — воспаление щитовидной железы, в образовании которого участвуют аутоиммунные механизмы.
Чаще встречается у женщин в возрасте 30-60 лет. Различают два вида подострого тиреоидита:
- тиреоидит де Кервина;
- подострый лимфоцитарный тиреоидит.
Искусственный тиреотоксикоз, как правило, является следствием приема препаратов щитовидной железы.
В 97% случаев причиной появления патологии является самолечение.
Недостаточная активность
Недостаточная функциональная активность щитовидки называется гипотиреоз.
Это состояние можно охарактеризовать, как длительный и стойкий недостаток в организме гормонов щитовидной железы.
Выделяют несколько видов патологии:
- первичный;
- вторичный;
- третичный.
К первичному гипотиреозу приводят следующие факторы:
- врожденное нарушение синтеза тиреоидных гормонов;
- особенности питания, недостаток йода;
- удаление железы или лучевая терапия.
Вторичный гипотиреоз связывают с недостатком гормонов гипофиза или гипоталамуса.
Третичный гипотиреоз возникает в связи со снижением выработки тиреотропина или со снижением чувствительности эпителиальных клеток щитовидки.
Как выявить отклонения от нормы?
Несмотря на то, что тиреоидные гормоны оказывают влияние практически на все процессы жизнедеятельности, обнаружить патологию на ранней стадии трудно.
Симптомы заболеваний носят неспецифический характер, большинство пациентов связывают свое состояние с переутомлением и стрессами.
Признаками дисфункции щитовидной железы могут являться:
- нарушение водного баланса кожного покрова;
- общая слабость и разбитость;
- головные боли, мигрени;
- резкие перепады в весе;
- нарушение менструального цикла;
- сбои терморегуляции.
В более чем 80% случаев первое обращение к эндокринологу связано с заметным увеличением щитовидки.
В тот момент, когда на передней поверхности шеи появляется выраженный дефект, пациент понимает, что причина – не в переутомлении и вероятнее всего он болен.
Обнаружить патологию щитовидки на более ранней стадии можно в рамках профилактических медицинских осмотров.
Кроме того, каждый желающий может сдать анализ на исследование гормонального фона.
Что делать, если функция щитовидки нарушена?
Появление тревожных симптомов — повод обратиться к специалисту.
Для постановки точного диагноза назначают следующие анализы:
| УЗИ для выявления увеличения, или наличия узлов в щитовидной железе; |
| анализ уровня тиреоидных гормонов; |
| сканирование с помощью радиоактивного йода; |
| анализ на антитела к рецепторам тиреотропного гормона; |
| КТ или МРТ при подозрении на заболевания гипофиза. |
Из дополнительных анализов могут быть назначены общий анализ крови, иммунограмма и коагулограмма.
В случаях узловых образований проводят тонкоигольную биопсии с последующим гистологическим анализом тканей.
После постановки точного диагноза назначается соответствующее лечение.
Важно подчеркнуть, что в процессе терапии пациенты также сдают все необходимые анализы, поскольку только динамическое наблюдение за показателями позволяет корректировать дозировки лекарств.
Для нормализации функции щитовидной железы при гипотиреозе назначают препараты тироксина.
В подавляющем большинстве случаев секреция гормонов не возвращается к нормальному уровню, поэтому прием лекарств должен продолжаться всю жизнь.
Фармакологический эффект от лекарств развивается в течение 10-12 недель, поэтому повторять анализы рекомендуется раз в три месяца.
При гиперфункции щитовидки используют препараты, подавляющие выработку гормонов.
Но даже при длительном курсе лечения рецидивы возникают более чем у половины пациентов.
На поздних стадиях патологии, при формировании зоба и при серьезных нарушениях витальных функций, показано оперативное лечение.
Полная или частичная резекция органа также проводится при неэффективности медицинского вмешательства.
После операции возникает хронический недостаток гормонов, поэтому медикаментозное лечение продолжают в течение всей жизни.
Щитовидная железа нуждается во внимании. Следует регулярно сдавать анализы, тщательно следить за своим самочувствием и проходить ежегодное обследование у эндокринолога.
Пациенты, которые употребляют в пищу достаточно йода, на 85% реже страдают болезнями щитовидки.
3. Влияние гормонов на рост организма
Ростовые процессы в организме определяются действием ряда гормональных факторов. Основным из них является соматотропин – гормон передней доли гипофиза. Под его влиянием происходит новообразование хрящевой ткани эпифизарной зоны и увеличение длины трубчатых костей. Одновременно под влиянием соматотропина активизируется образование мягкой соединительной ткани, что важно для обеспечения надежности соединения частей растущего скелета. Он оказывает стимулирующее действие и на развитие скелетной мышечной ткани.
влияние соматотропина резко снижается при недостаточном содержании в крови тиреоидных гормонов и инсулина. Тиреоидные гормоны необходимы для нормализации процессов размножения и дифференцировки клеток. Классическими признаками, характеризующими нарушение роста и развития детей и подростков при гипотиреозе, являются отставание длины тела, запаздывание окостенения скелета и развития зубов. Эти проявления сочетаются с замедлением частоты сердечных сокращений, понижением артериального давления, уменьшением тонуса и силы скелетных мышц.
Не менее значительна роль инсулина. Так, он увеличивает транспорт аминокислот через мембраны и участвует в обеспечении белкового синтеза строительных материалов. Кроме того, инсулин способствует углеводному питанию клеток.
Опосредованное влияние на рост оказывает тестостерон. Он стимулирует белковый синтез в хрящевой и костной ткани, скелетных мышцах, миокарде, печени, почках. В наибольшей степени это проявляется в период полового созревания. Стимулирующее воздействие на рост продолжается до закрытия эпифизарных зон роста.
эстрогены на общий рост организма оказывают тормозящее влияние, активизируя окостенение эпифизарных зон роста трубчатых костей. Эстрогены стимулируют рост и белковый синтез в женских половых органах и в меньшей степени в почках, печения, миокарде.
Нормальное протекание ростовых процессов обеспечивается также паратгормоном, кальцитонином и гормональной формой витамина Д3. Данная группа гормонов имеет первостепенное значение в формировании костной ткани и в поддержании гомеостаза кальция во внутренней среде организма и в клетках. Кальцитонин и паратгормон воздействуют на кальциевый обмен в тесном взаимодействии с гормональной формой витамина Д3, образующейся из холекальцифирола, поступающего с пищей.
Совершенно противоположный эффект на рост организма оказывают глюкокортикоиды. Так, при лечении детей и подростков массивными дозами глюкокортикоидов отмечается задержка роста. Этим можно объяснить задержку роста при действии на организм стрессирующих факторов независимо от их природы. Так, при стрессе активируется вся система кортиколиберин-кортикотропин-глюкокортикоиды.
Учитывая этот факт, необходимо исключать продолжительное действие на детский организм стрессирующих факторов, в том числе и физические нагрузки большого объема и интенсивности, а также частое участие в соревнованиях.
Влияние гормонов на развитие нервной системы и поведение. Из гормональных факторов, оказывающих влияние на развитие ЦНС, наиболее значимы гормоны щитовидной железы.
Недостаточное содержание гормонов в последнем триместре беременности и первые недели после рождения является причиной развития такого заболевания как кретинизм. Высока роль тиреодных гормонов и в первые 18 месяцев после рождения. Дефицит тироксина и трийодтиронина резко затормаживают дифференцировку нервных клеток. Если недостаток указанных гормонов возникает после 18 месяцев то нарушается в основном рост, а дефекты умственного развития выражены слабее. Раннее введение тиреоидных гормонов способствует восстановлению умственного развития. было установлено, что дефицит гормонов щитовидной железы в критические периоды развития мозга приводит к снижению синтеза белков в мозговой ткани и уменьшению содержания в ней белково-синтетических ферментов. Нарушается также развитие сосудистой системы мозга, задерживается морфологическая дифференцировка коры больших полушарий и мозжечка. Следовательно, тиреоидные гормоны необходимы для структурного, биохимического и функционального созревания мозговой ткани.
значительное влияние на нервную систему оказывают гормоны надпочечников, изменяя силу нервных процессов. Удаление коры надпочечных желез сопровождается нарушением функции всей ВНД.
Половые гормоны влияют на соотношение процессов возбуждения и торможения. На работоспособность нервной системы в большей степени оказывают влияние мужские половые гормоны. Решительность, агрессивность также определяется концентрацией мужских половых гормонов. Удаление половых желез или их патологическое недоразвитие в детском возрасте вызывает нарушение психики и нередко приводит к умственной неполноценности.
Оптимальные физические нагрузки повышают резервные возможности эндокринной системы и, тем самым, опосредованно влияют на общее состояние нервной системы и всего организма.
Характеристика отдельных гормонов организма
Гормоны передней доли гипофизаГипофиз занимает особое положение в системе эндокринных желез. Его называют центральной железой, так как за счет его тропных гормонов регулируется деятельность других эндокринных желез. Гипофиз – сложный орган, он состоит из аденогипофиза (передней и средней долей) и нейрогипофиза (задней доли). Гормоны передней доли гипофиза делятся на две группы: гормон роста и пролактин и тропные гормоны (тиреотропин, корти-котропин, гонадотропин).
К первой группе относят соматотропин и пролактин.
Гормон роста (соматотропин) принимает участие в регуляции роста, усиливая образование белка. Наиболее выражено его влияние на рост эпифизарных хрящей конечностей, рост костей идет в длину. Нарушение соматотропной функции гипофиза приводит к различным изменениям в росте и развитии организма человека: если имеется гиперфункция в детском возрасте, то развивается гигантизм; при гипофункции – карликовость. Гиперфункция у взрослого человека не влияет на рост в целом, но увеличиваются размеры тех частей тела, которые еще способны расти (акромегалия).
Пролактин способствует образованию молока в альвеолах, но после предварительного воздействия на них женских половых гормонов (прогестерона и эстрогена). После родов увеличивается синтез пролактина и наступает лактация. Акт сосания через нервно-рефлекторный механизм стимулирует выброс пролактина. Пролактин обладает лютеотропным действием, способствует продолжительному функционированию желтого тела и выработке им прогестерона. Ко второй группе гормонов относят.
1) тиреотропный гормон (тиреотропин). Избирательно действует на щитовидную железу, повышает ее функцию. При сниженной выработке тиреотропина происходит атрофия щитовидной железы, при гиперпродукции – разрастание, наступают гистологические изменения, которые указывают на повышение ее активности;
2) адренокортикотропный гормон (кортикотропин). Стимулирует выработку глюкокортикоидов надпочечниками. Кортикотропин вызывает распад и тормозит синтез белка, является антагонистом гормона роста. Он тормозит развитие основного вещества соединительной ткани, уменьшает коли-
чество тучных клеток, подавляет фермент гиалуронидазу, снижая проницаемость капилляров. Этим определяется его противовоспалительное действие. Под влиянием кортикотропина уменьшаются размер и масса лимфоидных органов. Секреция кортикотропина подвержена суточным колебаниям: в вечерние часы его содержание выше, чем утром;
3) гонадотропные гормоны (гонадотропины — фоллитропин и лютропин). Присутствуют как у женщин, так и у мужчин:
а) фоллитропин (фолликулостимулирующий гормон), стимулирующий рост и развитие фолликула в яичнике. Он незначительно влияет на выработку эстрагенов у женщин, у мужчин под его влиянием происходит образование сперматозоидов;
б) лютеинизирующий гормон (лютропин), стимулирующий рост и овуляцию фолликула с образованием желтого тела. Он стимулирует образование женских половых гормонов – эстрагенов. Лютропин способствует выработке андрогенов у мужчин.
Гормоны средней и задней долей гипофиза
В средней доле гипофиза вырабатывается гормон меланотропин (интермедии), который оказывает влияние на пигментный обмен.
Задняя доля гипофиза тесно связана с супраоптическим и паравентрикулярным ядром гипоталамуса. Нервные клетки этих ядер вырабатывают нейросекрет, который транспортируется в заднюю долю гипофиза. Накапливаются гормоны в питуицитах, в этих клетках гормоны превращаются в активную форму. В нервных клетках паравентрикулярного ядра образуется окситоцин, в нейронах супраоптического ядра – вазопрессин.
Вазопрессин выполняет две функции: 1) усиливает сокращение гладких мышц сосудов (тонус арте-риол повышается с последующим повышением артериального давления); 2) угнетает образование мочи в почках (антидиуретическое действие). Антидиуретическое действие обеспечивается способностью вазопрессина усиливать обратное всасывание воды из канальцев почек в кровь. Уменьшение образования вазопрессина является причиной возникновения несахарного диабета (несахарного мочеизнурения).
Окситоцин (оцитоцин) избирательно действует на гладкую мускулатуру матки, усиливает ее сокращение. Сокращение матки резко увеличивается, если она находилась под воздействием эстрогенов. Во время беременности окситоцин не влияет на сократительную способность матки, так как гормон желтого тела прогестерон делает ее нечувствительной ко всем раздражителям. Окситоцин стимулирует выделение молока, усиливается именно выделительная функция, а не его секреция. Особые клетки молочной железы избирательно реагируют на окситоцин. Акт сосания рефлекторно способствует выделению окситоцина из нейрогипофиза.
Гипоталамическая регуляция образования гормонов гипофиза
Нейроны гипоталамуса вырабатывают нейросекрет. Продукты нейросекреции, которые способствуют образованию гормонов передней доли гипофиза, называются либеринами, а тормозящие их образование – статинами. Поступление этих веществ в переднюю долю гипофиза происходит по кровеносным сосудам.
Регуляция образования гормонов передней доли гипофиза осуществляется по принципу обратной связи. Между тропной функцией передней доли гипофиза и периферическими железами существуют двусторонние отношения: тропные гормоны активируют периферические эндокринные железы, последние в зависимости от их функционального состояния тоже влияют на продукцию тропных гормонов. Двусторонние взаимоотношения имеются между передней долей гипофиза и половыми железами, щитовидной железой и корой надпочечников. Эти взаимоотношения называют «плюс-минус» взаимодействия. Тропные гормоны стимулируют («плюс») функцию периферических желез, а гормоны периферических желез подавляют («минус») продукцию и выделение гормонов передней доли гипофиза. Существует обратная связь между гипоталамусом и тропными гормонами передней доли гипофиза. Повышение концентрации в крови гормона гипофиза приводит к торможению нейросекрета в гипоталамусе.
Симпатический отдел вегетативной нервной системы усиливает выработку тропных гормонов, парасимпатический отдел угнетает.
Гормоны эпифиза, тимуса, паращитовидных железЭпифиз находится над верхними буграми четверохолмия. Значение эпифиза крайне противоречиво. Из его ткани выделены два соединения:
1) мелатонин (принимает участие в регуляции пигментного обмена, тормозит развитие половых функций у молодых и действие гонадотропных гормонов у взрослых). Это обусловлено прямым действием мелатонина на гипоталамус, где идет блокада освобождения люлиберина, и на переднюю долю гипофиза, где он уменьшает действие люлиберина на освобождение лютропина;
2) гломерулотропин (стимулирует секрецию альдостерона корковым слоем надпочечников).
Тимус (вилочковая железа) – парный дольчатый орган, расположенный в верхнем отделе переднего средостения. Тимус образует несколько гормонов: химозин, гомеостатический тимусный гормон, тимопоэтин I, II, тимусный гуморальный фактор. Они играют важную роль в развитии иммунологических защитных реакций организма, стимулируя образование антител. Тимус контролирует развитие и распределение лимфоцитов. Секреция гормонов тимуса регулируется передней долей гипофиза.
Вилочковая железа достигает максимального развития в детском возрасте. После полового созревания она начинает атрофироваться (железа стимулирует рост организма и тормозит развитие половой системы). Есть предположение, что тимус влияет- Hi обмен ионов Са и нуклеиновых кислот.
При увеличении вилочковой железы у детей возникает тимико-лимфатический статус. При этом состоянии, кроме увеличения тимуса, происходят разрастание лимфатической ткани, увеличение вилочковой железы является проявлением надпочечниковой недостаточности.
Паращитовидные железы – парный орган, они расположены на поверхности щитовидной железы. Гормон паращитовидной железы – паратгормон (паратирин). Паратгормон находится в клетках железы в виде прогормона, превращение прогормона в паратгормон происходит в комплексе Гольджи. Из паращитовидных желез гормон непосредственно поступает в кровь.
Паратгормон регулирует обмен Са в организме и поддерживает его постоянный уровень в крови. В норме содержания Са в крови составляет 2,25-2,75 ммоль/л (9-11 мг%). Костная ткань скелета – главное депо Са в организме. Имеется определенная зависимость между уровнем Са в крови и содержанием его в костной ткани. Паратгормон усиливает рассасывание кости, что приводит к увеличению освобождения ионов Са, регулирует процессы отложения и выхода солей Са в костях. Влияя на обмен Са, паратгормон параллельно воздействует на обмен фосфора: уменьшает обратное всасывание фосфатов в дистальных канальцах почек, что приводит к понижению их концентрации в крови.
Удаление паращитовидных желез приводит к вялости, рвоте, потере аппетита, к разрозненным сокращениям отдельных групп мышц, которые могут переходить в длительное тетаническое сокращение. Регуляция деятельности паращитовидных желез определяется уровнем Са в крови. Если в крови нарастает концентрация Са, это приводит к снижению функциональной активности паращитовидных желез. При уменьшении уровня Са повышается гормонооб-разовательная функция желез.
Гормоны щитовидной железы. Йодированные гормоны. Тиреокальцитонин. Нарушение функции щитовидной железы
Щитовидная железа расположена с обеих сторон трахеи ниже щитовидного хряща, имеет дольчатое строение. Структурной единицей является фолликул, заполненный коллоидом, где находится йодсодержащий белок – тиреоглобулин.
Гормоны щитовидной железы делятся на две группы:
1) йодированные – тироксин, трийодтиронин:
2) тиреокальцитонин (кальцитонин).
Иодированные гормоны образуются в фолликулах железистой ткани, его образование происходит в три 3 этапа:
1) образование коллоида, синтез тиреоглобулина;
2) йодирование коллоида, поступление йода в организм, всасывание в виде йодидов. Йодиды поглощаются щитовидной железой, окисляются в элементарный йод и включаются в состав тиреоглобулина, процесс стимулируется ферментом – тиреоидпероксиказой;
3) выделение в кровоток происходит после гидролиза тиреоглобулина под действием катепсина, при этом освобождаются активные гормоны – тироксин, трийодтиронин.
Основной активный гормон щитовидной железы – тироксин. соотношение тироксина и трийодтиронина составляет 4:1. Оба гормона находятся в крови в неактивном состоянии, они связаны с белками глобулиновой фракции и альбумином плазмы крови. Тироксин легче связывается с белками крови, поэтому быстрее проникает в клетку и имеет большую биологическую активность. Клетки печени захватывают гормоны, в печени гормоны образуют соединения с глюкуроновой кислотой, которые не обладают гормональной активностью и выводятся с желчью в ЖКТ. Этот процесс называется дезинтоксикацией, он предотвращает чрезмерное насыщение крови гормонами.
Роль йодированных гормонов:
1) влияние на функции ЦНС. Гипофункция ведет к резкому снижению двигательной возбудимости, ослаблению активных и оборонительных реакций;
2) влияние на высшую нервную деятельность. Включаются в процесс выработки условных рефлексов, дифференцировки процессов торможения;
3) влияние на рост и развитие. Стимулируют рост и развитие скелета, половых желез;
4) влияние на обмен веществ. Происходит воздействие на обмен белков, жиров, углеводов, минеральный обмен. Усиление энергетических процессов и увеличение окислительных процессов приводят к повышению потребления тканями глюкозы, что заметно снижает запасы жира и гликогена в печени,
5) влияние на вегетативную систему. Увеличивается число сердечных сокращений, дыхательных движений, повышается потоотделение;
6) влияние на свертывающую систему крови. Снижают способность крови к свертыванию (уменьшают образование факторов свертывания крови), повышают ее фибринолитическую активность (увеличивают синтез антикоагулянтов). Тироксин угнетает функциональные свойства тромбоцитов – адгезию и агрегацию
Регуляция образования йодсодержащих гормонов осуществляется:
1) тиреотропином передней доли гипофиза. Влияет на все стадии йодирования, связь между гормонами осуществляется по типу прямых и обратных связей;
2) йодом. Малые дозы стимулируют образование гормона за счет усиления секреции фолликулов, большие - тормозят;
3) вегетативной нервной системой: симпатическая – повышает активность продукции гормона, парасимпатическая – снижает;
4) гипоталамусом. Тиреолиберин гипоталамуса стимулирует тиреотропин гипофиза, который стимулирует продукцию гормонов, связь осуществляется по типу обратных связей;
5) ретикулярной формацией (возбуждение ее структур повышает выработку гормонов);
6) корой головного мозга. Декортикация активизирует функцию железы первоначально, значительно снижает с течением времени.
Тиреокальцитоцин образуется парафолликулярными клетками щитовидной железы, которые расположены вне железистых фолликул. Он принимает участие в регуляции кальциевого обмена, под его влиянием уровень Са снижается. Тиреокальцитоцин понижает содержание фосфатов в периферической крови.
Тиреокальцитоцин тормозит выделение ионов Са2+ из костной ткани и увеличивает его отложение в ней. Он блокирует функцию остеокластов, которые разрушают костную ткань, и запускают механизм активации остеобластов, участвующих в образовании костной ткани.
Уменьшение содержания Са2+ и фосфатов в крови обусловлено влиянием гормона на выделительную функцию почек, уменьшая канальцевую реабсорбцию этих ионов. Гормон стимулирует поглощение Са2+ митохондриями.
Регуляция секреции тиреокальцитонина: зависит от уровня Са2+ в крови: повышение его концентрации приводит к дегрануляции парафолликулов. Активная секреция в ответ на гиперкальциемию поддерживает концентрацию Са2+ на определенном физиологическом уровне.
Секреции тиреокальцитонина способствуют некоторые биологически активные вещества: гастрин, глюкагон, холецистокинин.
При возбуждении β -адренорецепторов повышается секреция гормона, и наоборот.
Нарушение функции щитовидной железы сопровождается повышением или понижением ее гормонообразующей функции.
Недостаточность выработки гормона (гипотиреоз), появляющаяся в детском возрасте, ведет к развитию кретинизма (задерживаются рост, половое развитие, развитие психики, наблюдается нарушение пропорций тела). Недостаточность выработки гормона ведет к развитию микседемы, которая характеризуется резким расстройством процессов возбуждения и торможения в ЦНС, психической заторможенностью, снижением интеллекта, вялостью, сонливостью, нарушением половых функций, угнетением всех видов обмена веществ.
При повышении активности щитовидной железы (гипертиреозе) возникает заболевание тиреотоксикоз. Характерные признаки: увеличение размеров щитовидной железы, числа сердечных сокращений, повышение обмена веществ, температуры тела, увеличение потребления пищи, пучеглазие. Наблюдаются повышенная возбудимость и раздражительность, изменяется соотношение тонуса отделов вегетативной нервной системы: преобладает возбуждение симпатического отдела. Отмечаются мышечное дрожание и мышечная слабость.
Недостаток в воде йода приводит к снижению функции щитовидной железы со значительным разрастанием ее ткани и образованием зоба. Разрастание ткани – компенсаторный механизм в ответ на снижение содержания йодированных гормонов в крови.
Гормоны поджелудочной железы. Нарушение функции поджелудочной железыПоджелудочная железа – железа со смешанной функцией. Морфологической единицей железы служат островки Лангерганса, преимущественно они расположены в хвосте железы. β -клетки островков вырабатывают инсулин, α -клетки – глюкагон, δ -клетки – соматостатин. В экстрактах ткани поджелудочной железы обнаружены гормоны ваготонин и центропнеин.
Инсулин регулирует углеводный обмен, снижает концентрацию сахара в крови, способствует превращению глюкозы в гликоген в печени и мышцах. Он повышает проницаемость клеточных мембран для глюкозы: попадая внутрь клетки, глюкоза усваивается. Инсулин задерживает распад белков и превращение их в глюкозу, стимулирует синтез белка из аминокислот и их активный транспорт в клетку, регулирует жировой обмен путем образования высших жирных кислот из продуктов углеводного обмена тормозит мобилизацию жира из жировой ткани.
В β -клетках инсулин образуется из своего предшественника проинсулина. Он переносится в клеточные аппарат Гольджи, где происходят начальные стадии превращения проинсулина в инсулин.
В основе регуляции инсулина лежит нормальное содержание глюкозы в крови: гипергликемия приводит к увеличению поступления инсулина в кровь, и наоборот.
Паравентрикулярные ядра гипоталамуса повышают активность при гипергликемии, возбуждение идет в продолговатый мозг, оттуда в ганглии поджелудочной железы и к β -клеткам, что усиливает образование инсулина и его секрецию. При гипогликемии ядра гипоталамуса снижают свою активность, и секреция инсулина уменьшается.
Гипергликемия непосредственно приводит в возбуждение рецепторный аппарат островков Лангерганса, что увеличивает секрецию инсулина. Глюкоза также непосредственно действует на β -клетки, что ведет к высвобождению инсулина.
Глюкагон повышает количество глюкозы, что также ведет к усилению продукции инсулина. Аналогично действует гормоны надпочечников.
Вегетативная нервная система регулирует выработку инсулина посредством блуждающего и симпатического нервов. Блуждающий нерв стимулирует выделение инсулина, а симпатический тормозит.
Количество инсулина в крови определяется активностью фермента инсулиназы, который разрушает гормон. Наибольшее количество фермента находится в печени и мышцах. При однократном протекании крови через печень разрушается до 50 % находящегося в крови инсулина.
Важную роль в регуляции секреции инсулина выполняет гормон соматостатин, который образуется в ядрах гипоталамуса и δ -клетках поджелудочной железы. Соматостатин тормозит секрецию инсулина. Активность инсулина выражается в лабораторных и клинических единицах.
Глюкагон принимает участие в регуляции углеводного обмена, по действию на обмен углеводов он является антагонистом инсулина. Глюкагон расщепляет гликоген в печени до глюкозы, концентрация глюкозы, в крови повышается. Глюкагон стимулиует расщепление жиров в жировой ткани.
Механизм действия глюкагона обусловлен его взаимодействием с особыми специфическими рецепторами, которые находятся на клеточной мембране. При связи глюкагона с ними увеличивается активность фермента аденилатциклазы и концентрации цАМФ, цАМФ способствует процессу гликогенолиза.
Регуляция секреции глюкагона. На образование глюкагона в α -клетках оказывает влияние уровень глюкозы в крови. При повышении глюкозы в крови происходит торможение секреции глюкагона, при понижении – увеличение. На образование глюкагона оказывает влияние и передняя доля гипофиза.
Гормон роста соматотропин повышает активность α -клеток. В противоположность этому гормон δ -клетки – соматостатин тормозит образование и секрецию глюкагона, так как он блокирует вхождение в α -клетки ионов Са, которые необходимы для образования и секреции глюкагона.
Физиологическое значение липокаина. Он способствует утилизации жиров за счет стимуляции образования липидов и окисления жирных кислот в печени, он предотвращает жировое перерождение печени.
Функции ваготонина – повышение тонуса блуждающих нервов, усиление их активности.
Функции центропнеина – возбуждение дыхательного центра, содействие расслаблению гладкой мускулатуры бронхов, повышение способности гемоглобина связывать кислород, улучшение транспорта кислорода.
Нарушение функции поджелудочной железы. Уменьшение секреции инсулина приводит к развитию сахарного диабета, основными симптомами которого являются гипергликемия, глюкозурия, полиурия (до 10 л в сутки), полифагия (усиленный аппетит), полидиспепсия (повышенная жажда). Увеличение сахара в крови у больных сахарным диабетом является результатом потери способности печени синтезировать гликоген из глюкозы, а клеток – утилизировать глюкозу. В мышцах также замедляется процесс образования и отложения гликогена. У больных сахарным диабетом нарушаются все виды обмена.
Гормоны надпочечников. Глюкокортикоиды
Надпочечники – парные железы, расположенные над верхними полюсами почек. Они имеют важное жизненное значение. Различают два типа гормонов: гормоны коркового слоя и гормоны мозгового слоя.
Гормоны коркового слоя длятся на три группы:
1) глюкокортикоиды (гидрокортизон, кортизон, кортикостерон);
2) минералокортикоиды (альдестерон, дезоксикортикостерон);
3) половые гормоны (андрогены, эстрогены, прогестерон).
Глюкокортикоиды синтезируются в пучковой зоне коры надпочечников. По химическому строению гормоны являются стероидами, образуются из холестерина, для синтеза необходима аскорбиновая кислота.
Физиологическое значение глюкокортикоидов.
Глюкокортикоиды влияют на обмен углеводов, белков и жиров, усиливают процесс образования глюкозы из белков, повышают отложение гликогена в печени, по своему действию являются антагонистами инсулина.
Глюкокортикоиды оказывают катаболическое влияние на белковый обмен, вызывают распад тканевого белка и задерживают включение аминокислот в белки.
Гормоны обладают противовоспалительным действием, что обусловлено снижением проницаемости стенок сосуда при низкой активности фермента гиалуронидазы. Уменьшение воспаления обусловлено торможением освобождения арахидоновой кислоты из фосфолипидов. Это ведет к ограничению синтеза простагландинов, которые стимулируют воспалительный процесс.
Глюкокортикоиды оказывают влияние на выработку защитных антител: гидрокортизон подавляет синтез антител, тормозит реакцию взаимодействия антитела с антигеном.
Глюкокортикоиды оказывают выраженное влияние на кроветворные органы: 1) увеличивают количество эритроцитов за счет стимуляции красного костного мозга; 2) приводят к обратному развитию вилочковой железы и лимфоидной ткани, что сопровождается уменьшением количества лимфоцитов.
Выделение из организма осуществляется двумя путями: 1) 75—90 % поступивших гормонов в кровь удаляется с мочой; 2) 10—25 % удаляется с калом и желчью.
Регуляция образования глюкокортикоидов.
Важную роль в образовании глюкокортикоидов играет кортикотропин передней доли гипофиза. Это влияние осуществляется по принципу прямых и обратных связей: кортикотропин повышает продукцию глюкокортикоидов, а избыточное их содержание в крови приводит к торможению кортикотропина в гипофизе.
В ядрах переднего отдела гипоталамуса синтезируется нейросекрет кортиколиберин, который стимулирует образование кортикотропина в передней доле гипофиза, а он, в свою очередь, стимулирует образование глюкокортикоида. Функциональное отношение «гипоталамус – передняя доля гипофиза – кора надпочечников» находится в единой гипоталамо-гипофизарно-надпочечниковой системе, которая играет ведущую роль в адаптационных реакциях организма.
Адреналин – гормон мозгового вещества надпочечников – усиливает образование глюкокортикоидов.
Гормоны надпочечников. Минералокортикоиды. Половые гормоныМинералокортикоиды
Минералокортикоиды образуются в клубочковой зоне коры надпочечников и принимают участие в регуляции минерального обмена. К ним относятся альдостерон и дезоксикортикостерон. Они усиливают обратное всасывание ионов Na в почечных канальцах и уменьшают обратное всасывание ионов К, что приводит к повышению ионов Na в крови и тканевой жидкости и увеличению в них осмотического давления. Это вызывает задержку воды в организме и повышение артериального давления.
Минералокортикоиды способствуют проявлению воспалительных реакций за счет повышения проницаемости капилляров и серозных оболочек. Они принимают участие в регуляции тонуса кровеносных сосудов. Альдостерон обладает способностью увеличивать тонус гладких мышц сосудистой стенки, что приводит к повышению величины кровяного давления. При недостатке альдостерона развивается гипотония.
Регуляция образования минералокортикоидов
Регуляция секрета и образования альдостерона осуществляется системой «ренин – ангиотензин». Ренин образуется в специальных клетках юкстагломерулярного аппарата афферентных артериол почки и выделяется в кровь и лимфу. Он катализирует превращение ангиотензиногена в ангиотензин I, который переходит под действием специального фермента в ангиотензин II. Ангиотензин II стимулирует образование альдостерона. Синтез минералокортикоидов контролируется концентрацией ионов Na и К в крови. Повышение ионов Na приводит к торможению секреции альдостерона, что приводит к выделению Na+ с мочой. Снижение образования минералокортикоидов происходит при недостаточном содержании К+. На синтез минералокортикоидов влияет количество тканевой жидкости и плазмы крови. Увеличение их объема приводит к торможению секреции альдостеронов, что обусловлено усиленным выделением Na+ и связанной с ним воды. Гормон эпифиза гломерулотропин усиливает синтез альдостерона.
Половые стероиды надпочечников
Половые гормоны (андрогены, эстрогены, прогестерон) образуются в сетчатой зоне коры надпочечников. Они имеют большое значение в развитии половых органов в детском возрасте, когда внутрисекреторная функция половых желез незначительна. Оказывают анаболическое действие на белковый обмен: повышают синтез белка за счет увеличенного включения в его молекулу аминокислот.
При гипофункции коры надпочечников возникает заболевание – бронзовая болезнь, или аддисонова болезнь. Признаками этого заболевания являются: бронзовая окраска кожи, особенно на руках шее, лице, повышенная утомляемость, потеря аппетита, появление тошноты и рвоты. Больной становится чувствителен к боли и холоду, более восприимчив к инфекции.
При гиперфункции коры надпочечников (причиной которой чаще всего является опухоль) происходит увеличение образования гормонов, отмечается преобладание синтеза половых гормонов над другими, поэтому у больных начинают резко изменяться вторичные половые признаки. У женщин наблюдается проявление вторичных мужских половых признаков, у мужчин – женских.
Гормоны мозгового слоя надпочечников
Мозговой слой надпочечников вырабатывает гормоны, относящиеся к катехоламинам. Основной гормон – адреналин, вторым по значимости является предшественник адреналина – норадреналин. Хромаффиновые клетки мозгового слоя надпочечников находятся и в других частях организма (на аорте, у места разделения сонных артерий и т.д.), они образуют адреналовую систему организма. Мозговой слой надпочечников – видоизмененный симпатический ганглий.
Значение адреналина и норадреналина.
Адреналин выполняет функцию гормона, он поступает в кровь постоянно, при различных состояниях организма (кровопотере, стрессе, мышечной деятельности) происходит увеличение его образования и выделения в кровь.
Возбуждение симпатической нервной системы приводит к повышению поступления в кровь адреналина и норадреналина, они удлиняют эффекты нервных импульсов в симпатической нервной системе. Адреналин влияет на углеродный обмен, ускоряет расщепление гликогена в печени и мышцах, расслабляет бронхиальные мышцы, угнетает моторику ЖКТ и повышает тонус его сфинктеров, повышает возбудимость и сократимость сердечной мышцы. Он повышает тонус кровеносных сосудов, действует сосудорасширяюще на сосуды сердца, легких и головного мозга. Адреналин усиливает работоспособность скелетных мышц.
Повышение активности адреналовой системы происходит под действием различных раздражителей, которые вызывают изменение внутренней среды организма. Адреналин блокирует эти изменения.
Адреналин – гормон короткого периода действия, он быстро разрушается моноаминоксидазой. Это находится в полном соответствии с тонкой и точной центральной регуляцией секреции этого гормона для развития приспособительных и защитных реакций организма.
Норадреналин выполняет функцию медиатора, он входит в состав симпатина – медиатора симпатической нервной системы, он принимает участие в передаче возбуждения в нейронах ЦНС.
Секреторная активность мозгового слоя надпочечников регулируется гипоталамусом, в задней группе его ядер расположены высшие вегетативные центры симпатического отдела. Их активация ведет к увеличению выброса адреналина в кровь. Выделение адреналина может происходить рефлекторно при переохлаждении, мышечной работе и т. д. При гипогликемии рефлекторно повышается выделение адреналина в кровь.
Половые гормоны. Менструальный цикл
Половые железы (семенники у мужчин, яичники у женщин) относятся к железам со смешанной функцией, внутрисекреторная функция проявляется в образовании и секреции половых гормонов, которые непосредственно поступают в кровь.
Мужские половые гормоны – андрогены образуются в интерстициальных клетках семенников. Различают два вида андрогенов – тестостерон и андростерон.
Андрогены стимулируют рост и развитие полового аппарата мужских половых признаков и появление половых рефлексов Они контролируют процесс созревания сперматозоидов, способствуют сохранению их двигательной активности, проявлению полового инстинкта и половых поведенческих реакций, увеличивают образование белка, особенно в мышцах, уменьшают содержание жира в организме. При недостаточном количестве андрогена в организме нарушаются процессы торможения в коре больших полушарий.
Женские половые гормоны эстрогены образуются в фолликулах яичника. Синтез эстрогенов осуществляется оболочкой фолликула, прогестерона – желтым телом яичника, которое развивается на месте лопнувшего фолликула.
Эстрогены стимулируют рост матки, влагалища, труб, вызывают разрастание эндометрия, способствуют развитию вторичных женских половых признаков, проявлению половых рефлексов, усиливают сократительную способность матки, повышают ее чувствительность к окситоцину, стимулируют рост и развитие молочных желез.
Прогестерон обеспечивает процесс нормального протекания беременности, способствует разрастанию слизистой эндометрия, имплантации оплодотворенной яйцеклетки в эндометрий, тормозит сократительную способность матки, уменьшает ее чувствительность к окситоцину, тормозит созревание и овуляцию фолликула за счет угнетения образования лютропина гипофиза.
Образование половых гормонов находится под влиянием гонадотропных гормонов гипофиза и пролактина. У мужчин гонадотропный гормон способствует созреванию сперматозоидов, у женщин – росту и развитию фолликула. Лютропин определяет выработку женских и мужских половых гормонов, овуляцию и образование желтого тела. Пролактин стимулирует выработку прогестерона.
Мелатонин тормозит деятельность половых желез.
Нервная система принимает участие в регуляции активности половых желез за счет образования в гипофизе гонадотропных гормонов. ЦНС регулирует протекание полового акта. При изменении функционального состояния ЦНС могут произойти нарушение полового цикла и даже его прекращение.
Менструальный цикл включает четыре периода:
1. Предовуляционный (с пятого по четырнадцатый день). Изменения обусловлены действием фоллитропина, в яичниках происходит усиленное образование эстрогенов, они стимулируют рост матки, разрастание слизистой оболочки и ее желез, ускоряется созревание фолликула, поверхность его разрывается, и из него выходит яйцеклетка – происходит овуляция.
2. Овуляционный (с пятнадцатого по двадцатьвосьмой день). Начинается с выхода яйцеклетки в трубу, сокращение гладкой мускулатуры трубы способствует продвижению ее к матке, здесь может произойти оплодотворение. Оплодотворенное яйцо, попадая в матку, прикрепляется к ее слизистой и наступает беременность. Если оплодотворение не произошло, наступает послеовуляционный период. На месте фолликула развивается желтое тело, оно вырабатывает прогестерон.
3. Послеовуляционный период. Неоплодотворенное яйцо, достигая матки, погибает. Прогестерон уменьшает образование фоллитропина и снижает продукцию эстрогенов. Изменения, возникшие в половых органах женщины исчезают. Параллельно уменьшается образование лютропина, что ведет к атрофии желтого тела. За счет уменьшения эстрогенов матка сокращается, происходит отторжение слизистой оболочки. В дальнейшем происходит ее регенерация.
4. Период покоя и послеовуляционный период продолжаются с первого по пятый день полового цикла.
Гормоны плаценты
Понятие о тканевых гормонах и антигормонах
Плацента – уникальное образование, которое связывает материнский организм с плодом. Она выполняет многочисленные функции, в том числе метаболическую и гормональную. Она синтезирует гормоны двух групп:
1) белковые – хорионический гонадотропин (ХГ), плацентарный лактогенный гормон (ПЛГ), релаксин;
2) стероидные – прогестерон, эстрогены.
ХГ образуется в больших количествах через 7-12 недель беременности, в дальнейшем образование гормона снижается в несколько раз, его секреция не контролируется гипофизом и гипоталамусом, его транспорт к плоду ограничен. Функции ХГ – увеличение роста фолликулов, образование желтого тела, стимулирование выработки прогестерона. Защитная функция заключается в способности предотвращать отторжение зародыша организмом матери. ХГ обладает антиаллергическим действием.
ПЛГ начинает секретироваться с шестой недели беременности и прогрессивно увеличивается. Он влияет на молочные железы подобно пролактину гипофиза, на белковый обмен (повышает синтез белка в организме матери). Одновременно возрастает содержание свободных жирных кислот, повышается устойчивость к действию инсулина.
Релаксин секретируется на поздних стадиях развития беременности, расслабляет связки лонного сочленения, снижает тонус матки и ее сократимость.
Прогестерон синтезируется желтым телом до четвертой – шестой недели беременности, в дальнейшем в этот процесс включается плацента, процесс секреции прогрессивно нарастает. Прогестерон вызывает расслабление матки, снижение ее сократимости и чувствительность к эстрогенам и окситоцину, накопление воды и электролитов, особенно внутриклеточного натрия. Эстрогены и прогестерон способствуют росту, растяжению матки, развитию молочных желез и лактации.
Тканевые гормоны – биологически активные вещества, действующие в месте своего образования, не поступающие в кровь. Простагландины образуются в микросомах всех тканей, принимают участие в регуляции секреции пищеварительных соков, изменении тонуса гладких мышц сосудов и бронхов, процесса агрегации тромбоцитов. К тканевым гормонам, регулирующим местное кровообращение, относят гистамин (расширяет сосуды) и серотонин (обладает прессорным действием). Тканевыми гормонами считают медиаторы нервной системы – норадреналин и ацетилхолин.
Антигормоны – вещества, обладающие противогормональ-ной активностью. Их образование происходит при длительном введении гормона в организм извне. Каждый антигормон обладает выраженной видовой специфичностью и блокирует действие того вида гормона, на который выработался. Он появляется в крови спустя 1-3 месяца после введения гормона и исчезает через 3-9 месяцев после последней инъекции гормона.
Факторы, регулирующие рост человека
Эндокринная система играет огромную роль в регуляции роста и развития, будучи одним из главных факторов, при участии которых заключенная в генах информация реализуется во взрослый организм с такой скоростью и в такой форме, как это допускает данная конкретная среда.
На 9-й нед. внутриутробного развития, считая с первого дня последний менструации (или на 7-й нед., считая с момента оплодотворения), под воздействием генов Y-хромосомы ранее недифференцированная гонада начинает превращаться в яичко. Пока не ясно, какова роль гормонов в этом процессе.
Наиболее важным гормоном, воздействующим на процесс роста от момента рождения до подросткового периода, является соматотропин, или гормон роста. Он представляет собой полипептид, выделяемый гипофизом и обладающий большей степенью видовой (точнее, надвидовой) специфичности, чем остальные гормоны гипофиза. Стимуляцию роста у человека вызывают только гормоны человека или обезьяны.
С наступлением подросткового периода начинается новая фаза роста, во время которой действие гормонов половых желез и надпочечников в сочетании с гормоном роста вызывает пубертатный скачок роста. По-видимому, полная реализация скачка роста зависит от присутствия гормонов того и другого типа: у мальчиков с недостаточностью гормона роста максимальная скорость роста во время пубертатного периода достигает половины нормальной величины.
Известно множество факторов, оказывающих влияние на скорость развития. Некоторые из них носят наследственный характер и с раннего возраста способствуют ускорению или замедлению физиологического созревания. Другие (например, недостаточное питание, время года, тяжелый психологический стресс) относятся к категории факторов внешней среды и влияют на скорость роста лишь в период своего действия. И наконец, некоторые факторы, например, социально-экономическое положение, представляют собой результат сложного взаимодействия наследственности и среды.
Факторы роста - это белковые молекулы, регулирующие деление и выживание клеток. Факторы роста можно получать с помощью генной инженерии в лаборатории и использовать в терапии.Факторы роста связываются с рецепторами на поверхности клеток, активируя таким образом пролиферацию и / или дифференциацию клеток. Факторы роста достаточно универсальны и стимулируют клеточное деление в различных типах клеток, в то время как некоторые из них специфичны только для определенных типов клеток. Факторы роста - это белки, стимулирующие рост клеток. Факторы роста - это белки, которые функционируют как стимуляторы роста (митогены) и / или ингибиторы роста, стимулируют миграцию клеток, действуют как хемотоксичные агенты, ингибируют миграцию клеток, ингибируют инвазию раковых клеток, регулируют различные клеточные функции, участвуют в апоптозе и ангиогенезе и стимулируют выживаемость клеток, не влияя на рост и дифференциацию. Часто исследователи используют термин «факторы роста» как синоним цитокинов. В качестве примеров факторов роста можно привести: EGF, FGF, NGF, PDGF, VEGF, IGF, GMCSF, GCSF, TGF, эритропиетин, TPO, BMP, HGF, GDF, нейротрофины, MSF, SGF, GDF и более. Гемопоэтические факторы роста - это гормоно-подобные вещества, которые стимулируют костный мозг к производству клеток крови. Недостаток клеток крови является причиной большинства симптомов у людей, страдающих миелодиспластическим синдромом. Эритропоэтин - это фактор роста, который стимулирует продукцию красных кровяных телец. Интерлейкин-11 (IL-11) стимулирует продукцию тромбоцитов после хемотерапии. Современные исследования посвящены попыткам понять, какие факторы роста позволят лечить ряд болезней и как комбинировать факторы роста друг с другом и с другими методами лечения, такими как химиотерапия или гормоны.
Факторы роста являются биологически активными полипептидами, которые функционируют как гормоно-подобные регуляторные сигналы, контролирующие рост и дифференциацию чувствительных клеток. Различие между факторами роста и гормонами, как правило, неочевидно.
Подозревают также, что оплодотворению перезревшими гаметами (сперматозоид и яйцеклетка) может благоприятствовать ограничение периода половых сношений только предовуляторной или постовуляторной фазами менструального цикла, как это практикуется в методах так называемого естественного контроля рождаемости. При проведении экспериментов на животных были описаны различные аномалии (главным образом ряд аберраций хромосом), возникающие после оплодотворения перезрелых овоцитов. Аналогично недозрелые овоциты, по-видимому, создают недостаточную преграду против полиспермии, что приводит к повышенной частоте развития анеуплоидии. Несмотря на эти данные, для человеческой популяции нет четких доказательств того, что перезрелость или недозрелость гамет создает реальную опасность возникновения аномалий развития у потомка. Напротив, что кажется более вероятным (на основании некоторых косвенных наблюдений), это — существование зависимости между ненормальной степенью зрелости овоцита и нарушениями имплантации, ведущими в конечном итоге к выкидышу, возникновению внематочной беременности или предлежанию плаценты, а, возможно, также и к замедлению роста плода. Проблема старения гамет обсуждалась здесь довольно подробно не из-за ее высокой значимости в патогенезе нарушений роста плода, но главным образом потому, что она редко обсуждается в качестве возможной причины нарушений роста эмбриона и плода. Среди других факторов, регулирующих рост плода, можно упомянуть следующие 1. Генетическая характеристика плода. 2. Материнские факторы (анатомия матки и степень развития ее сосудистой сети, адаптация материнского организма к беременности и т. д.). 3. Питание матери (как количественные, так и качественные аспекты). 4. Гормоны плода (в частности, инсулин).
5. Почки плода (при недоразвитии почек обычно наблюдается замедление внутриутробного роста плода, нефрэктомия, выполненная у плода овцы, приводит к последующему замедлению внутриутробного роста). Более детальное рассмотрение этих факторов лежит за пределами возможностей данного раздела, поэтому читателя, интересующегося этими вопросами, мы отсылаем к списку рекомендуемой литературы, приведенному в конце раздела.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе