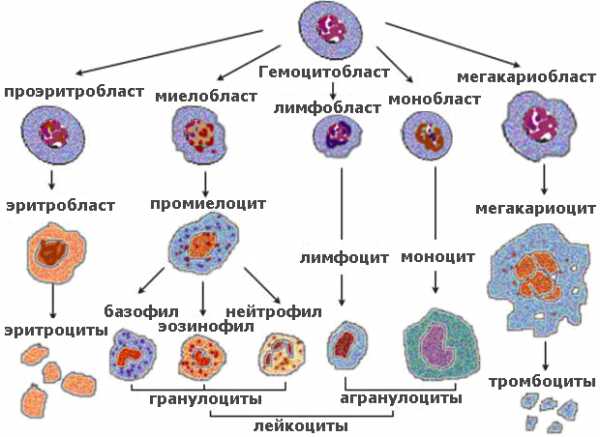
Полиморфизм генов системы гемостаза
Полиморфизм генов системы гемостаза и метаболизма фолатов, полное обследование, 12 показателей. Генетические полиморфизмы, ассоциированные с риском развития тромбофилии и нарушениями фолатного обмена.
F2: 20210 G>A
Ген F2 – протромбин (фактор II свертывания крови), кодирует предшественник тромбина.
Функция продукта гена: протромбин – предшественник тромбина, белка, стимулирующего образование тромба. Мутация F2: 20210 G>A наследуется по аутосомно-доминантному типу. Гетерозиготными носителями гена являются 2 - 3% представителей европейской расы. Гомозиготный вариант мутации является очень редким. При наличии мутации в гене протромбина повышена его экспрессия, вследствие чего обнаруживаются повышенные количества химически нормального протромбина. В сравнении с нормой уровень протромбина может быть превышен в 1,5 - 2 раза. При возникновении тромбозов мутация G20210A часто встречается в сочетании с мутацией Лейдена.
Проявление генотипа с аллелями «риска» (G/A, A/A): мутация является фактором риска невынашивания беременности, фетоплацентарной недостаточности, внутриутробной гибели плода в I триместре, гестоза, задержки развития плода, отслойки плаценты. Венозные тромбозы, повышение риска послеоперационной смерти. Ишемический инсульт, увеличение риска развития тромбоэмболии в 3 раза.
Возможные генотипы и клинические проявления: G/G: без особенностей. G/A: повышенная экспрессия гена. Уровень протромбина в плазме увеличен на 30 %, что приводит к увеличению образования тромбина и обусловливает высокий риск тромбоза. Ранние репродуктивные потери. A/A: повышенная экспрессия гена. Уровень протромбина в плазме увеличен на 70 %, что приводит к увеличению образования тромбина и обусловливает крайне высокий риск тромбоза. Ранние репродуктивные потери.
F5: 1691 G>A
Ген F5 – проакцелерин (фактор V свертывания крови), кодирует белковый кофактор при образовании тромбина и з протромбина.
Функция продукта гена: коагуляционный фактор свёртываемости крови. Фактор V вместе с другими факторами формирует комплекс протромбиназу, который превращает протромбин в тромбин. Наличие мутации G1691А (лейденский фактор, мутация Лейдена) делаетфактор V нечувствительным к ингибированию активированным протеином С (резистентность к активированному протеину С), являющимся одним из главных физиологических антикоагулянтов, ограничивающих тромбообразование. Частота встречаемости аллелей «риска» составляет 2 - 3%. Мутация наследуется по аутосомно-доминантному типу, то есть повышенная склонность к тромбозам проявляется уже в гетерозиготном состоянии гена (наличии измененного гена только на одной первой хромосоме, на другой первой хромосоме ген фактора V не изменен).
Проявление генотипа с аллелями «риска» (G/A, A/A): тромбоз вен нижних конечностей, ТЭЛА, тромбозы церебральных сосудов и ишемический инсульт, артериальные тромбозы в молодом возрасте. Привычное невынашивание беременности, поздние потери плода ( II -III триместр), отставание развития плода, фетоплацентарная недостаточность. У беременных пациенток, носительниц мутации Лейдена, повышен риск плацентарного тромбообразования. Тромбозы развиваются при наличии дополнительных факторов риска: приема гормональных контрацептивов (риск тромбозов повышается в 6 - 9 раз), наличия мутаций в гене MTHFR и гене протромбина, присутствия антифосфолипидных антител, повышения уровня гомоцистеина.
Возможные генотипы и клинические проявления: G/G: без особенностей. G/A и A/A: резистентность к активированному протеину C, который в норме расщепляет активированный фактор V и тем самым препятствует неуправляемому расширению процесса свертывания крови (APC-резистентность). Для гомозигот риск венозных тромбозов возрастает в 50-100 раз.
MTHFR: 677 С>T
Ген MTHFR (метилентетрагидрофолатредуктаза).
Функция продукта гена: восстанавливает 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата (катализатор реакции образования 5-метилтетрагидрофолата, необходимого для превращения гомоцистеина в метионин). Исследуемый полиморфизм MTHR обозначается как мутация C677T. Наличие мутации сопровождается повышением уровня гомоцистеина в крови. Частота встречаемости аллелей «риска» C/T и T/T составляет 30 - 40%.
Проявление генотипа с аллелями «риска»: снижение функциональной активности фермента, 3-х кратное повышение риска кардиоваскулярных заболеваний в молодом возрасте, тромбоэмболии. Невынашивание беременности, поздний гестоз, преэклампсия, отслойка плаценты. Антенатальная гибель плода, задержка и дефекты внутриутробного развития плода. Риск развития рака молочной железы, усиление побочных эффектов химиотерапии.
Возможные генотипы и клинические проявления: С/С: без особенностей. С/T: снижение функциональной активности фермента до 65 % от среднего значения. Повышение уровня гомоцистеина плазмы. T/T: отмечается термолабильность фермента и снижение его функциональной активности до 35% от среднего значения. Выраженное повышение уровня гомоцистеина плазмы (в большей степени, чем у гетерозигот). Кроме того, у лиц, гомозиготных по данной мутации, отмечается нарушенное распределение фолатов в эритроцитах, выражающееся в накоплении формильных полиглютаматов тетраглютамата и метилированных дериватов тетрагидрофолата.
PAI-1: 675 5G>4G
Ген PAI1 – серпин (антагонист тканевого активатора плазминогена).
Функция продукта гена: основная функция – ограничение фибринолитической активности в месте расположения гемостатической пробки путем ингибирования тканевого активатора плазминогена. Нарушения системы фибринолиза в большинстве случаев обусловлено полиморфизмами гена PAI-1 (675 5G>4G) и фактора свертывания крови XIII. Частота вариантов 5G/4G и 4G/4G составляет 5 - 8%.
Проявление генотипа с аллелями «риска»: повышение уровня PAI-1 в крови приводит к снижение фибринолитической активности крови, как следствие, - к повышению риска тромбозов. Известно, что ингибирование фибринолиза часто приводит к нарушению процесса имплантации плода и может явиться одной из причин раннего прерывания беременности. Снижение вероятности имплантации эмбриона при ЭКО. Привычное невынашивание беременности, увеличение риска тяжёлого гестоза (в 2 - 4 раза). Гипоксия, задержка развития и внутриутробная смерть плода. Повышение риска коронарных нарушений.
Возможные генотипы и клинические проявления: 5G/5G: без особенностей. 5G/4G: незначительное повышение уровня PAI-1 в крови, снижение фибринолитической активности крови. 4G/4G: в крови людей, имеющих вариант 4G/4G, концентрация PAI-1 значительно выше, чем у людей с вариантами 5G/5G и 5G/4G. Оказалось также, что вариант 4G/4G предрасполагает не только к повышению риска тормбозов, но и к ожирению, повышению уровня холестерина. Повышение риска тромбоза при дефиците протеина S.
FGB: -455 G>A
Ген FGB – фибриноген (фактор I свертывания крови).
Функция продукта гена: под влиянием фермента тромбина из фибриногена образуется нерастворимый белок фибрин на заключительном этапе свертывания крови. Исследуемый полиморфизм обозначается FGB: -455 G>A. Частота аллелей «риска» G/A и A/A - 5 -10%.
Возможные генотипы и клинические проявления: G/G: без особенностей. G/A и A/A: мутация сопровождается повышенной экспрессией гена, что приводит к повышению уровня фибриногена в крови на 10 - 30 % и увеличивает вероятность образования тромбов, развития кардиоваскулярных заболеваний . Повышенный в 2,6 раза риск инсульта с многоочаговостью поражений. Привычное невынашивание беременности, фетоплацентарная недостаточность, гипоксия плода.
F7: 10976 G>A
Ген F7 – проконвертин, или конвертин (коагуляционный фактор VII свертывания крови). В активном состоянии фактор VII взаимодействует с фактором III, что приводит к активации факторов IX и X системы свертывания крови, то есть коагуляционный фактор VII участвует в образовании кровяного сгустка. Вариант G10976A приводит к понижению экспрессии гена фактора VII и является защитным фактором в развитии тромбозов и инфаркта миокарда (2-х кратное снижение риска инфаркта миокарда). Частота вариантов гена (аллелей) G/A и A/A в европейской популяции составляет 10 -20%.
Проявление генотипа с аллелями «риска»: у новорожденных гморрагический диатез, кровотечение из пупочной ранки, слизистой оболочки носа.
Возможные генотипы и клинические проявления: G/G: без особенностей. G/A: снижение экспрессии гена фактора VII в крови на 30 %, снижение риска инфаркта миокарда, утяжеление течения гемофилии. A/A: снижение экспрессии гена фактора VII в крови на 5 %, снижение риска инфаркта миокарда, утяжеление течения гемофилии.
FXIII: G>T (Val34Leu)
Ген F13A1 – фибриназа (фактор XIII свертывания крови).
Функция продукта гена: участвует в образовании нерастворимого фибрина, представляющего собой основу кровяного сгустка. Стабилизация фибринового сгустка заключается как в повышении его механической прочности, так и в защите от лизиса. Частота (мутантных) аллелей G/T, T/T — 12- 20%.
Возможные генотипы и клинические проявления: G/G: без особенностей. G/T и T/T: снижение уровня XIII фактора в плазме, нарушение структуры и свойств фибринового сгустка, что может быть причиной отсроченных кровотечений. Повышенный риск на фоне антикоагулянтной терапии. Геморрагический синдром, гемартрозы. Уменьшение риска венозного тромбоза.
ITGA2: 807 С>T
Ген ITGA2 – α–интегрин (тромбоцитарный рецептор к коллагену).
Функция продукта гена: обеспечивает взаимодействие тромбоцитов с поврежденной стенкой сосудов, что является необходимым условием включения последующих звеньев свертывающей системы крови.Частота аллелей С/Т и Т/Т составляет 8 - 15%.
Возможные генотипы и клинические проявления: С/С: без особенностей. C/T и T/T: изменение первичной структуры субъединицы вызывает изменение свойств рецептора, что приводит к увеличению скорости адгезии тромбоцитов. Повышенный риск инфаркта миокарда (в 2,8 раза), ишемического инсульта. Повышенный риск послеоперационных тромбозов, постангиоопластические тромбозы. Развитие тромбоэмболических заболеваний.
ITGB3: (GpIIIa) 1565 T>C
Ген ITGB3 – интегрин (GpIIIa) (тромбоцитарный рецептор фибриногена, или тромбоцитарный гликопротеин IIIa).
Функция продукта гена: участвует в агрегации тромбоцитов, в большей степени отвечая за адгезию тромбоцитов к субэндотелиальным структурам. Обеспечивает взаимодействие тромбоцита с фибриногеном плазмы крови, что приводит к быстрой агрегации тромбоцитов и, таким образом, к последующему купированию поврежденной поверхности эпителия. Изменение свойств рецептора вследствие мутации Т1565С приводит к гиперагрегации тромбоцитов.
Возможные генотипы и клинические проявления: T/T: без особенностей. T/C и C/C: повышение сродства к фибриногену, повышенная адгезия клеток, более интенсивная ретракция фибринового сгустка. Посттрансфузионная тромбоцитопения. Тромбоэмболия. Увеличен риск развития сердечно-сосудистых заболеваний. Повышенный риск потери плода на ранних сроках.
MTR: 2756 A>G
Ген MTR (В12-зависимая метионин-синтаза), кодирует аминокислотную последовательность фермента метионинсинтазы - одного из ключевых ферментов обмена метионина. Фермент катализирует образование метионина из гомоцистеина путём его реметилированияю (обратное превращение гомоцистеина в метионин). Частота аллелей A/G, G/G составляет 20 - 30%.
Возможные генотипы и клинические проявления: A/A: без особенностей. A/G и G/G: отмечается снижение функциональной активности фермента, рост уровня гомоцистеина в крови, гипергомоцистеинемия. Повышение риска развития синдрома Дауна (рождение ребёнка с хромосомным синдромом при нормальном кариотипе родителей). Нарушение развития плода: незаращение нервной трубки, изолированные расщелины губы и нёба. Снижение гомоцистеина в плазме в ответ на повышение фолатов в пище.
MTRR: 66A>G
Ген MTRR (метионин-синтаза-редуктаза). Фермент, необходимый для поддержания активности метионин-синтазы путем восстановительного метилирования. При наличии мутации снижается функциональная активность фермента. Отмечается рост уровня гомоцистеина в крови. Частота аллелей A/G, G/G достигает 40 - 50%.
Возможные генотипы и клинические проявления: A/A: без особенностей. A/G и G/G: снижение функциональной активности фермента, гомоцистеинемия, особенно в сочетании с полиморфизмом гена MTR: 2756A>G. Дефекты развития нервной трубки. Усиливает патологический эффект, ассоциированный с полиморфизмами генов MTHFR и MTR. Исследование полиморфизма 66A>G имеет прогностическое значение при оценке риска сердечно-сосудистых заболеваний.
MTHFR: 1298 A>C
Ген MTHFR (метилентетрагидрофолатредуктаза).
Функция продукта гена: восстанавливает 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата (катализатор реакции образования 5-метилтетрагидрофолата, необходимого для превращения гомоцистеина в метионин). Исследуемый полиморфизм MTHR обозначается как мутация A1298C. Снижение функциональной активности фермента. Риск развития тромбозов. Невынашивание беременности, поздний гестоз. При генотипе C/C — повышенный риск эмбриональных опухолей.
Возможные генотипы и клинические проявления: A/A: без особенностей. A/C: комбинация гетерозиготности аллелей 677T и 1298C сопровождается не только снижением активности фермента, но и повышением концентрации гомоцистеина в плазме и снижением уровня фолатов. C/C: снижение активности MTHFR примерно до 60 % от нормы. При беременности может вызывать снижение фолатов в плазме.
Для экономии времени оформите заказ на анализ в Интернет-магазине! Оплачивая заказ онлайн, Вы получаете скидку 10% на весь оформленный заказ!
У Вас есть вопросы? Напишите нам или позвоните +7 (495) 514-00-11. По анализам Вы можете задать вопрос на нашем форуме и обратиться на консультацию к специалисту.
Исследование крови на наследственные дефекты гемостаза (мутации гемостаза): полиморфизм генов системы гемостаза
| Исследования последних лет показали, что у пациенток с привычным невынашиванием беременности часто обнаруживают один или несколько генетических факторов тромбофилии. Тромбофилия - склонность к развитию тромбозов. Может быть наследственная и ненаследственная. |
* также встречаются названия: мутации системы гемостаза, наследственные тромбофилии, лейденская мутация, мутация PAI-I, мутация протромбина, мутация МТГФР, мутации свертывания крови, генетические тромбофилии
Исследования последних лет показали, что у пациенток с привычным невынашиванием беременности часто обнаруживают один или несколько генетических факторов тромбофилии. Тромбофилия - склонность к развитию тромбозов. Может быть наследственная и ненаследственная. Наличие тромбофилии сопряжено с повышенным риском развития осложнений беременности (привычное невынашивание, плацентарная недостаточность, задержка роста плода, поздний токсикоз (гестоз)).
В нашей лаборатории исследование на полиморфизм генов системы гемостаза имеет два варианта:
Базовый блок состоит из 4 показателей
Полиморфизм генов системы гемостаза и метаболизма фолатов, полное обследование, 12 показателей. Генетические полиморфизмы, ассоциированные с риском развития тромбофилии и нарушениями фолатного обмена.
- Ген протромбина (F2): 20210 G>A
- Лейденская мутация (F5): 1691 G>A
- Ген ингибитора активатора плазминогена (PAI-1): 675 5G>4G
- Ген фибриногена (FGB): -455 G>A
- Ген VII фактора (F7): 10976 G>A
- Ген фактора 13 (FХIII): G>T
- Ген интегрина альфа-2 (ITGA2): 807 С>T
- Ген тромбоцитарного гликопротеина Gp-IIIa (GPIIb/IIIa) ITGB3: 1565 T>C
- Ген MTR: 2756 A>G
- Ген MTRR: 66A>G
- Ген метилентетрагидрофолатредуктазы MTHFR: 677 С>T
- MTHFR: 1298 A>C
Какой анализ сдавать - 4 или 12 показателей?
Варианты генов системы гемостаза делятся на более частые и редкие. Традиционно считается, что более частые варианты генов, предрасполагающие к развитию тромбозов - это соответствующие полиморфизмы генов MTHFR (метилентетрагидрофолатредуктазы), протромбина, PAI-I, фактора V (лейденская мутация), входящие в блок «Полиморфизмы генов системы гемостаза, 4 фактора». Это обследование выявляет достаточно большой процент проблем. Но иногда за рамками этого стандартного обследования остаются скрытые факторы, которые могут осложнять течение беременности, прием контрацептивов, хирургические вмешательства, поэтому для получения большей информации о потенциальных рисках желательно сдавать анализ «Полиморфизмы генов системы гемостаза, 12 факторов».
Особенности молекулярно-генетических анализов
- Не требуют подготовки
- Сдаются один раз в жизни
Смотрите также:
Теги: гемостаз
Назад в разделПолиморфизм генов гемостаза 4 фактора - лейденская мутация (мутация фактора V), мутация гена протромбина, мутация MTHFR, мутация PAI-I
Артикул 00325
Блок состоит из 4 показателей:
| ген протромбина (II фактор, G20210A) | лейденская мутация (ген фактора V, G1691A) |
| ген МТГФР (MTHFR, C677T) | ген активатора плазминогена (PAI-I, 675 5G/4G) |
Какой анализ сдавать - 4 или 12 факторов?
Варианты генов системы гемостаза делятся на более частые и редкие. Традиционно считается, что более частые варианты генов, предрасполагающие к развитию тромбозов - это соответствующие полиморфизмы генов MTHFR (метилентетрагидрофолатредуктазы), протромбина, PAI-I, фактора V (лейденская мутация), входящие в блок «Полиморфизмы генов системы гемостаза, 4 фактора». Это обследование выявляет достаточно большой процент проблем. Но иногда за рамками этого стандартного обследования остаются скрытые факторы, которые могут осложнять течение беременности, прием контрацептивов, хирургические вмешательства, поэтому для получения большей информации о потенциальных рисках желательно сдавать анализ «Полиморфизмы генов системы гемостаза, 12 факторов».
Если Вы ни разу не сдавали анализ «Полиморфизмы генов системы гемостаза» - сдайте полный блок из 12 показателей!
Показания к сдаче анализа:
- В прошлом были осложнения беременности, невынашивание беременности, остановки развития плода, гестозы, неудачные попытки ЭКО.
- У ваших родственников были заболевания сердечно-сосудистой системы.
- Вы планируете контрацепцию (важно провести всестороннее обследование - гормоны, гемостаз, биохимические показатели).
- Ваш образ жизни связан с риском получения травм или, напротив, Вы ведете сидячий образ жизни
- Вы готовитесь к плановому оперативному лечению (особенно «большие» операции).
- Вы хотите знать о рисках развития той или иной патологии. Это знание реально поможет спланировать свою жизнь так, чтобы предотвратить заболевания, снижающие качество жизни.
Особенности молекулярно-генетических анализов
Ø Не требуют подготовки
Ø Сдаются один раз в жизни
Как сдаётся анализ?
Сдать анализ можно 7 дней в неделю в часы работы Центра в любой из наших клиник.
Если Вы живёте в другом городе
Вы можете отправить нам материал экспресс-почтой и оплатить по безналичному расчету.
- Маркеры генов сперматогенеза (AZF-фактор) - делеции Y хромосомы
- Генетические маркеры синдрома поликистозных яичников (СПКЯ) - гены: рецептора андрогенов, инсулина, рецептора активатора пероксисом, цитохрома P450 (CYP11)
- Полиморфизм генов сосудистого тонуса. Предрасположенность к гипертоническим состояниям, нарушениям плацентарной функции, преэклампсии, инфаркту миокарда. Микроциркуляция, сосудистый тонус: (AGT), (ATGR2), (ATGR1), (ADD), (ACE), (CYP11B2)
- Полиморфизм генов цитокинов (цитокиновый профиль, иммунная конституция человека) (IL1Ra, IL1β +3953, IL4, TNF-α)
- Генетические маркеры адрено-генитального синдрома (мутации 21-гидроксилазы (CYP-21)
Теги: Полиморфизм генов гемостаза лейденская мутация гомоцистен гипертензия гипертония сердечно-сосудистые заболевания тромбоз инфаркт инсульт
Синонимы: Мозаичность генов свертывания
Для экономии времени оформите заказ на анализ в Интернет-магазине! Оплачивая заказ онлайн, Вы получаете скидку 10% на весь оформленный заказ!
У Вас есть вопросы? Напишите нам или позвоните +7 (495) 514-00-11. По анализам Вы можете задать вопрос на нашем форуме и обратиться на консультацию к специалисту.
Свертываемость крови как признак наследственной патологии
Нарушения гемостаза имеют врожденный и приобретенный характер. Те, которые передались по наследству, являются генетическими. Такая патология приводит к усилению или уменьшению свертываемости крови, которая обычно наследуется как признак полиморфизма генов. Первыми эту проблему чаще всего замечают акушеры-гинекологи, когда во время родов возникают коагулопатии. Также проблемы с системой гемостаза провоцируют внутриутробную гибель плода, привычное невынашивание беременности, ее осложнения или бесплодие, которая может быть обусловлена аутоиммунными заболеваниями родителей. Поэтому на этапе планирования беременности необходимо пройти полное обследование, чтобы максимально устранить эти риски.
Полиморфизмы генов системы свертываемости крови
Врачи утверждают, что полиморфизмы генов системы свертываемости крови не всегда обуславливают патологию, но они отыгрывают значительную роль в ее развитии. Поэтому при их обнаружении во время обследования будущих родителей информируют о том, что существует риск, который измеряется отношением возможности. В западных странах обязательно во время беременности изучают мутации генов FV, F2, PAI-1, MTHFR.
Необходимо отметить, что свертывающая система крови – огромная совокупность всевозможных биохимических процессов, призванных поддерживать кровь в жидком состоянии, что обеспечивает нормальную ее вязкость и своевременную остановку кровотечений. Она содержит факторы, которые отвечают за свертываемость, кровоточивость и растворение тромбов. Нарушение такого гомеостаза за счет воздействия различных триггеров ведет за собой тяжелые осложнения, которые иногда очень тяжело остановить.
Например, больной гемофилией может погибнуть от незначительного пореза, если ему не оказать медицинскую помощь, при этом гемофилией страдает достаточно большое количество людей. Инфаркты, ишемические инсульты или другие сосудистые катастрофы также имеет огромную долю летальных исходов, при этом они могут наследоваться либо формироваться по причине генетических мутаций и полиморфизмов.
Полиморфизм гена АСЕ
Этот ген оказывает влияние, по своей сути кодирует работу системы АПФ, занимающейся регуляцией артериального давления и нормального водно-солевого метаболизма. При проведении обследования у генетика, расшифровка укажет на два варианта – наличие и отсутствие интрона гена. Если его нет, то на треть повышается риск развития следующих заболеваний:
- гипертоническая болезнь;
- сосудистые катастрофы – инфаркты, инсульты, тромбозы;
- ТЭЛА;
- нефропатия.
Высокая свертываемость обусловлена снижением количества воды в циркуляторном русле. Для исследования берут цельную кровь, анализ проводится методом ПЦР или рестрикционно. Лечение полиморфизма зависит от развившейся патологии.
Полиморфизм коагуляционного фактора F5 V
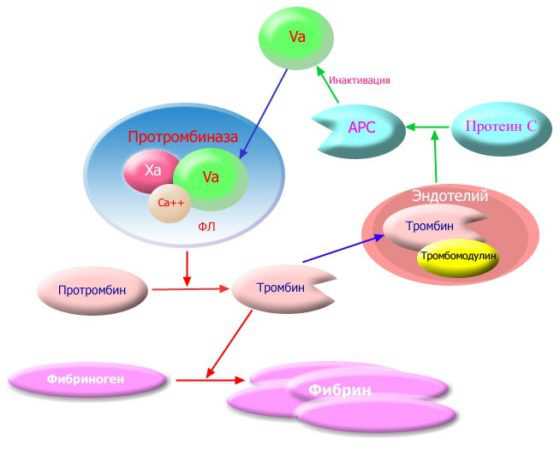
Это заболевание также называют мутацией Лейден или симптомом наследственных нарушений свертывания крови. Оно связано с образованием тромбина, отображает риск венозных тромбозов. Ее распространенность достигает 5%. 7-кратное увеличение риска наблюдается тогда, когда мутация определяется рецессивным геном, то есть речь идет о том, что возникла рецессивная мутация у гетерозигот. При гомозиготности он увеличивается в 100 раз.
Существуют триггерные факторы по риску полиморфизма:
- прием таблетированных контрацептивов;
- беременность;
- заместительная терапия гормонами;
- оперативные вмешательства;
- наличие центрального венозного доступа (подключичная вена) анамнезе;
- гиподинамия;
- путешествия на самолетах;
- инфекции или онкологические процессы.
Наличие такой мутации провоцирует нарушение свретываемости крови, а также приводит к таким осложнениям беременности, как ранний выкидыш, задержка внутриутробного развития, гестоз и другие. Повышение свертываемости провоцирует артериальные эмболии и сосудистые катастрофы.
Полиморфизм коагуляционного фактора F2 20210 G
Среди всего исследования, генетический анализ на второй фактор свертываемости или протромбин, является одним из самых важных. Он является предвестником тромбина. При его недостатке состояние системы свертываемости ухудшается, что проявляется появлением кровотечений. Если же экспрессия гена повышена, то вместо плохой свертываемости крови развивается гиперкоагуляция. Мутация наследуется аутосомно-доминантно. Носителями считается около 3% людей.
Клиническая картина включает бесплодие, гестозы, преэклампсия, привычное невышашивание беременности, а также задержка и нарушение внутриутробного развития со стороны репродуктивной системы. Со стороны коагулопатий чаще отмечается повышение риска тромбообразования и тромбозом, эмболий, что проявляется сосудистыми катастрофами. Лечение зависит от симптоматики.
Полиморфизм гена MTHFR C677T
Этот ген программирует последовательность фермента, участвующего в метаболических процессах фолиевой кислоты, которая играет большую роль в синтезе метионина и S-аденозилметионина. При дефиците фермента активируются онкогены и клеточные гены, накапливается гомоцистеин. При беременности повышается воздействие тератогенных факторов, а вероятность рождения здорового ребенка снижается. Если генотип материнского организма содержит такой полиморфизм, необходимо обязательно следовать всем рекомендациям генетика.
Полиморфизм имеет связь с заменой цитозина на тимин в 677 позиции, что влечет за собой замену остатка аланина на валин в позиции 223, которая отвечает за связывание фолиевой кислоты. У гомозигот теряется термолабильность, из-за чего происходит потеря активность в двух случаях из трех. У гетерозигот отмечаются сердечно-сосудистые патологии, нарушения внутриутробного развития, рак половых органов. У гомозиготных женщин в период беременности отмечается нарушения внутриутробного развития плода, проявляющиеся патологией нервной трубки. Усугубляется патология факторами внешней среды и вредными привычками.
Лечение патологических процессов симптоматическое.
Показания к проведению теста:
- гипергомоцистинемия;
- врожденные пороки нервной, сердечно-сосудистой и мочеполовой систем;
- хромосомный синдром при здоровых отце и матери;
- ишемическая болезнь сердца, гипертензия, в том числе наличие этих патологий у ближайших родственников;
- бесплодие, невынашивание беременности.
Исследуется цельная кровь, метод проведения анализа – ПЦР.
Полиморфизм коагуляционного фактора F7 ARG353GLN
Нормальные условия подразумевают то, что 7 и 3 факторы взаимодействуют, тем самым активируют работу фактора IX и X. То есть они все участвуют в формировании сгустка крови. Если развился полиморфизм F7 ARG353GLN, то снижается экспрессия гена, что снижает свертываемость.
Показанием к проведению данного анализа является изучение рисков сосудистых катастроф, а также тромбоэмболические процессы.
Симптоматика обуславливает гиперкоагуляцию, повышенный риск смерти по ее причине. Лечение такой мутации симптоматическое.
Полиморфизм тромбоцитарного рецептора фибриногена
Этот рецептор играет роль во взаимодействии тромбоцитов с фибриногеном, что обуславливает их повышенную агрегацию. Патология генетического кода подразумевает замену цитозана на тимин, из-за чего меняется аминокислота рецептора. Это приводит к изменению его свойств. Отмечается повышенная агрегация форменных элементов. Симптоматически встречаются:
- сосудистые катастрофы – инфаркты, инсульты;
- коронарный синдром;
- тромбозы.
Важно отметить, что люди, у которых была определена такая мутация, намного лучше реагируют на назначение антиагрегантной терапии аспирином или клопедогрелем.
Показания к проведению теста:
- тромбозы, тромбоэмболии у обследуемого или его ближайших родственников;
- сосудистые катастрофы;
- определение успешности атиагрегантной терапии.
Исследуется венозная кровь, определение происходит методом ПЦР.
Полиморфизм фибриногена 455G
Эта мутация приводит к повышению экспрессии гена, который отвечает за продукцию фибриногена. Показанием к анализу служат повышенные цифры фибриногена при изучении коагулограммы, сосудистые катастрофы анамнестически, артериальная гипертензия.
Клинически мутация проявляется тромбозами, кардиоваскулярными патологиями. Изменение уровня фибриногена развивается еще и на фоне приема лекарственных средств, алкоголизма, избыточной массы тела. Лечение симптоматическое, зависит от развившейся патологии.
Читать также Типы кровоточивостиПолиморфизм ARG353GNL 10976 GA коагуляционного фактора VII F7

Этот ген кодирует прокорвентин, являющийся синтезируюемым в печени белком, который активирует факторы 9, 10 и витамин К. При его недостатке может возникать заболевание гемофилия за счет воздействия фактора 7 на другие. Хромосома аллельных генов не содержит аденина, что провоцирует изменение всех свойств фермента за счет замены аргинина глутамином. Аллель А встречается у каждого десятого европейца. При полиморфизме развиваются тромбоэмболические процессы, а также тромбозы – инфаркты, инсульты и другие сосудистые катастрофы. Больные гемофилией, помимо дефицита факторов 8 и 9, могут содержать недостаточное количество фактора 7.
Проконвертин является 7м фактором свертывания крови. По своей сути это профермент, который зависит от витамина К. Его синтез происходит в печени, а главной функцией является активация десятого фактора.
Большинство случаев мутации отыгрывают фунцкию защиты от тромбоэмболии. Замена аргинина глутамином приводит к пониженной свертываемости, что также положительно влияет на развитие инфаркта миокарда даже при выраженном атеросклерозе коронарных сосудов.
Полиморфизм IIEMET66 AG мутация редуктазы метионинсинтетазы
Фермент, кодируемый этим геном, воздействует на большинство процессов, которые связаны с перемещением метильной группы. Другой функцией ученые называют обратную трансформацию гомоцистеина в метонин, кофактором здесь выступает коболамин – витамин В12.
Полиморфизм обуславливается заменой аминокислот, за счет чего снижается нормальная активность фермента. Это ведет к повышению риска развития патологий внутриутробного формирования, в том числе нервной системы за счет незарощения нервной трубки. Дефицит кобаламина значительно утяжеляет явления полиморфизма. Также усиливается гипергомоцистеинемия, если таковая была обусловлена дефектом 677СТ. Количество гомоцистеина увеличивается только при двойной мутации. Риск появления на свет ребенка с трисомией по 21й хромосоме (болезнь Дауна) повышается до 4% при данной мутации.
Полиморфизм 675 5G4G мутация ингибитора активатора плазминогена PAI1

Белок считается одной из основных составляющей комплекса плазминоген-плазмин. PAI1 блокирует активаторы плазминогена, что определяет подверженность сосудистым катастрофам. Гомозиготный вариант считается одним из их факторов риска. Также стоит подчеркнуть то, что этот ген подвержен стрессу больше, чем все другие известные гены человека.
Клинически при варианте 4G повышается экспрессия гена и уровень PAI1. Это ведет к снижению активности тромболитической системы, что отображается повышенной вязкостью крови, тромбозами. Риск их возникновения увеличивается почти вдвое. При этом, согласно многочисленным исследованиям, он растет у тех пациентов, у которых встречался тромбоз внутренних органов и воротной вены, однако корреляция не была установлена.
Такой ген также встречался у лиц, страдающих ожирением. При этом речь идет о центральном, а не периферическом отложении жира. В некоторой мере это обусловлено тем, что такая патология является коморбидной для кардиоваскулярных заболеваний, считается одним из триггерных факторов атеросклероза, инфарктов или инсультов. Поэтому полиморфизм, влияющий на уровень PAI1 дополнительно повышает риск относительно сердечно-сосудистых проблем.
Показания для проведения такого теста:
- тромбоз воротной вены, а также паренхиматозных или полых внутренних органов;
- наличие инфаркта миокарда в анамнезе или у ближайших родственников;
- острый коронарный синдром;
- ожирение;
- сахарный диабет типа 2.
Следует отметить, что лечение всех клинических проявлений генетических мутаций генов, кодирующих свертываемость крови, зависит от заболевания, которое развилось. Обычно назначается симптоматическая терапия, поскольку на мутацию повлиять никоим образом нельзя, лишь иногда ее можно предупредить, снизив влияние факторов окружающей среды, которые могут ее спровоцировать.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе