Описание костной клетки
Костные клетки описание
Костные клетки (остеоциты) лежат между костными пластинками, пронизывая их костными канальцами. Прочность костной ткани обусловлена тем, что коллагеновые волокна соседних костных пластинок располагаются под различными углами друг к другу и некоторая часть волокон переходит из одной костной пластинки в другую. Пучки коллагеновых волокон цементируются аморфным межклеточным веществом — остеомукоидом, сходным с хондромукоидом межклеточного вещества хрящевой ткани. Коэффициенты преломления аморфного и волокнистого межклеточного вещества кости почти равны, поэтому коллагеновые волокна костной ткани исследуют при помощи поляризационного микроскопа. Межклеточное вещество кости содержит кристаллы гидрооксиапатита в виде игольчатых либо пластинчатых частиц толщиной от 1,5 до 7,5 им и длиной до 150 нм, которые располагаются как в коллагеновых фибриллах, так и вокруг них.Развитие костной ткани (остеогенез) происходит из мезенхимы склеротома. В эмбриональном гистогенезе костная ткань может возникать непосредственно из мезенхимы либо развиваться на месте хряща.
Особенности регенерации нервов При повреждении центральных отделов нервной системы в очаге повреждения скопляется множество астроцитов, которые закрывают рану. Погибшие перикарионы нейронов и их отростки распадаются на отдельные фрагменты и фагоцитируются клетками микроглии, а также, по некоторым данным, астроцитами, в цитоплазме которых обнаруживаются лизосомы.
Отростки нервных клеток, не утратившие связи с перикарионом, только в месте повреждения незначительно дегенерируют, но уже спустя несколько дней начинают регенерировать. На их концах возникают…
Восстановление нервной ткани Регенерация нервной ткани у млекопитающих животных и человека затруднена, так как в процессе эмбрионального гистогенеза все нейробласты дифференцируются в нервные клетки. В связи с отсутствием в нервной ткани камбиальных элементов новые нервные клетки не образуются. Нервные клетки не могут увеличивать своей численности и в постэмбриональный период. Не наблюдается также регенерации перикарионов нервных клеток в связи с высокой дифференциацией нейронов. Регенерировать могут лишь отростки нервных клеток, не утратившие…
Описание костных клеток
Костные клетки (остеоциты) лежат между костными пластинками, пронизывая их костными канальцами. Прочность костной ткани обусловлена тем, что коллагеновые волокна соседних костных пластинок располагаются под различными углами друг к другу и некоторая часть волокон переходит из одной костной пластинки в другую. Пучки коллагеновых волокон цементируются аморфным межклеточным веществом — остеомукоидом, сходным с хондромукоидом межклеточного вещества хрящевой ткани. Коэффициенты преломления аморфного и волокнистого межклеточного вещества кости почти равны, поэтому коллагеновые волокна костной ткани исследуют при помощи поляризационного микроскопа. Межклеточное вещество кости содержит кристаллы гидрооксиапатита в виде игольчатых либо пластинчатых частиц толщиной от 1,5 до 7,5 им и длиной до 150 нм, которые располагаются как в коллагеновых фибриллах, так и вокруг них.Развитие костной ткани (остеогенез) происходит из мезенхимы склеротома. В эмбриональном гистогенезе костная ткань может возникать непосредственно из мезенхимы либо развиваться на месте хряща.
Особенности регенерации нервов При повреждении центральных отделов нервной системы в очаге повреждения скопляется множество астроцитов, которые закрывают рану. Погибшие перикарионы нейронов и их отростки распадаются на отдельные фрагменты и фагоцитируются клетками микроглии, а также, по некоторым данным, астроцитами, в цитоплазме которых обнаруживаются лизосомы.
Отростки нервных клеток, не утратившие связи с перикарионом, только в месте повреждения незначительно дегенерируют, но уже спустя несколько дней начинают регенерировать. На их концах возникают…
Восстановление нервной ткани Регенерация нервной ткани у млекопитающих животных и человека затруднена, так как в процессе эмбрионального гистогенеза все нейробласты дифференцируются в нервные клетки. В связи с отсутствием в нервной ткани камбиальных элементов новые нервные клетки не образуются. Нервные клетки не могут увеличивать своей численности и в постэмбриональный период. Не наблюдается также регенерации перикарионов нервных клеток в связи с высокой дифференциацией нейронов. Регенерировать могут лишь отростки нервных клеток, не утратившие…
Описание костной клетки
Костные клетки (остеоциты) лежат между костными пластинками, пронизывая их костными канальцами. Прочность костной ткани обусловлена тем, что коллагеновые волокна соседних костных пластинок располагаются под различными углами друг к другу и некоторая часть волокон переходит из одной костной пластинки в другую. Пучки коллагеновых волокон цементируются аморфным межклеточным веществом — остеомукоидом, сходным с хондромукоидом межклеточного вещества хрящевой ткани. Коэффициенты преломления аморфного и волокнистого межклеточного вещества кости почти равны, поэтому коллагеновые волокна костной ткани исследуют при помощи поляризационного микроскопа. Межклеточное вещество кости содержит кристаллы гидрооксиапатита в виде игольчатых либо пластинчатых частиц толщиной от 1,5 до 7,5 им и длиной до 150 нм, которые располагаются как в коллагеновых фибриллах, так и вокруг них.Развитие костной ткани (остеогенез) происходит из мезенхимы склеротома. В эмбриональном гистогенезе костная ткань может возникать непосредственно из мезенхимы либо развиваться на месте хряща.
Особенности регенерации нервов При повреждении центральных отделов нервной системы в очаге повреждения скопляется множество астроцитов, которые закрывают рану. Погибшие перикарионы нейронов и их отростки распадаются на отдельные фрагменты и фагоцитируются клетками микроглии, а также, по некоторым данным, астроцитами, в цитоплазме которых обнаруживаются лизосомы.
Отростки нервных клеток, не утратившие связи с перикарионом, только в месте повреждения незначительно дегенерируют, но уже спустя несколько дней начинают регенерировать. На их концах возникают…
Восстановление нервной ткани Регенерация нервной ткани у млекопитающих животных и человека затруднена, так как в процессе эмбрионального гистогенеза все нейробласты дифференцируются в нервные клетки. В связи с отсутствием в нервной ткани камбиальных элементов новые нервные клетки не образуются. Нервные клетки не могут увеличивать своей численности и в постэмбриональный период. Не наблюдается также регенерации перикарионов нервных клеток в связи с высокой дифференциацией нейронов. Регенерировать могут лишь отростки нервных клеток, не утратившие…
Костной ткани а также. Характеристика костной ткани
Костные ткани
Костные ткани (textus ossei) - это специализированный тип соединительной ткани с высокой минерализацией межклеточного органического вещества, содержащего около 70% неорганических соединений, главным образом фосфатов кальция. В костной ткани обнаружено более 30 микроэлементов (медь, стронций, цинк, барий, магний и др.), играющих важнейшую роль в метаболических процессах в организме.
Органическое вещество - матрикс костной ткани - представлено в основном белками коллагенового типа и липидами. По сравнению с хрящевой тканью в нем содержится относительно небольшое количество воды, хондроитинсерной кислоты, но много лимонной и других кислот, образующих комплексы с кальцием, импрегнирующим органическую матрицу кости.
Таким образом, твердое межклеточное вещество костной ткани (в сравнении с хрящевой тканью) придает костям более высокую прочность, и в тоже время – хрупкость. Органические и неорганические компоненты в сочетании друг с другом определяют механические свойства костной ткани - способность сопротивляться растяжению и сжатию.
Несмотря на высокую степень минерализации, в костных тканях происходят постоянное обновление входящих в их состав веществ, постоянное разрушение и созидание, адаптивные перестройки к изменяющимся условиям функционирования. Морфофункциональные свойства костной ткани меняются в зависимости от возраста, физических нагрузок, условий питания, а также под влиянием деятельности желез внутренней секреции, иннервации и других факторов.Классификация
Существует два основных типа костной ткани:ретикулофиброзная (грубоволокнистая),
пластинчатая.
Эти разновидности костной ткани различаются по структурным и физическим свойствам, которые обусловлены главным образом строением межклеточного вещества. В грубоволокнистой ткани коллагеновые волокна образуют толстые пучки, идущие в разных направлениях, а в пластинчатой ткани костное вещество (клетки, волокна, матрикс) образуют системы пластинок.
К костной ткани относятся также дентин и цемент зуба, имеющие сходство с костной тканью по высокой степени минерализации межклеточного вещества и опорной, механической функции.
Клетки костной ткани: остеобласты, остеоциты и остеокласты. Все они развиваются из мезенхимы, как и клетки хрящевой ткани. Точнее – из мезенхимных клеток склеротома мезодермы. Однако остеобласты и остеоциты связаны в своём диффероне так же, как фибробласты и фиброциты (или хондробласты и ходроциты). А остеокласты имеют иное, - гематогенное происхождение.Костный дифферон и остеогистогенез
Развитие костной ткани у эмбриона осуществляется двумя способами:
1) непосредственно из мезенхимы, - прямой остеогенез;
2) из мезенхимы на месте ранее развившейся хрящевой модели кости, - это непрямой остеогенез.
Постэмбриональное развитие костной ткани происходит при ее физиологической и репаративной регенерации.
В процессе развития костной ткани образуется костный дифферон:стволовые клетки,полустволовые клетки (преостеобласты),остеобласты (разновидность фибробластов),
остеоциты.
Вторым структурным элементом являются остеокласты (разновидность макрофагов), развивающиеся из стволовых клеток крови.
Стволовые и полустволовые остеогенные клетки морфологически не идентифицируются.
Остеобласты (от греч. osteon - кость, blastos - зачаток), - это молодые клетки, создающие костную ткань. В кости они встречаются только в надкостнице. Они способны к пролиферации. В образующейся кости остеобласты покрывают почти непрерывным слоем всю поверхность развивающейся костной балки.
Форма остеобластов бывает различной: кубической, пирамидальной или угловатой. Размер их тела около 15-20 мкм. Ядро округлой или овальной формы, часто располагается эксцентрично, содержит одно или несколько ядрышек. В цитоплазме остеобластов хорошо развиты гранулярная эндоплазматическая сеть, митохондрии и аппарат Гольджи. В ней выявляются в значительных количествах РНК и высокая активность щелочной фосфатазы.
Остеоциты (от греч. osteon - кость, cytus - клетка) - это преобладающие по количеству зрелые (дефинитивные) клетки костной ткани, утратившие способность к делению. Они имеют отростчатую форму, компактное, относительно крупное ядро и слабобазофильную цитоплазму. Органеллы развиты слабо. Наличие центриолей в остеоцитах не установлено.
Костные клетки лежат в костных лакунах, которые повторяют контуры остеоцита. Длина полостей колеблется от 22 до 55 мкм, ширина - от 6 до 14 мкм. Канальцы костных лакун заполнены тканевой жидкостью, анастомозируют между собой и с периваскулярными пространствами сосудов, заходящих внутрь кости. Обмен веществ между остеоцитами и кровью осуществляется через тканевую жидкость этих канальцев.
Остеокласты (от греч. osteon - кость и clastos - раздробленный), - это клетки гематогенной природы, способные разрушать обызвествленный хрящ и кость. Диаметр их достигает 90 мкм и более, и они содержат от 3 до нескольких десятков ядер. Цитоплазма слабобазофильна, иногда оксифильна. Остеокласты располагаются обычно на поверхности костных перекладин. Та сторона остеокласта, которая прилежит к разрушаемой поверхности, богата цитоплазматическими выростами (гофрированная каемка); она является областью синтеза и секреции гидролитических ферментов. По периферии остеокласта находится зона плотного прилегания клетки к костной поверхности, которая как бы герметизирует область действия ферментов. Эта зона цитоплазмы светлая, содержит мало органелл, за исключением микрофиламентов, состоящих из актина.
Периферический слой цитоплазмы над гофрированным краем содержит многочисленные мелкие пузырьки и более крупные - вакуоли.
Полагают, что остеокласты выделяют СО2 в окружающую среду, а фермент карбоангидраза способствует образованию угольной кислоты (Н2СО3) и растворению кальциевых соединений. Остеокласт богат митохондриями и лизосомами, ферменты которых (коллагеназа и другие протеазы) расщепляют коллаген и протеогликаны матрикса костной ткани.
Считается, что один остеокласт может разрушить столько кости, сколько создают 100 остеобластов за это же время. Функции остеобластов и остеокластов взаимосвязаны и регулируются гормонами, простагландинами, функциональной нагрузкой, витаминами и др.
Межклеточное вещество (substantia intercellularis) состоит из основного аморфного вещества, импрегнированного неорганическими солями, в котором располагаются коллагеновые волокна, образующие небольшие пучки. Они содержат в основном белок - коллаген I и V типов. Волокна могут иметь беспорядочное направление - в ретикулофиброзной костной ткани, или строго ориентированное направление - в пластинчатой костной ткани.
В основном веществе костной ткани, по сравнению с хрящевой, содержится относительно небольшое количество хондроитинсерной кислоты, но много лимонной и других кислот, образующих комплексы с кальцием, импрегнирующим органическую матрицу кости. Кроме коллагенового белка, в основном веществе костной ткани обнаруживают неколлагеновые белки (остеокальцин, сиалопротеин, остеонектин, различные фосфопротеины, протеолипиды, принимающие участие в процессах минерализации), а также гликозаминогликаны. Основное вещество кости содержит кристаллы гидроксиапатита, упорядоченно расположенные по отношению к фибриллам органической матрицы кости, а также аморфный фосфат кальция. В костной ткани обнаружено более 30 микроэлементов (медь, стронций, цинк, барий, магний и др.), играющих важнейшую роль в метаболических процессах в организме. Систематическое увеличение физической нагрузки приводит к нарастанию костной массы от 10 до 50% вследствие высокой минерализации.
Костный скелет выполняет три важнейшие функции: механическую, защитную и метаболическую (обменную). Механическая функция . Кости, хрящи и мышцы образуют опорно-двигательный аппарат, бесперебойная работа которого во многом зависит от прочности костей. Защитная функция. Кости образуют каркас для жизненно важных органов (грудная клетка, череп, тазовые кости, позвоночник). также являются вместилищем для костного мозга, играющего важнейшую роль в развитии клеток крови и иммунной системы.
Метаболическая функция. Костная ткань выступает как депо кальция, фосфора и принимает участие в минеральном обмене веществ в организме, что обусловлено ее высокой лабильностью.
Выделяют губчатую и компактную костные ткани, которые имеют сходный состав и структуру матрикса, но различаются плотностью.
Компактная костная ткань составляет 80 % зрелого скелета, окружает костный мозг и области губчатой кости.
Губчатая костная ткань по сравнению с компактной имеет примерно в 20 раз большую поверхность на единицу объема.
Компактная кость и костные трабекулы образуют каркас для костного мозга.
Костная ткань представляет собой динамическую систему , в которой на протяжении всей жизни человека протекают процессы разрушения старой кости и образования новой, что составляет цикл ремоделирования костной ткани. Это цепь последовательных процессов, благодаря которым кость растет и обновляется.
В детском и подростковом возрасте кости подвергаются активному ремоделированию, при этом костное образование преобладает над костным разрушением (резорбцией).
Кости состоят из двух основных частей: органической и неорганической. Органической основой кости являются клетки нескольких классов. Остеобласты представляют группу клеток-строителей, остеокласты разрушают костную ткань, удаляя лишнее. Основной структурной единицей кости являются остеоциты, синтезирующие коллаген . Клетки костной ткани - остеобласты, остеоциты и остеокласты - в кости составляют 2%.
Остеоциты - высокодифференцированные клетки, происходящие из остеобластов, окруженные минерализованным костным матриксом и располагающиеся в остеоцитарных лакунах, заполненных коллагеновыми фибриллами. В зрелом скелете человека остеоциты составляют 90 % всех остеогенных клеток.
Биосинтетическая активность остеобластов и остеоцитов, а в связи с этим и организация межклеточного вещества, зависит от величины и направленности вектора нагрузки, характера и величины гормональных влияний и факторов местного окружения клетки. Поэтому костная ткань - это лабильная и постоянно меняющаяся структура.
Одним из наиболее интенсивных способов резорбции костной ткани является остеокластическая резорбция , осуществляемая остеокластами. Они имеют внескелетное происхождение из предшественников моноцитов макрофагов.
Матрикс костной ткани занимает 90 % от объема, остальная часть приходится на клетки, кровеносные и лимфатические сосуды. В межклеточном веществе костной ткани содержание воды низкое.
Костный матрикс состоит из органического и минерального компонентов. Неорганические компоненты составляют около 60% веса кости, органические - 30%; надолго клеток и воды приходится около 10%. Суммарно в составе компактной кости минеральный матрикс по весу и в процентном отношении несколько меньше органического.
В костной ткани содержится более 30 микроэлементов: магний, медь, цинк , стронций, барий и другие, принимающие активное участие в метаболических процессах в организме.
Кости являются крупнейшим банком минералов в организме . В них сосредоточено 99% кальция, 85% фосфора и 60 % магния. Минералы постоянно расходуются на нужды организма, и, следовательно, существует необходимость восполнять их.
В определенные периоды жизни (беременность, кормление грудью, половое созревание у детей, климакс у женщин , стрессовые ситуации, при ряде заболеваний кишечника и эндокринной системы, когда нарушена всасываемость кальция и витамина при травмах) возникает повышенная потребность в кальции.
Особенно быстро кальций расходуется при гормональной перестройке организма женщины (беременность, менопауза). Для будущих матерей очень важно позаботиться о достаточном содержании кальция в пище, ибо от этого зависит правильное формирование и развитие скелета у ребенка и отсутствие в дальнейшем кариеса. Восполнение кальция необходимо для нормального функционирования органов и систем, а также для профилактики ряда заболеваний, в том числе остеопороза.
В норме баланс между синтезом и резорбцией костной ткани меняется очень медленно. Но он подвергается множеству влияний со стороны как эндокринной системы (гормоны яичников, щитовидной и паращитовидной желез, надпочечников), так и окружающей среды и многих других факторов. И малейший сбой в системах регуляции и обмена веществ ведет к нарушению равновесия между клетками-строителями и клетками-разрушителями, снижению уровня кальция в костях.
Большинство людей достигает максимальной костной массы между 25 и 35 годами. Это значит что в это время кости обладают наибольшей плотностью и крепостью. К сожалению, в дальнейшем эти свойства постепенно теряются, что может привести к развитию остеопороза и впоследствии к неожиданным переломам.
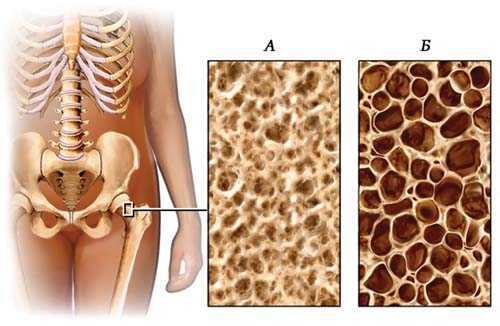

Состояние костной ткани:
А — в норме;
Б — при остеопорозе
Моделирование и ремоделирование костной ткани обеспечивается сложным комплексом факторов. К ним относят системные факторы, среди которых можно выделить две группы гормонов:
- кальцийрегулирующие гормоны (паратиреоидный гормон, кальцитриол - активный метаболит витамина 03, кальцитонин);
- другие системные гормоны (глюкокортикоиды, половые гормоны, тироксин, соматотропный гормон, инсулин и др.).
Участвуют в регуляции костной перестройки ростовые факторы, объединенные в большую группу, - инсулиноподобные факторы роста (ИФР-1, ИФР-2), фактор роста фибробластов, трансформирующий фактор роста (ТФР-р), фактор роста тромбоцитарного происхождения и др.
Важную роль в регуляции костного метаболизма и минерального обмена играют и другие факторы микроокружения, продуцируемые самими клетками, - простагландины, морфогенетические белки, остеокластактивирующий фактор и др.
Среди гормонов наиболее существенное влияние на метаболизм костной ткани и гомеостаз кальция оказывают паратгормон, витамин D и его метаболиты и в меньшей степени - кальцитонин. У женщин на регуляцию метаболизма костной ткани влияют эстрогены. То или иное участие в регуляции ремоделирования кости принимают почти все другие гормоны, продуцируемые железами организма.
Родоначальные клетки костной и хрящевой тканей
Костные клетки имеют мезенхимальное (мезенхимное, мезодермальное) происхождение. Во взрослом организме они образуются из остеогенных стволовых клеток-предшественников, которые локализуются на границе между костью и хрящевой или костномозговой тканью. Дифференцируясь, они превращаются в остеобласты, а затем - остеоциты. Рост длинных трубчатых костей осуществляется путем энхондрального окостенения. Причем увеличение диафизов в ширину происходит только со стороны периоста, а метафизов - только со стороны эндооста. Процесс костной резорбции имеет, соответственно, обратное направление (Burne, 1971, 1976; Фриденштейн, Лалыкина, 1973).
Схема образования костной и хрящевой ткани, построенная на основании работ А.Я. Фриденштейна, Е.А. Лурия (1980), А.Я. Фриденштейна и др. (1999), И.Л. Черткова, О.А. Гуревич (1984), В.П. Шахова (1996). Н. Castro-Malaspina et al., (1980, 1982) с некоторыми модификациями, представлена на рисунке.
Схема остеогенеза, хондрогенеза и остеокластогенеза. СККХ - стволовая клетка костной и хрящевой ткани, СКК - стволовая клетка кроветворения, ПКПК - полипотентная клетка-предшественница кроветворной ткани, ПКХК - полипотентная клетка-предшественница для костной и хрящевой тканей, Б(У)КПКХ - би(уни)потентная клетка-предшественница костной и хрящевой ткани, КПКМ - клетка, переносящая кроветворное микроокружение, КОЕф - колониеобразующая единица фибробластов, У (Б) КПК (X, М, Г, Э, Мег, Т, В) - унипотентная (бипотентная) клетка-предшественница костной (хрящевой, макрфагальной, гранулоцитарной, эритроидной, мегакариоцитарной, Т и В-лимфоидной) ткани
Процесс образования костной ткани представляет собой сложный многоступенчатый процесс, при котором клетки различных гистогенетических линий проходят последовательную трансформацию путем пролиферации, дифференцировки и специализации с образованием композитной структуры, называемой костью.
При этом следует подчеркнуть, что если костная и хрящевая ткань формируется в эмбриогенезе из дорсального сомита мезодермы, то кроветворная ткань, из которой ведут свое происхождение остеокласты, - через стадию спланхнической мезодермы. По своему гистогенезу остеоциты и остеобласты ближе к соединительно-тканным, мышечным и кожным элементам, а остеокласты - к клеткам крови и эндотелию (Coalson, 1987). Наличие в остеокластобластомах эпителиальной и мышечной ткани, по-видимому, подтверждает эту точку зрения.
После расхождения направления развития остеохондрогенеза от гемопоэза в эмбриональном развитии, в зрелом организме процесс образования костных клеток осуществляется из более дифференцированного, фиксированного в тканях или циркулирующего незрелого стромального элемента (мезодермальной клетки, недифференцированного фибробласта, остеогенного предшественника или прекурсора) (Фриденштейн, Лурия, 1980; Альберст и др., 1994; Омельянченко и др., 1997). Наряду с наличием полипотентной стволовой клетки для костной и хрящевой ткани, существуют и более дифференцированные прекурсоры. СККХ имеют высокий пролиферативный потенциал, обладают полипотентностью. Они образуют, как минимум, костные и (или) хрящевые кариоциты, которые преимущественно находятся в G1-G2-стадии клеточного цикла (Фриденштейн, Лалыкина, 1977; Фриденштейн, Лурия, 1980; Фриденштейн и др., 1999; Чертков, Гуревич, 1984).
В культуре ткани in vivo и in vitro они образуют хрящевую или костную ткань, которая может быть представлена в форме колоний, обозначенных как колониеобразующие единицы фибробластов-КОЕф (Фриденштейн, Лурия, 1980). С помощью хромосомных и биохимических маркеров на радиационных химерах было показано, что КОЕф имеют клональную природу, отличную по своему происхождению от гемопоэтических клеток костного мозга, включая остеобласты и остеоциты (Чертков, Гуревич, 1984).
Нами в суспензионной культуре ткани костного мозга мышей линии Balb/c была изучена зависимость между количеством вводимых в среду кариоцитов и числом образовавшихся колоний. Для этого костный мозг вымывался в силиконизированную пробирку, суспендировался в D-MEM среде, содержащей 20% эмбриональной телячьей сыворотки, 40 мкг/мл гентамицина, 200 мМ, L-глютамина хепес и культивировался в течение 2-3 недель в пластиковых флаконах при 37 °С. Плотность посева составила от 104 до 107 клеток на мл.
Зависимость образования КОЕф при введении в культуру различного количества клеток костного мозга мышей линии Balb/c
Приведенные данные свидетельствуют о том, что в целом зависимость между количеством вводимых в культуру миелокариоцитов и КОЕф носит линейный характер, что еще раз подтверждает их клональное происхождение.
При трансплантации их под капсулу почки или под кожу, они обладают способностью формировать костную, либо хрящевую ткань.
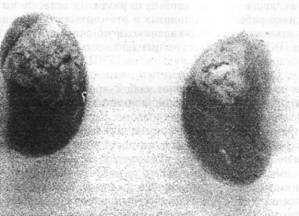
Макроскопический препарат эктопической костной ткани, выросшей под капсулой почки после трансплантации в нее костного мозга стрессированных мышей F1 (CBAxC57Bl). Слева - на верхнем полюсе органа отчетливо виден большой очаг костеобразования. Справа - контроль (костный мозг взят от нестрессированного животного)
Одним из свойств СККХ является то, что они сохраняют свои пролиферативные и дифференцировочные потенции при многократном переносе первоначальной культуры от одного донора к другому. По-видимому, повреждение генома на этом уровне приводит к образованию остеосарком.
В результате дифференцировки СККХ образуются более дифференцированные клетки-предшественники типа КПКХ (клетки предшественники для костной и хрящевой ткани) или БКПКХ (бипотентные), затем - УПКПК и УПКПХ (унипотентные для кости, либо хряща). Общей закономерностью для пула родоначальных клеток любой ткани, в том числе и костной, является постепенное снижение способности к самообновлению и пролиферации, утрате полипотентности, увеличению доли прекурсоров, находящихся в S-периоде клеточного цикла, повышению чувствительности к действию ростовых факторов, гормонов, цитокинов и других регуляторных молекул. Теоретически этот процесс может идти равномерно или скачкообразно. Из-за этого течение остеогенеза может идти в различных режимах, темпе, с образованием костной ткани качественно и количественно отличной по своим морфофункциональным свойствам. На наш взгляд, введение биоматериала в кость обязательно включит тот или иной путь развития остеогенных клеток. Однако работ, выполненных в этом чрезвычайно интересном направлении, мы, к сожалению, не обнаружили.
Если ПКПКХ обладают полипотентностью, то БКПКХ образуют хрящевую или костную ткань, УКПК - только кость, а УКПХ - хрящ. Следует отметить, что все категории родоначальных клеток представляют собой чрезвычайно гетерогенную популяцию, внутри которой морфофункциональные свойства варьируют в широком диапазоне. Кроме того, для каждой из стадий развития КП имеется значительное количество переходных форм, которые все еще не могут быть идентифицированы с помощью имеющихся технологий. Несмотря на то, что методы выявления стромальных и остеогенных клеток-предшественников были открыты еще в начале 70-х годов, явного прогресса в понимании их свойств, способов регуляции и роли в процессах ремоделирования костной ткани достигнуто не было (Фриденштейн, Лалыкина, 1973; Фриденштейн и др., 1999; Чертков, Гуревич, 1984; Стецулла, Девятов, 1987; Омельянченко и др., 1997).
Следует отметить, что стволовые и коммитированные клетки-предшественники костной и хрящевой тканей находятся под контролем локальных и дистантных регуляторных механизмов. В последнюю группу входят факторы, которые оказывают свое действие через нейроэндокринную, иммунную, ретикулоэндотелиальную, опиатную, NO и другие системы путем выработки или связывания дальноранговых мессенжеров (эстрогены, глюкокортикоиды, эндорфины, адреналин и т.п.). Локальные механизмы действуют через прямое изменение морфофункциональных свойств микроокружения костной ткани, межклеточные контакты, местную выработку цитокинов, медиаторов, коротко-живущих биоактивных веществ и т.п. Межклеточные взаимодействия относятся к морфогенетическим процессам, они контролируют дифференцировку, специализацию, морфообразование клеток в тканях и органах. Механизмы их реализации осуществляются с помощью позиционно-информационных и индукционных взаимодействиях. Они еще малоизученны. Тем не менее, согласно концепции о позиционной информации, в организме существует морфогенетическое поле. Оно контролируется с помощью экспрессии гомейозисных генов типа НOХ1, НOХ2, НОХЗ, НOХ4, НOХ7, заставляя клетки помнить не только место своей локализации, в соответствии с координатными осями, но и выполнять миссию, которую они должны осуществить в процессе своей жизни, например восстановление кости при ее повреждении. Считается, что в сохранении позиционной информации большую роль играют мезенхимальные элементы, в частности макрофаги, остеобласты, остеоциты, остеокласты, эндотелий и фибробласты (Gilbert, 1994).
Индукционные механизмы регулируют процессы пролиферации и дифференцировки самообновляющихся клеточных популяций с помощью цитокинов, ростовых факторов, различных метаболитов и короткоранговых мессенжеров, вплоть до прямых клеточных взаимодействий.
Особенностью выбора направления дифференцировки поли- и бипотентных остеогенных предшественников является то, что он в первую очередь зависит от парциального давления кислорода. Если это давление достаточно высоко, то костные прекурсоры развиваются в направлении остеогенеза, а если низкое, то напротив, образуют хрящевую ткань (Bassett, Herman, 1961). При этом следует помнить, что адекватное поступление кислорода к клеткам возможно только при наличии развитой сети микроциркуляторного русла: максимальная величина удаления костных прекурсоров не должна превышать 100 мкм (Хэм, Кормак, 1983).
Система остеонов
Гаверсова система во взрослой кости постоянно обновляется. При этом всегда можно выделить несколько типов остеонов - эволюционирующих или развивающихся (5-10%), зрелых (50-75%), дегенерирующих или инволюционирующихся (10-20%), реконструирующихся (5-10%) и нежизнеспособных (5-10%).
Считается, что остеон (Гаверсова система) возникает только на основе туннеля, образующегося в результате действия моноцитов, макрофагов и остеокластов, заполняющегося изнутри концентрированными слоями костной ткани, формирующейся остеобластами и остеокластами (Хэм, Кормак, 1983). Следует отметить, что система остеонов представляет собой подвижную структуру, которая постоянно эволюционирует. Как это не парадоксально, работ, посвященных изучению кинетики остеонов, крайне мало. С помощью радионуклидных методов исследования было установлено, что годичная скорость замещения поверхностного слоя костной ткани составляет 5-10% (Harris, Heaney, 1969). По-видимому, и темп обновления остеонов имеет сходные параметры. Интересно, что диаметр остеонов в процессе развития не является постоянной величиной, а в течение всей своей жизни подвержен ряду последовательных изменений. Анализ литературных и собственных данных позволяет считать, что границы Гаверсовой системы, ограниченные линией цементации, у молодых, развивающихся и реконструирующихся остеонов составляют 80-150 мкм, зрелых - 120-300, а инволюцинирующих, дегенерирующих - менее 200 мкм. Если процесс образования остеонов протекает на границе надкостница/ кость, то вместо канала в начале формируется желобок, стенки которого выстланы остеогенными клетками, которые пролиферируют, формируя валик. Стенки этих клеточных выступов смыкаются, образуя полость, внутри которой, как правило, располагается не менее одной питающей артерии. Затем остеогенные клетки дифференцируются в остеобласты и остеоциты с формированием остеона. Предположения о том, что материал, используемый в травматологии, должен иметь диаметр пор равный размеру остеонов, высказывалось и ранее (Гюнтер и др., 1992). Однако этими авторами не был обоснован главный критерий, согласно которому размер пор должен соответствовать диаметру развивающихся, реконструирующихся, зрелых остеонов. При нарушении этого принципа в сторону увеличения или уменьшения диаметра пор полноценная костная ткань образовываться не будет. Иными словами, можно считать, что размер остеонов представляет собой важный морфообразующий фактор, который необходимо учитывать при создании искусственной костной ткани. Механизм этого феномена не совсем понятен. Он, вероятно, генетически запрограммирован в самих остеогенных клетках и является важным элементом костного микроокружения. Вместе с тем, следует подчеркнуть, что наряду с объемными характеристиками, например диаметром остеонов, при создании материалов необходимо учитывать и другие биологические принципы, речь о которых пойдет ниже.
А.В. Карпов, В.П. Шахов
Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе