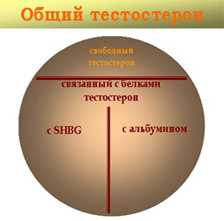
Идиотиповые и антиидиотиповые антитела
Антиидиотиповые антитела
Выше было упомянуто о том, что структуры активного центра иммуноглобулиновой молекулы - идиотипы - обладают специфическими антигенными свойствами. Такими же свойствами обладают структуры активного центра клеточных рецептров лимфоцитов. Поскольку до начала иммунного ответа структуры данной специфичности в организме практически отсутствуют, к ним не формируется естественная иммунологическая толерантность. После того как в организме произошло образование антител, к их идиотиповым структурам продуцируются антитела II порядка, называемые антиидиотиповыми. В свою очередь, в ответ на антиидиотиповые структуры образовавшихся антител II порядка в организме формируются антитела III порядка, которые могут быть названы анти-антиидиотиповыми. Те антиидиотиповые антитела, которые образовались против антигенсвязывающей структуры идиотипа, представляют собой зеркальное изображение этой структуры. Следовательно, они являются внутренним аналогом активного центра антигена (эпитопа), который вызвал образование антител I порядка. Роль антиидиотиповых антител (АИА) в организме очень разнообразна. Связываясь с идиотипами антител, они нейтрализуют их действие. Будучи аналогом антигена АИА, могут вызывать в организме иммунный ответ и иммунологическую толерантность, а при определенных условиях и иммунопатологический процесс. По современным представлениям, идиотипы, антиидиотипы и антитела и III, и IV порядка формируют в организме сложную сеть ауторегуляции специфического иммунного ответа, в которой кроме гуморальных антител участвуют идиотипы клеточных рецепторов.
Антиидиотиповые антитела, полученные по гибридомной технологии, используются в качестве принципиально новых вакцин, особенно в тех случаях, когда применение вакцин из микроорганизмов встречает затруднения вследствие высокой реактогенности или трудностей изготовления.
32) Антигенные свойства иммуноглобулинов, изотипы, аллотипы, идиотипы. Полные и неполные антитела.
Иммуноглобулин, как и всякий белок, обладает антигенностью и выраженной иммуногенностью. В молекуле Ig различают 4 типа атигенных детерминант: видовые, изотипические, аллотипические и идиотипические. Видовые антигенные детерминанты характерны для Ig всех особей данного вида (например, кролика, собаки, человека). Они определяются строением легкой и тяжелой цепей. По этим детерминантам можно идентифицировать видовую принадлежность антител.
Изотипические антигенные детерминанты являются групповыми. Они локализуются в тяжелой цепи и служат для дифференцировки Ig на 5 изотипов (классов) и множество подклассов .
Аллотипические антигенные детерминанты являются индивидуальными, т.е. присущими конкретному организму. Они располагаются в легкой и тяжелой полипептидных цепях. На основании строения аллотипических детерминант можно различать особи внутри одного вида.
Идиотипические антигенные детерминанты отражают особенности строения антигенсвязывающего центра самой молекулы Ig. Они образованы V-доменами легкой и тяжелой цепей молекулы Ig. Обнаружение идиотипических антигенных детерминант послужило основанием для создания теории идиотип-антиидиотипической регуляции биосинтеза антител.
Полные и неполные антитела. Такое подразделение основано на способности образовывать в реакции агглютинации или преципитации (in vitro) хорошо различимый глазом результат. Таким свойством обладают полные антитела. К ним относятся IgМ, а также некоторые IgA и G.
Неполные антитела лишены такой способности, несмотря на то, что они специфически связываются с антигеном - их еще называют неагглютинирующими, непреципитирующими или блокирующими антителами.
33) Моноклональные антитела.Получение( гибридомная технология) и применение.
Каждый В-лимфоцит и его потомки, образовавшиеся в результате клеточного деления (т.е. клон), способны синтезировать антитела с паратопом строго определенной специфичности. Такие антитела получили название моноклональных. В естественных условиях макроорганизма получить моноклональные антитела практически невозможно, так как на одну и ту же антигенную детерминанту одновременно реагируют до 100 различных клонов В-лимфоцитов, незначительно различающихся антигенной специфичностью. Поэтому в результате иммунизации даже монодетерминантным антигеном мы всегда получаем поликлональные антитела.
Принципиально получение моноклональных антител выполнимо, если провести предварительную селекцию антителопродуцирующих клеток и их клонирование, т.е. получение необходимых клонов. Однако задача осложняется тем, что число генераций В-лимфоцитов, как и других эукариотических клеток, ограничено. Тем не менее проблема была успешно решена Д. Келлером и Ц. Мильштайном (1975). Исследователи получили гибриды иммунных В-лимфоцитов и миеломных (опухолевых) клеток, которые обладали свойствами антителопродуцента и «бессмертием» раково-трансформированной клетки. Такой вид клеток получил название гибридом. В ходе дальнейшей селекции были отобраны клоны с наивысшей продуктивностью и аффинностью специфических антител. Гибридомные моноклональные антитела нашли широкое применение при создании диагностических и лечебных иммунобиологических препаратов.
Антиидиотипические антитела как иммуногены, толерогены и патогены
Медииинсшя иммунологи*
1999. Т. 1, № 1-2, С. 23 - 26 © 1999. СПб РО РААКИ
АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА КАК ИММУНОГЕНЫ, ТОЛЕРОГЕНЫ И ПАТОГЕНЫ
Софронов Б.Н., Косицкая Л.С., Шемеровская Т.Г.,
Житнухин Ю.Л., Бичурина М.А.
Институт экспериментальной медицины РАМП. ГЪроЬской ревматологический центр, Научна исследовательский институт эпидемиологии и микробиологии им. Пастера,
Санкт - Петербург
В1943 году В.И. Иоффе к К.М. Роаенталь впервые установили, что антитела обладают антигенной специфичностью и способны индуцировать продукцию шті-антател, нзанмодейству кшцтхс антителам и к данному антигену, независимо от их происхождения [3]. Через 20 лет появились новые сообщения [10.11 |, установившие тот же факт антигенной специфичности .иггител. В 1974 году.)ете [9] обозначил антигенсвязы-шлцие структуры антител как идиотипы. состоящие из шшотопов-компонеитов, обладающих самостоя-тгьиой антигенной специфичностью. Антитела к ішіютгтам получили название антииднотипнческнх. ]егпе сформулировал теорию идиотштическнх цепей, с огласно которой регуляция иммунного ответа осуще-пьчяется аз счёт взаимодействия идиотипических и аіггиидготіпичсских структур, формируемых в орга-тпме. Очевидно, чго анги-аптитела по В.И. Иоффе и іщпшдпотктшчі'сіпіе антитела по |сгпе обозначают одниИТОжеструктуры. Мы в дальнейшем пользуемся герм (том «антиндиотипичсские антитела (ЛИ А), который принят в современной литературе.
Цель пастоящего сообщения — обобщить результаты собственных исследовании по выявлению имму-ногеїпцдх.тшіерогеїпгьіх и патогенных свойств АИА и условий реализации этих свойств
Адрес для переписки:
Копщкая Людмила Самуилота — к. 6 н.. старішій научный сотрудник Отдела имму-игшгии НИИ экспериментальной медицины РАМИ 1Ц7376. Спеккт - Петербург, ул. академика Павлова. 12. ЛИИ экспериментальной медицины РАМН, отдня иммунологии
Тел: Ш) 234*16-69
Фт: (№) 234-94-8.9
■ -талі: [email protected]
Методика исследований
Опыты проводили из непородных кроликах массой тела 2-2,5 кг. мышах / С BA х С57 В! / FI Maccofi 16 -18 г, морских свинках-сампах массой тела 350 - 400 г. Животные были получены из питомника РАМН «Рал-иолово» В качестве антигенов использовали яичный альбумин («Sigma»), Vi-антиген (НИИ им. Габричевского, Москва), инактивированную гриппозную вак цииу А/Мнсшсиии (ИЗ N2) и кроличий иммуноглобулин к ней (НИИ им. Пастера, С.-Петербург), а также основной белок миелина из ткани спинного мозга быка. Из исследуемых сывороток готовили солевым методом иммуног лобулины, либо методом аффинной хроматографии чистые антитела |7 |. Для выявления антител использовали реакции пассивной гемагглюти-нации (РПГА). связывания комплемента (РС-К) EL1SA. Продукцию антител клетками определяли по методу Jerne и Nordin [8]. Циркулирующие иммунные комплексы (ЦИК) определяли методом осаждения подкисленной дистиллированной водой, а состав иммунных комплексов определяли после диссоциации комплексов солянокислым цистеином ]5|.
Результаты и обсуждение
Для изучения динамики АИА в аутологичной системе кроликов иммунизировали Vi-антигеном, вводимым дважды в подушечки лап (2 мкг) в полном адъюванте Фрейнда (Г1АФ), а затем в лимфоузлы (10 мкг). Каждые 10 дней в течение 160 суток j животных брали пробы крови, готовили сыворотки н иммуноглобулиновые фракции из них для последу ющего анализа. Анализ состоял в том, что в пробах определяли антитела к введенному антигену. 11о способности сывороток или иммуноглобулинов из них,
А)
Пи - А Г'
J>u
imj
КО
5(1 100 сутки
Динамика антител, антиидиотипических антител (АИА) и циркулирующих иммунных комплексов (ЦИК) после введения Уі-антигена или собственных АИА.
1 - Антитела к Уі-антигену.
2 - Антиидиотипические антитела (АИА).
3 - АИА после их введения в составе аутоиммуноглобулина.
4 - Антитела к Уі-антигену после введения АИА.
5 - ЦИК, состоящие из Уі-антигена и антител к нему.
6 - ЦИК, состоящие из антител к Уі-антигену и АИА.
содержащих антитела, взаимодействовать с пробами, в которых айтител не было, выявляли АИА. В пробах определяли наличие иммунных комплексов и их состав. Как показано на рисунке, в крови иммунизированных кроликов выявлялись антитела к \Ч-антп-гену (1 трафик). После снижения уровня антител с 30 - 40 суток в крови появлялись АИА, достигающие максимального уровня к 80 -100 суткам после окончания иммунизации (2 график). На 10-е и 50 -70-е сутки в крови обнаруживались циркулирующие иммунные комплексы. Однако в первом случае (5 график) они состояли из \м-антигена и соответствующих антител, а во втором (6 график) из антител и АИА. Иммуноглобулиновые фракции, выделенные из сывороток, содержащих АИА, были введены на МО день опыта тем же кроликам, от ко-
горьгх они были получены В результате, сразу после введения в крови были обнаружены введенные АИА, а через 10 суток наблюдался подъем антител (4 трафик). Таким образом, введение иммунизированным кроликам АИА обеспечивало развитие ревакциналь-ного подъема антител. Второй группе кроликов этой серии вместо АИА были введены соответственно антитела. Естественно, что эти антитела могли быт ь обнаружены в крови сразу после введения. Более удивительно то, что вслед за антителами в крови можно было обнаружить появление новой волны АИА, указывающей на то, что и этих условиях антитела обус ловлнвали ревакцнпальный эффект для продукции АИА, образование которых происходило значит е льно раньше, чем после первою появления антител у иммунизированных кроликов.
Эффекты АИА в гомологичной системе были исследованы в опытах иммунизации кроликов кроличьим иммуноглобулинам к вирусу А/Мясспсипи/1/85 (НЗМ2). Иммуноглобулин вволили кроликам двукрат -ни в ПАФ в суммарной дозе 8 мг. Между 10 и 40еутка мі после второй инъекции аи шгена в крови животных можно было обнаружить антитела, взаимодействую щиев РСК с иммуноглобулином, использованным для пмлгугпшции. по нес кроличьими иммуноглобулинами других специфичностей. Это показывало, что в сыворотках содержались А НА В крови животных содержались также ДИК, состоящие из введенных антител и образовавшихся АИА. Через 100 дней, когдав крови животных уже нельзя было определить НИ АИА, НИ ЦИК, этих кроликов, а также грушгу интактных живо тых вакцинировали инактивированной гршшозной вакциной. В результате в крови животных, подготовленных антителами, формировались антитела, достигающие в РИГА ти гра 35 ± 0.9. а в РСК 16± 2,4. У кро-.шков контрольной фуппы аггтитела в Р ИГА достигали шиш, титра 8,5 ± 0,4, а в РСК не обнаруживались вовсе. Следовательно, введение животным гомологичных антител индуцирует через хгосредство АИА иммунологическую память, то есть готовность к вторичному ответ)' на впервые вводимый гриппозный антиген.
Обнаружение в организме ЦИ К. состоящих из двух иммуноглобулинов-антител и АИА, поставило вопрос: какой га компонентов иммунного комплекса ифаст роль антигена, а какой выполняет функцию антитела Для ответа на этот вопрос из кроличьих агп и те л к V І-лнтагену н соответствующих АИА были пряготоаче-ны РаЬ-фрагмеыты [ 121. Полученные ИзЬ-фрагмснты соединяли с цельными антителами с целью получить йймушгые комплексы. Как известно, способность им млілого комплекса фиксировать комплемент обусловлен;! активацией молекул антител, вступивших в соединение с антигеном, тогда как антиген в составе ггомплркса таким изменениям не подвергается. Оцен-іл способности приготовленных комплексов фиксировать хомплемент показала следующее. Иммунные комплексы, составленные нативными антителами гг АТ ТА ;< такжг РаЬ-фрашеытамп АИА и нативными антигенами, обладали способностью фиксировать комплемент в разведениях 1:128 ± 0 и 1:142 і 14. Комплексы, иктаплепгшр нативными АИА и РаЬ-фрагментами ниQjye.ii, как и комбинации РаЬ-фрагмеитов обоих иммуноглобулинов, комплемент не фиксировали. Это Показывает, что в иммунном комплексе «идиотип-ан-тппдоотид» глобулин. содержащий ндиотигшчеекую структуру, играет роль антитела, а АИА является ан-тш-пом.
Толерагепныс свойства АИА оценивали в опытах на мы шах (СВА х С57В1)П Мышей иммуммзирова-.11! \'|-антнгеном пли яичным альбумином (ЯА). получали емворолки, содержащие антитела. Выделенными из сына роток иммуноглобулинами иммунизировали ^рупа мышей н получали от них сыворотки, содержа
щие АИА. Из этих сывороток готовили иммуноглобу лины. содержащие АИА которые испьгтывали на то-.лерогенность. Для этого интактнг.гм мышам той же линии вводили в вену но 0,5 мг нативною иммуноглобулина, содержащего АИА, либо 0.5 мг того же иммуноглобулина, подвергнул ого ультркщенфнфу гар< »ва нпю с целью деагрегации. У этих мышей не формировались антитела в отличие от контрольных животных, кот орым те же иммуноглобулины вводили в ПАФ. Иммунизация подготовленных введением АИА мышей антигенами в иммуиогенных дозах не обусловливали продукции агггител. Это е.видетельел вуст о том. что введение АИА бел ПАФ индуцировало развит ие иммунологической толерантности к соответствующим антигенам. Наличие толерантности было под тверждено в опытах переноса клеток селезенки мы -шей, толерантных к Vi-антигеву, облученным реципиентам. Перенесенные клетки сохраняли ареакливность к антигену в другом организме, что указывает на индукцию АИА истинной толерантности клеток, обусловливающих иммунные реакции.
Для оценки патогенного действия АИА ау тологичные АИА были введены виуфикожно кроликам, сенсибилизированным яичным альбумином (ЯА). Было установлено, что сенсибилизированные кролики о твечают иа введение АИА местными реакциями диаметром 17 ± 1,2 мм, на введение ЯА реакцией диаметром 16 ± 1,2 мм. на введение любого другого глобулина или человеческого альбумина реакции не дают. Введеній, кроличьих АИА или ЯА в кожу несено поил тирован ных животных реакции не вызывало. АИА и Я Л в опытах in vitro снижали миг рационную активность лейко цитов сенсибилизированных животных, что отражает способность АИА. как и антигена, стимулировать продукцию лнмфокнна (фактора ингибирующего миграцию) клетками сенсибилизированного животного
Способность АИА оказывать патогенное действие было выявлено на модели экспериментального ал лергического энцефаломиелита (ЭАЭ) V морских свинок. Было показано, что этот процесс, иидуциру емый у морских свинок введением 0,1 ли- основного белка миелина в ПАФ, сопровождается появлением в крови, через 28 - 48 суток после введения указанного белка АИА у 20.6 % животных. Сыворотки, со держащие АИА, смешивали г ПАФ и вводили свежим морским свинкам. Для контроля другим животным вводили гомологические сыворотки, не содержащие АИА. В результате у 5 из 25 животных иноку лированных АИА в ПАФ, возникали неврологические расстройства в виде атаксии, мышечной слабости, моно- и параплегий задних конечностей. Указанные симптомы появлялись у животных позднее. чем после введешся основного белка миелина, -па 29 ± 5 сутки, против 17 ± 0.4 суток Летальные случаи не наблюдались. Морфологическое исследование подтвердило заключение о развипш у живої-ных признаков иммунопатологического процесса.
Выявлено наличие клеточной инфильтрации в ЦНС и распада миелина и зонах клеточной воспалительной инфильтрации.
Сыворотки морских свинок, содержащие АИА, вводимые животным до инокуляции энцефалитогенной смеси, снижали частоту развития ЭАЭ в 4 раза — с 35,8 % до 83 %. Этот эффект АИА был подобен действию основного белка миелина, который в случаях введения животных до индукции ЭАЭ предупреждал развитие заболевания [ 1 ].
Приведенные ватой статье материалы, фрагменты которых публиковались ранее [ 2. 5. б |. подтверждают, что формирование АИА или антм-антител по В.И. Иоффе является закономерным этапом развития в организме любой иммунологической или иммунопатологической реакции. Продуцируемые в организме АИА вступаю! в соединение с имеющимися антителами, образуя иммунные комплексы антиген-антитело. в которых роль антигена играют ЛИЛ. Это обстоятельство предстанляется важным для определения функции АИА п организме. АИЛ в составе иммунного комплекса не претерпевают существенных изменений и могут оказывать на организм иммуногенное действнедо тех пор, пока иммунные комплект не подвергнутся элиминации. При этом вопрос об особенностях.элиминадтш иммунных комплексов, составленных Собственными ндиотипи-ческими и антиидиотитшческимн 1 тммуноглобулИНЙ-ми, остается открытым.
Антигеппые свойства АИА проявляются в способности индуцировать в организме как вторичный, так и первичный иммунный ответ, а в экспериментальных условиях и иммунопатологическую реакцию.
Полученные материалы позволяют по-новому оценить эффект пассивной иммунизации иммуноглобулинами, используемой,как известно, для профилактики кори, гриппа, вирусного гепатита и других заболеваний. Ранее считалось, что введение иммуноглобулинов обусловливает временный защитный эффект и после введенных иммуноглобулинов организм остается им мунологич ески девственным. Нами же было показано, что введение антител не только способствует продукции АИА, но и вызывает иервичную активную пммунтто реакцию, выражающуюся в формировании иммунологической памяти н способности организма к ответу па соответствующий антш'еи по втори'тому типу - боцее выраженной реакцией, чем та, которая возникает на впервые вводимый антиген.
АИА как и антигены, способны индуцировать в организме как позитивный иммунный ответ и иммунопатологические реакции, так и иммунологическую толерантность. Отличия состоят в приоритетности развития той и другой формы ответа. Антигены обладают специфической гаптенной структурой и не-специфической структурой, определяющей их имму-иогеииость, Только в тех случаях, когда иммуноген-ная структура на антигене не представлена или
иммуногенный стимул не воспринимается организмом, он проявляет свои голерогенные свойства [6| ЛНА могут быть сравнены с гаптеном. который без дополнительного неспецифического стимула неспособен вызвать позитивную иммунологическую реакцию. Нативные АИЛ выраженнойнммуногенностыо не обладают и в организме ішдуцируют иммуноло-гическую толерантность. В экспериментальных условиях для получения иммуиизаторного эффекта АИА необходимо применение дополнительных неспецифических стимуляторов-адъювантов. В организме ауто-АМА могут быть толерогенами и имму-ногепами. Осуществлен то иммуногенного действия АИА способствует формирование ими иммунных комплексов с антителами, в которых АИА сохраняют все свои свойства и могут приобрести дополнительную иммуногеиность, так как иммунные комплексы способны активно взаимодействовать с антиген - представл ягощими клетками.
Все это показывает, что открытие В.И. Иоффе і імм у-ногеппых свойств антител начало новую страницу в иммунологии, обосновав нопые представления о саморету-ляиии иммунного ответа и новые тти управления им.
Список литературы
1. Житнухии Ю.Л., Софронов Б Н. и соанг // Патол. физнол. - 1976. — X? 5. — С. 55 - 59
2. Житнухии Ю.Л., Косицкая Л.С. и совет, // В кн. «Ыейроиммунологня, эпидемиология и ИНТСрфе-ронология рассеянного склероза*. Мат. 5-н межд. конференции. СПб, 1996. — С. 12 - 15.
3. Иоффе В.И., Розенталь К.М. // ЖМЭИ. 1943. -№ 12. - С. 14- 18.
4. Иоффе В.И., Розенталь К.М. // 'Гам же. -1974. -№3. - С.З - 9.
5. Коспцкая JI С., Софронов Б.Н. // И мм зоология. - 1990. - .№ 3. - С. 17 - 19,
6. Софронов Б.Н.. Шемеровская Т.П. // Иммунология. — 1990. — № 4. — С. 4 - S.
7. Jaton J.C, et al. In Methods of Investigation in immimol. Russ, trans. 1981, М., P. 58 - 59.
S. Jerne N.K., Nofdin N.A, // Science, - 1963. — Vol. 140.- P, 405 - 409.
9. Jerne N.K. // Ann. Immunol. (Paris). — 1974. Vol. 125. -P. 373 -409.
Ю. Kunkel H.C., Mannic M // Science. - 1963. — Vol. 140.-P. 1218-1219.
11. Qndui J.. Michel M. // C. R. Acad. Sci. - 1963. Vol. 257. - P. 805- 807.
12. Porter R.R. // Biochemistry. - 1959. — Vo). 73. — P. 118 - 127.
антиидиотипические антитела
Антитела — Эта статья об иммунологии. Об украинской поп рок группе см. Антитела (группа); о фильме см. Антитела (фильм, 2005). Антитела (иммуноглобулины, ИГ, Ig) это особый класс гликопротеинов, присутствующих на… … Википедия
Иммуноглобулин — Антитела (иммуноглобулины, ИГ, Ig) это белки, относящиеся к подклассу гамма глобулинов, находящиеся в крови, слюне, молоке и других биологических жидкостях позвоночных животных. Иммуноглобулины синтезируются В лимфоцитами в ответ на чужеродные… … Википедия
Иммуноглобулины — Антитела (иммуноглобулины, ИГ, Ig) это белки, относящиеся к подклассу гамма глобулинов, находящиеся в крови, слюне, молоке и других биологических жидкостях позвоночных животных. Иммуноглобулины синтезируются В лимфоцитами в ответ на чужеродные… … Википедия
Иммунитет — I Иммунитет (лат. immunitas освобождение, избавление от чего либо) невосприимчивость организма к различным инфекционным агентам (вирусам, бактериям, грибкам, простейшим, гельминтам) и продуктам их жизнедеятельности, а также к тканям и веществам… … Медицинская энциклопедия
Аутоаллергия — I Аутоаллергия (греч autos сам + Аллергия; синоним: эндоаллергия, аутоагрессия, аутоиммунитет) патологический процесс, в основе которого лежит развитие иммунных реакций на антигены собственных тканей организма. Полагают, что в организме имеются… … Медицинская энциклопедия
идиотип — Идиотипом называют структуру, характеризующую антигенные свойства V области молекулы антител и клеточных рецепторов. Антиидиотипические антитела являются «зеркальным отражением» антигена и поэтому способны вызывать образование антител и… … Справочник технического переводчика
Нестеренко, Владимир Георгиевич — Нестеренко Владимир Георгиевич Место рождения: Днепропетровск, Украина Научная сфера: иммунология Место работы: ФГБУ НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи Минздравсоцразвития РФ Нестеренко Владимир Георгиевич доктор медицинских … Википедия
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе