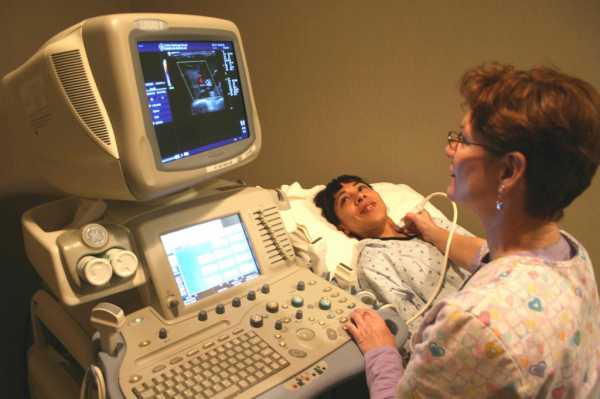
Железистая гиперплазия эндометрия что это
Железистая гиперплазия эндометрия
Железистая гиперплазия – это не опухоль, и это состояние нельзя отнести в область онкологии. Не смотря на то, что гиперплазия характеризуется привычными для опухолевых образований признаками (неукротимым ростом с потерей функции), ее, все же, не относят даже к предраковым заболеваниям.
Поэтому мы будем рассматривать железистую гиперплазию эндометрия как одно из невоспалительных заболеваний матки, которое может, в конечном счете, озлакочествиться, но делает это крайне редко.
Причины железистой гиперплазии эндометрия
Среди причин развития железистой гиперплазии эндометрия множество разнообразных факторов, которые, чаще всего, дополняют друг друга:
- нарушения баланса половых гормонов;
- нарушение функции надпочечников;
- расстройства щитовидной железы;
- расстройства, связанные со снижение чувствительности клеток эндометрия к воздействию гормонов;
- «поломки» генетического кода;
- болезни печени и ЖКТ, которые сопровождаются недостаточным всасыванием незаменимых аминокислот и витаминов;
- болезни яичников, нарушающие их функцию;
- нарушения на высшем уровне регуляции работы половых желез – расстройства синтеза гормонов гипофиза;
- сахарный диабет и другие болезни обмена;
- длительно существующие хронические воспалительные процессы в эндометрии;
- длительный бесконтрольный прием оральных контрацептивов и других гормональных препратов;
- механические повреждения слизистой оболочки матки.
Симптомы железистой гиперплазии эндометрия
Все жалобы, как правило, появляются в период менструации, до или после него. Больные отмечают некоторые изменения менструального цикла и отличия последних циклов от предыдущих. 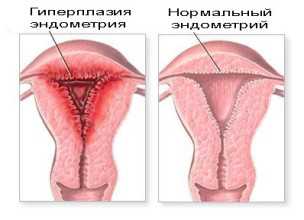 Менструации при железистой гиперплазии сопровождаются болями внизу живота (при этом до начала заболевания женщина могла не страдать от болезненных менструаций), выделения становятся более обильными.
Менструации при железистой гиперплазии сопровождаются болями внизу живота (при этом до начала заболевания женщина могла не страдать от болезненных менструаций), выделения становятся более обильными.
Кроме того, вне цикла могут появляться кровянистые выделения: от мажущих до серьезных маточных кровотечений.
Никаких специфических симптомов это заболевание не имеет: его проявления типичны для всех подобных заболеваний. На фоне гиперплазии эндометрия из него могут формироваться полипы, которые тоже редко приносят женщине какой-либо дискомфорт и обнаруживаются случайно, при очередном обследовании.
Полипы могут быть нескольких видов, в зависимости от характера, давности и тяжести заболевания:
- покрытые нормальным эндометрием;
- железистые;
- фиброзные, не покрытые эпителием;
- железисто-фиброзные;
- аденоматозные (полипы, покрытые активно обновляющимся и растущим эпителием).
В любом случае, эти полипы пронизаны сосудами со «стеклянными» склерозированными стенками, которые легко повреждаются и очень долго кровоточат.
В силу того, что железистая гиперплазия эндометрия напрямую связана с изменениями в гормональном фоне женщины, клиническая картина обязательно дополняется симптомами эндокринных нарушений. Чаще всего женщины отмечают:
- резкие изменения массы тела (как правило, ее увеличение);
- головные боли и другие проявлении вегето-сосудистой дистонии, как следствия гормонального дисбаланса;
- избыточное оволосение, иногда – мо мужскому типу (на ногах, руках, животе);
- бессонница;
- появление на коже (чаще всего живота, поясницы, бедер, плеч и груди) полос растяжения – стрий;
- недомогание, быстрая утомляемость;
- раздражительность, резкие перепады настроения.
Диагностика
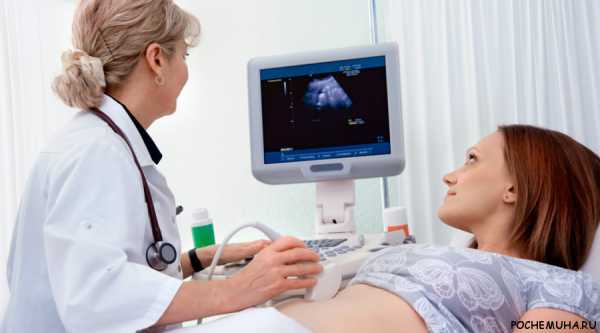
Диагностика железистой гиперплазии необходима для уточнения диагноза. Главная задача врача в этом случае – достоверно установить доброкачественную природу заболевания. Для этого используется гистероскопия – осмотр полости матки и диагностическое выскабливание с последующим микроскопическим исследованием материала.
Достаточно информативным оказывается анализ, определяющий уровень половых гормонов в крови. Его минус в том, что он не обладает никакой специфичностью: гиперплазия эндометрия всегда сопровождается расстройствами гормонального баланса, но эти расстройства не могут служить доказательством наличии гиперплазии.
В случае с появлением полипов определенную информацию может дать УЗИ органов малого таза. Это исследование важно также в проведении дифференциальной диагностики между полипами, возникшими на фоне гиперплазии эндометрия и миоматозными узлами матки.
к оглавлению ↑Лечение гиперплазии эндометрия
Железистая гиперплазия нередко сопровождается появлением неотложных состояний, связанных с массивными маточными кровотечениями. Если больная поступает в больницу в таком состоянии, то первым этапом лечения обязательно должна быть остановка кровотечения и восстановление объема циркулирующей крови.
В дальнейшем лечение железистой гиперплазии проводится по нескольким направлениям:
- гормональная терапия для остановки роста эндометрия;
- борьба с анемией;
- нормализация работы половых желез.
- Гормональная терапия проводится гестагенами и аналогами гонадотропин-рилизинг фактора (гормона гипоталамуса, которые ответственен за выработку половых гормонов), которые назначаются на длительный срок, от 3 до 6 месяцев, в определенные дни менструального цикла или непрерывно.
- Прекращение постоянных кровотечений хорошо достигается за счет назначения гормональных препаратов (это т.н. гормональный гемостаз). В случае, если этот метод лечения оказывается неэффективным, проводят лечебное выскабливание полости матки и назначение средств, которые повышают тонус ее стенок, тем самым пережимая кровоточащие сосуды. Для лечения анемии применяются препараты железа, в случае массивной кровопотери – препараты крови и кровезамещающие растворы.
- Для восстановления нормального менструального цикла используются препараты, которые могут вызвать овуляцию. Установившаяся овуляция, которая происходит самостоятельно на протяжении 4 месяцев, является критерием эффективности лечения. Если же возраст пациентки близок к менопаузальному, вызывается искусственная менопауза.
В ряде случаев оказывается необходимым применение оперативного лечения (удаления матки). Такой метод применяется в том случае, если консервативная терапия не дает эффекта после 3 месяцев приема препаратов, при большом количестве полипов на эндометрии и, кроме того, у женщин в периоде менопаузы при тяжелом течении заболевания.
к оглавлению ↑Железистая гиперплазия эндометрия и беременность
По сути, беременность не может возникнуть на фоне существующей гиперплазии эндометрия, или даже на фоне лечения этого заболевания. Дело в том, что эта патология изменяет эндометрий настолько, что он теряет свою функцию и способность создавать нормальные условия для имплантации яйцеклетки, равно как и для дальнейшего развития плода.
Как правило, беременность возможна только через 1-1.5 года после проведенного гормонального лечения. Более того, беременность эта будет искусственной (например, путем экстракорпорального оплодотворения), поскольку вероятность нормального естественного зачатия после лечения железистой гиперплазии эндометрия крайне мала.
В итоге, даже если говорить о редчайших случаях возникновения беременности на фоне железистой гиперплазии эндометрия или после нее, можно однозначно сказать: сохранять такую беременность нельзя. В случае, если она возникла, рациональнее всего прервать ее, в остальных же случаях – постараться избегать ее, используя все доступные методы контрацепции. Нормальной беременность в таких условиях быть не может по определению: она всегда будет сопряжена с риском возникновения у плода врожденных аномалий развития.
Что такое железистая гиперплазия эндометрия?
Железистая гиперплазия эндометрия — это патологическое нарушение структуры тканей слизистого слоя матки, вызванное избыточным ростом железистых клеток и ведущее к наращиванию их объема и изменению строения. Процесс сопровождается утолщением тканей внутренней поверхности матки. В нормальном состоянии железы эндометрия похожи на прямые вертикальные полосы, а при наличии заболевания становятся извилистыми и сливаются друг с другом.

Во время месячных происходит отторжение тканей эндометрия, восстанавливающихся к следующему циклу, чтобы в случае оплодотворения у зародыша была возможность закрепиться на стенках детского места. Усиленное разрастание клеток слизистых тканей ведет к значительному увеличению объема матки, затрудняющему гемодинамику в ней. Этот процесс получил называние гиперплазии эндометрия.
Что вызывает заболевание?
Причины могут быть различны:
- гормональный сбой и возрастной критерий;
- генитальные заболевания и половые инфекции;
- общие заболевания;
- аборты и хирургические вмешательства.
Ведущим обстоятельством развития железистой гиперплазии служит сбой в выработке гормонов (нехватка прогестерона и переизбыток эстрогена).
Он может произойти вне зависимости от возраста, но чаще развивается в переходные фазы формирования организма женщины: пубертатном и климактерическом периодах.
Вызывают изменения в эндометрии и различные заболевания мочеполовой системы:
- поликистоз и опухоль яичников;
- дисфункции яичников;
- миома матки;
- эндометрит и эндометриоз.
Инфекции половых органов провоцируют разрастание слизистого слоя матки и усугубляют положение. При недостаточном лечении воспалительных процессов в женских половых органах гиперплазия наступает со стопроцентной вероятностью.
К факторам риска появления железистой гиперплазии можно отнести наличие у женщины следующих патологий:
- избыточной полноты;
- недостаточной выработки инсулина;
- опухоли гранулезных клеток;
- повышенного артериального давления;
- доброкачественной опухоли молочной железы;
- сбоя в функционировании эндокринной системы;
- разлада в работе печени и почек.
Жертвами этого заболевания могут стать женщины, делавшие многочисленные аборты, диагностические выскабливания и гинекологические операции. Резкое прекращение курса гормональной контрацепции, поздняя менопауза и отсутствие родов также провоцируют развитие болезни.
Вернуться к оглавлению
Симптомы этой патологии не всегда явно выражены, поэтому их часто принимают за проявления миомы матки. Тем не менее можно выделить основные сигналы болезни. Возникают маточные кровотечения различного характера: патологические, не связанные с менструальным циклом; обильные и продолжительные месячные; менструации без овуляции, ведущие к бесплодию; мажущие выделения у женщин климактерического возраста; обильные кровотечения со сгустками у подростков. На фоне большой потери крови возникают железодефицитная анемия, боли внизу живота, головокружение и слабость.
По толщине, строению и присутствию аномалий железистую гиперплазию можно разделить на простую и комплексную.
К простому типу относятся железистая и железисто кистозная, а в комплексную входят очаговая и атипичная (аденоматозная) гиперплазии.
Простая железистая гиперплазия эндометрия выражается в численном и размерном приросте железистых клеток, происходящем без аномальных изменений в строении. Очертания и месторасположение клеток желез при таком типе гиперплазии могут быть различными. Четкость границ между основным и функциональным слоями стирается, но граница между мышечным слоем матки и слизистой оболочкой, покрывающей ее, остается неизменной. Перерастание такого типа гиперплазии в раковую опухоль практически невозможно и происходит в одном случае из ста.
Железисто-кистозная гиперплазия эндометрия — вторая стадия аномальных модификаций слизистого слоя детского места. Внутри матки формируются кисты — небольшие каверны, наполненные жидкостью, которая содержит избыток эстрогенов.
Это вызвано неспособностью клеток эндометрия усваивать избыточное число гормонов и выдавливанием его в пространство между клетками. Кистевидные или древовидные аномалии развиваются в функциональном слое эндометрия.
Очаговая железистая гиперплазия возникает на дне и в уголках матки, которые в нормальном состоянии имеют чуть большую толщину внутренней слизистой оболочки. В таких частях происходит разрастание не только покровных и железистых слоев эндометрия, но и расположенных ниже тканей, что и приводит к образованию полипов. Остальная поверхность матки сильным изменениям не подвергается. К сожалению, такой вид патологии может перерастать в онкологические заболевания.
Атипическая железистая гиперплазия выражается в трансформации строения клеток и возникновении чрезмерного разрастания тканей с уменьшением числа соединительных клеток и наличием в них различных по величине и форме ядер. Такой тип болезни еще называют аденоматозной гиперплазией, для которой свойственно возникновение участка матки с аномальным строением слизистой прослойки. Патология может возникнуть как в основном, так и в функциональном слоях. В наиболее сложных случаях затрагивает оба слоя.
Атипическая форма болезни является состоянием, предшествующим появлению злокачественных новообразований. В десяти случаях из ста аденоматоз заканчивается раком слизистой оболочки детского места.
Вернуться к оглавлению
Если пациентке была диагностирована железистая гиперплазия, ей нужно сдать анализы, чтобы определить соотношение уровня эстрогена и прогестерона, а также содержание гормонов щитовидной железы и надпочечников в крови.
Лечение проводят различными методами:
- оперативными;
- консервативными;
- общеукрепляющей терапией.
Оперативный способ терапии заключается в хирургическом извлечении патологически измененных фрагментов слизистого слоя при помощи чистки внутренней полости матки — гистероскопии. Этот метод используется, если пациентка находится в репродуктивном или климактерическом возрасте, при наличии обильных кровотечений или полипов внутри матки.
Образцы тканей с патологическими изменениями отдают в лабораторию на гистологическое изучение, проанализировав результаты которого, гинеколог может назначить консервативное лечение.
Консервативные методы терапии включают в себя прием гормональных средств как в виде оральных комбинированных противозачаточных средств, так и в виде чистых препаратов с прогестероном, снижающих выработку собственных гормонов яичниками.
Врач может установить внутриматочную спираль, содержащую гестагены, однако побочным действием этого способа может быть возникновение кровотечений в течение полугода.
Наиболее действенным методом лечения, назначаемым женщинам во время менопаузы и после достижения тридцатипятилетнего возраста, является применение препаратов «Золадекс» и «Бусерелин». При их использовании могут возникать обильное потоотделение и волнообразные приступы жара.
В качестве общеукрепляющих мероприятий можно использовать комплексы витаминов и минералов, железосодержащие медикаменты для предотвращения анемии, успокоительные настойки валерианы, пиона и пустырника. Лечащий врач при необходимости назначает иглотерапию или электрофорез. Диета и оздоровительная физкультура помогают сбросить лишний вес и повышают эффективность лечения.
По окончании курса терапии нужно помнить, что, если не прислушиваться к советам врача, не посещать консультации гинеколога и эндокринолога, а также не следить за собственным весом и рационом, может наступить рецидив заболевания.
Оцените статью:
(Нет голосов) Загрузка...Железистая гиперплазия эндометрия
- Маточные кровотечения (часто после задержки менструации или в межменструальный период).
- Нарушение менструального цикла (длительное отсутствие менструаций, задержки менструаций, обильные длительные менструации со сгустками).
- Общая слабость, недомогание, быстрая утомляемость, бледность кожных покровов – признаки анемии, появляющиеся в результате кровопотери.
- Бесплодие.
- Тянущие боли внизу живота и в поясничной области.
- Возможно бессимптомное течение.
- Гормональные нарушения (повышенное содержание эстрогенов или дефицит прогестерона, например, при синдроме поликистозных яичников, опухолях яичников и матки, дисфункции яичников и т.д.).
- Климакс — физиологический (естественный) процесс угасания функции яичников, как правило, сопровождающийся гормональным дисбалансом (нарушением соотношения женских половых гормонов).
- Нарушения обмена веществ (сахарный диабет, ожирение).
- Оперативные вмешательства на органах репродуктивной системы (матке, яичниках).
- Артериальная гипертензия, заболевания печени, надпочечников и щитовидной железы, которые ведут к нарушению гормонального фона и обмена веществ.
LookMedBook напоминает: чем раньше Вы обратитесь за помощью к специалисту, тем больше шансов сохранить здоровье и снизить риск развития осложнений:
- Анализ анамнеза заболевания и жалоб (когда появились маточные кровотечения, как долго они длятся, как часто возникают, чем сопровождаются и т.д.).
- Анализ акушерско-гинекологического анамнеза (перенесенные гинекологические заболевания, операции, заболевания, передающиеся половым путем, беременности, их исходы и т.д.).
- Анализ менструальной функции (в каком возрасте начались первые менструации, длительность и регулярность цикла, обильность и болезненность менструаций и т.д.).
- Гинекологический осмотр с обязательным бимануальным (двуручным) влагалищным исследованием (гинеколог двумя руками на ощупь (пальпаторно) определяет размеры матки, яичников, шейки матки, их соотношение, состояние связочного аппарата матки и области придатков, их подвижность, болезненность и пр.).
- Ультразвуковое исследование органов малого таза.
- Микроскопия гинекологического мазка.
- Определение уровня гормонов в крови в 1 и 2 фазу менструального цикла (ФСГ, ЛГ, эстрадиол, прогестерон, пролактин, тестостерон, ДГА-S, 17-ОН-прогестерон, глобулин, связывающий половые гормоны).
- Раздельное диагностическое выскабливание полости матки и цервикального канала с последующим гистологическим исследованием (изучение структуры ткани под увеличением) полученного материала.
- Лечебно-диагностическая лапароскопия (через несколько небольших разрезов в передней брюшной стенке вводится специальный оптический прибор ( лапароскоп), с помощью которого производится непосредственный осмотр органов малого таза и брюшной полости, и при выявлении патологии производятся лечебные манипуляции).
- Гистероскопия (осмотр полости матки специальным оптическим прибором) и биопсия эндометрия (взятие участка эндометрия специальным инструментом) с последующим его гистологическим исследованием.
- Определение уровня онкомаркеров в крови (веществ, которые выделяют опухоли) - СА 125, СА 15-3.
- Хирургическое: удаление патологически измененного участка слизистой (выскабливание полости матки).
- Консервативное:
- гормональная терапия – прием оральных гормональных контрацептивов с лечебной целью, чистых гестагенов (препаратов прогестерона), препаратов, снижающих выработку яичниками половых гормонов;
- общеукрепляющая терапия (прием витаминно-минеральных комплексов, препаратов железа и т.д.);
- физиотерапия (электрофорез, иглорефлексотерапия и пр.).
- Своевременное и достаточное лечение инфекционно-воспалительных заболеваний органов малого таза.
- Отказ от вредных привычек.
- Здоровый образ жизни (регулярные физические нагрузки, здоровое питание с исключением жирной, копченой и консервированной пищи, соли и т.д.).
- Соблюдение правил личной гигиены.
- Рациональный выбор метода контрацепции.
- Соблюдение схемы приема гормональных препаратов.
- Исключение абортов.
- Регулярное посещение гинеколога (2 раза в год).
- Своевременное лечение заболеваний щитовидной железы, надпочечников, печени, контроль уровня глюкозы в крови при диабете, снижение давления при гипертонии.
Железистая гиперплазия эндометрия лечение
 «Золотым стандартом» в лечении железистой гиперплазии эндометрия у пациенток разного возраста служит назначение синтетических прогестинов.
«Золотым стандартом» в лечении железистой гиперплазии эндометрия у пациенток разного возраста служит назначение синтетических прогестинов.
Применение синтетических прогестинов вызывает секреторную трансформацию железистой гиперплазии (включая атипическую гиперплазию), завершающуюся «секреторным истощением» и переходом слизистой оболочки в атрофическое состояние. Подобный эффект прогестинов обусловливает и прекращение маточных кровотечений.
Эффективность прогестинотерапии в устранении гиперпластических изменений эндометрия довольно высока и составляет по данным разных авторов 55–82% излечений. Морфологическим признаком прогестинового влияния на гиперплазированный эндометрий служит его состояние, описываемое как «железистая регрессия».
Последняя описывается как феномен выраженной секреторной трансформации желез, сопровождаемой уменьшением их числа и размеров, уплощением эпителиальной выстилки и атрофией.
В строме могут наблюдаться децидуаподобные изменения. Такова развернутая морфологическая картина изменений эндометрия при постоянном приеме средних и высоких доз препаратов в конце лечения длительностью 6–8 недель.
Эффект прогестинов.
На клеточном уровне эффект прогестинов выражается в подавлении митозов и синтеза РНК (стимулируемые эстрогенами), а также снижении уровней цитоплазматических и ядерных рецепторов к эстрадиолу и прогестерону. Содержание ферментов — 17-β-эстрадиол- и 20-α-дигидропрогестин-дегидрогеназы — имеет тенденцию к снижению.
На системном уровне высокие дозы прогестинов (например, Медроксипрогестерона ацетат) подавляют активность гипоталамо-гипофизарного комплекса, что проявляется снижением секреции ФСГ и особенно ЛГ, и как результат развивается снижение эстрогенного фона в организме пациентки.
Другим важным обстоятельством, которое следует учитывать при назначении прогестинов, служит тот факт, что прогестерон сам по себе способен связываться не только со своим рецептором и таким путем проявлять специфический гормональный эффект, но может, в меньшей степени, соединяться и с другими стероидными рецепторами, блокируя их, что проявляется антиэстрогенным, антиандрогенным и антиминералокортикоидным эффектами.
Можно полагать, что такой способностью к связыванию с широким спектром стероидных рецепторов обладают и синтетические прогестины, производные молекулы прогестерона и нортестостерона. Отсюда следует, что помимо специфического гормонального эффекта у этих соединений, как и у прогестерона, могут наблюдаться признаки влияний, обусловленных таким «неспецифическим» связыванием стероида с рецептором.
Этим свойством молекулы прогестинов может быть объяснен тера певтический эффект прогестинов, обусловленный не только их потенциалом, реализуемым через связывание со «своим» рецептором, но и активностью их молекулы по отношению к другим лигандам. Тем не менее, благодаря высокому аффинитету молекулы прогестинов к рецепторному белку прогестерона, доминирующим влиянием этих препаратов на ткани-мишени будет прогестероновый эффект.
Так, например, при лечении недостаточности лютеиновой фазы менструального цикла, проявляемой вторичной аменореей, или нарушением ритма менструального цикла, сочетающегося с маточным кровотечением, положительного лечебного эффекта можно достичь назначением любого прогестина. Однако предпочтение следует отдать препарату с высокой избирательной прогестиновой активностью и не обладающему другими параллельными эффектами.
В клинических ситуациях, когда требуется создать выраженное противодействие эстрогенному влиянию и обеспечить регресс железистой гиперплазии эндометрия, выбираются прогестины с высокой антиэстрогенной активностью. При необходимости подавить овуляцию выбираются прогестины с высокой антигонадотропной активностью. Обычно молекулы прогестинов с высокой потенцией подавлять секрецию гонадотропинов одновременно обладают и выраженными антиэстрогенными свойствами. Если в клинической картине, помимо высокого эстрогенного фона, имеются признаки гиперандрогении, то показано назначение прогестинов, обладающих антиандрогенным эффектом.
С учетом этих соображений важно подчеркнуть, что, например, компенсировать недостаточность желтого тела может любой прогестин, но для полностью адекватной терапии следует выбирать препарат, могущий, помимо основного эффекта, смягчить проявления сопутствующих гормональных нарушений (гиперандрогения, мастодиния и пр.).
Гормонотерапия гиперпластических процессов.
Гормонотерапия гиперпластических процессов в эндометрии и обусловленных ими маточных кровотечений проводится как патогенетическое воздействие, в основе которого лежит создание выраженного антиэстрогенного влияния на эндометрий в виде снижения пролиферативной активности эпителия желез, развития секреторной трансформации слизистой оболочки, появлении в ней различной степени выраженности атрофических изменений, что приводит к остановке маточного кровотечения. Одновременно такое лечебное воздействие ингибирует активность гипоталамо-гипофизарного комплекса, вызывая подавление гонадотропной активности, снижение стероидогенеза в яичниках и, как следствие, снижение эстрогенного фона в организме пациентки.
При обнаружении патологических процессов в полости матки (подслизистые узлы миомы, полипы), а также в придатках матки (цистаденомы, кисты яичников, длительно существующие пиосальпингсы) в первую очередь решается вопрос о хирургическом лечении этой патологии. Последнее является непременным условием успешной гормональной терапии гиперменструального синдрома, проводимого на втором этапе у этих больных.
Такая тактика считается «классической» и вполне оправдала себя. Вместе с тем следует учитывать и тот факт, что с появлением высокоактивных прогестинов (левоноргестрел или его комбинация с этинилэстрадиолом) некоторые позиции в этой тактике могут пересматриваться, в частности сужение показаний к хирургическому вмешательству. Например, при наличии мелких субмукозных узлов миомы, небольших одиночных полипов в слизистой оболочке стало возможным проведение гормонотерапии этими препаратами в циклической схеме или в постоянном режиме.
Читайте также: Шумы в области сердца - эхокардиографическое исследованиеПри сохраняющемся кровомазании возможно увеличение суточной дозы до 2 или даже до 3 таблеток, с постепенным снижением дозы по достижении клинического эффекта. Продолжительность лечения определяется индивидуальными особенностями, но не должна быть менее 6 месяцев. Такой подход оправдан у пациенток с осложненным соматическим статусом, у которых проведение хирургического вмешательства может быть связано с риском серьезных осложнений.
Современные лекарственные формы гормональных препаратов.
Современные лекарственные формы гормональных препаратов позволяют проводить как системное лечение прогестинами, принимаемыми внутрь, так и местное воздействие (Левоноргестрелом), когда препарат доставляется непосредственное в полость матки (внутриматочный контрацептив «Мирена»).
При системном воздействии, с целью антиэстрогенного влияния на слизистую оболочку полости матки применяются препараты с прогестиновой активностью, например Дюфастон, Медроксипрогестерона ацетат (МПА) или высокодозные стероидные противозачаточные средства (Нон-овлон, Овидон, Микрогинон).
Возможность обеспечения выраженного антиэстрогенного влияния на эндометрий, приводящего к прекращению маточного кровотечения, секреторной трансформации слизистой оболочки и появлению в ней признаков атрофии при достаточно продолжительном лечении — все это, а также хорошая переносимость препаратов позволяет охарактеризовать лечение прогестинами как метод выбора.
После прекращения маточного кровотечения (выделений) необходимо сформировать правильный ритм менструального цикла. При этом следует стремиться восстановить обычную для данной пациентки продолжительность межменструального интервала и уменьшить длительность и величину кровопотери во время менструации. Последнее достигается присоединением эстрогенов к терапии прогестинами или назначением комбинированных (эстроген-прогестиновых) противозачаточных препаратов.
Применение эстрогенов в сочетании с прогестинами.
Применение эстрогенов в сочетании с прогестинами в прерывистом (циклическом) режиме не противоречит общему принципу лечения, заключающемуся в создании антиэстрогенного влияния на эндометрий. Это положение обосновывается тем, что применяемые дозы эстрогенов в прерывистом режиме не вызывают значительной пролиферации элементов эндометрия и их влияние сбалансировано прогестином. При этом следует иметь в виду ряд положительных свойств эстрогенов, таких как способность повышать чувствительность эндометрия к прогестинам, подавлятьсекрецию гонадотропинов и снижать интенсивность строидогенеза в яичниках. С помощью эстрогенов удается восстановить правильный ритм менструального цикла, что не всегда достигается при изолированном применении прогестинов.
Гормональное лечение железистой гиперплазии эндометрия.
Гормональное лечение железистой гиперплазии эндометрия и обусловленной ею мено-метроррагии в репродуктивном периоде складывается из двух этапов:
1) остановка маточного кровотечения;
2) формирование правильного ритма менструального цикла и предупреждение кровотечения.
Остановка маточного кровотечения.
Если маточное кровотечение прекратилось после диагностического выскабливания слизистой оболочки матки, то лечение начинают со 2–3-го дня по одной из схем для формирования правильного менструального цикла. При продолжающемся кровотечении прибегают к гормональному гемостазу.
С этой целью введение эстрогенов является наиболее эффективным и быстрым методом воздействия, превосходящим по результатам лечение прогестинами или андрогенами.
Лечение следует начинать с внутримышечного введения эстрогенов или, что удобнее (отсутствие инъекций), с приема таблетированных стероидных противозачаточных препаратов (Микрогинон, Ригевидон) внутрь, по одной из приводимых схем. Пусть читателю не покажется применение синэстрола слишком архаичным методом лечения. При всем том этот препарат действует безотказно:
◆ Синэстрол, 2% масляный раствор, по 1 мл (20 мг), внутримышечно, ежедневно, в теплом виде. Введение продолжается до полной остановки кровотечения, что обычно требует 3–4 инъекций.
После остановки кровотечения на следующий день вводится оксипрогестерона капронат — 12,5%, 2 мл (250 мг) внутримышечно.
При выраженном маточном кровотечении с целью гемостаза возможно введение:
◆ Масляного «коктейля»: Синэстрол 2% — 2 мл + Оксипрогестерона капронат — 2 мл + Тестостерона пропионат 5% раствор — 2 мл, в одном шприце, внутримышечно, однократно. Или назначение Микрогинона (Овидон, Ригевидон), по 2–3 таб. в день, внутрь, до полного прекращения кровотечения, которое останавливается через 48–72 часа, после чего доза препарата постепенно снижается до 1 таб. в день и лечение продолжается 21 день, считая от начала приема препарата, или более продолжительное время, если необходимо состояние аменореи (например, для достижения компенсации анемии).
Формирование правильного менструального цикла.
Для формирования правильного менструального цикла после остановки маточного кровотечения или с любого дня аменореи применяются:
◆ эстроген-прогестиновые противозачаточные препараты монофазного типа, по контрацептивной (циклической) схеме. Первые циклы после остановки кровотечения могут быть нестабильными, что может потребовать увеличения суточной дозы препарата до 2–3 таблеток в сутки, в случае появления кровянистых выделений. У этих пациенток целесообразно применять препараты монофазного типа (Микрогинон, Овидон), позволяющие учитывать и легко менять суточную дозу в первый цикл лечения в зависимости от гемостатического эффекта (прекращение кровомазания). После перерыва в приеме препарата (3–5 дней) и с наступлением нового менструального цикла, лечение проводится по контрацептивной схеме, длительностью не менее 6–8 циклов.
Читайте также: Болезнь лепра - этиопатогенез, проявления, лечение В последующие циклы лечения (с 4–6-го цикла) возможно применение низкодозных контрацептивов (Жанин, Логест, Ярина), продлив общую продолжительность приема (при хорошей переносимости препарата) до 2 лет.
В последующие циклы лечения (с 4–6-го цикла) возможно применение низкодозных контрацептивов (Жанин, Логест, Ярина), продлив общую продолжительность приема (при хорошей переносимости препарата) до 2 лет.
Такая тактика гормонотерапии обеспечивает сохранение правильного (искусственного) менструального цикла и предупреждает развитие рецидива железистой гиперплазии эндометрия.
◆ При плохой переносимости ОК (что часто обусловлено синтетическим эстрогеном этинилэстрадиолом, входящим в состав всех ОК) возможно изолированное применение прогестинов.
С этой целью назначается Норколут по 5 мг в день или Дуфастон (5–10 мг в день) с 10-го дня цикла (или сразу же после диагностического выскабливания слизистой оболочки полости матки) в течение 20 дней. Менструация наступает через 2–4 дня после отмены прогестинов. С 10-го дня нового цикла лечение возобновляется и проводится не менее года.
Для лучшей переносимости гормональных препаратов, принимаемых внутрь, дополнительно назначаются желчегонные средства, витамин Е (200–300 мг в день), панкреатин или комплекс ферментов (Фестал).
◆ Для восстановления овуляторных циклов при хронической ановуляции, с целью наступления запланированной беременности (что также может рассматриваться как мера профилактики рецидива ЖГЭ) возможно применение нескольких схем гормональной стимуляции овуляции.
Ключевыми методами стимуляции овуляции в этом подходе служат человеческие мочевые гонадотропины (Менопур, Меногон с ФСГ-активностью; Хорагон, Прегнил, Профази с ЛГ-активностью) или рекомбинантные гонадотропины (Пурегон, Гонал-Ф с ФСГ-активностью и Лютропин-α с ЛГ-активностью); антиэстрогены (кломифена цитрат) и аналоги гонадотропин-рилизинг гормона (агонисты Гн-Рг и антагонисты Гн-Рг).
С помощью этих препаратов осуществляется проведение контролируемой индукции овуляции в циклах естественной фертильности.
К настоящему времени разработано много методик индивидуализированных количественных воздействия для стимуляции овуляции, которые составляют предмет вспомогательной репродуктивной технологии. Здесь же мы приводим несколько несложных схем стимуляции овуляции, которые могут применяться на первом этапе лечения.
Схемы стимуляции овуляции.
Для достижения этой цели на предварительном этапе важно определить имеющиеся резервы яичников для успешной стимуляции фолликулогенеза после продолжительной терапии прогестинами. Показателями хорошего овариального резерва служат возраст пациентки до 30 лет, уровень ФСГ на 2–3-й день менструального цикла 3–10 МЕ/л, число антральных фолликулов до 10 мм в диаметре равное 10 в каждом яичнике, объем яичника по данным УЗИ более 12 см3 (Назаренко Т. А., 2008).
Все схемы стимуляции овуляции обычно начинаются со 2–3-го дня менструального цикла. Преимущественно применяются комбинированные схемы стимуляции, с последовательным назначением препаратов с разными механизмами действия, так как сочетание препаратов дает более высокие результаты, чем монотерапия.
- Кломифена цитрат назначается по 50 мг 2 раза в день, со 2-го дня цикла, внутрь, 5 дней. Проводится мониторинг роста примордиального фолликула под влиянием лечения (УЗИ). По достижении доминантного фолликула размеров 18–20 мм вводится триггер овуляции — гормон с ЛГ активностью, Хорионический гонадотропин в дозе 5000–10 000 ЕД/сут на 14-й и 16-й дни цикла.
С 16-го дня цикла назначается дуфастон, 10 мг в день, в течение 12 дней. Проводится четыре цикла стимуляции.
- Кломифена цитрат, по 50 мг 2 раза в день, внутрь, со 2-го дня цикла, 5 дней. С 5-го дня менструального цикла Меногон, по 150 ЕД (ФСГ+ЛГ) в течение 7 дней, внутримышечно. С 12-го дня цикла дважды вводится триггер овуляции Прегнил, по 5000 ед, на 12 и 14-й дни цикла. С 14-го дня назначается дуфастон, по 10 мг в день, 12 дней. Проводится четыре цикла лечения.
При проведении стимуляции овуляции необходимо осуществлять мониторирование индуцированного цикла. Главную роль в мониторировании индуцированного цикла играют УЗИ роста фолликула и увеличения толщины эндометрия (увеличение фолликула более 18 мм и толщины эндометрия до 14-16 мм) (Назаренко Т. А., 2008).
В случае неуспеха стимуляции кломифеном можно прибегнуть к более сложным комбинированным методам стимуляции (аналоги Гн-Рг), используемым в репродуктивных технологиях.
Так, в современной репродуктивной технологии разработаны методики применения как агонистов гонадотропин-РГ (аг-Гн-РГ), так и антагонистов гонадотропин-РГ (ант-Гн-РГ) в индукции овуляции. Обсуждаются преимущества каждой из схем. Но многие специалисты сходятся во мнениях в одном: каждая схема стимуляции должна быть предельно индивидуализирована с учетом возраста пациентки и состояния резерва яичников.
Применительно к пациенткам с ГС представляется, все-таки, более адекватными схемы с применением ант-Гн-РГ. Ниже приводится одна из их числа:
- Со 2-го дня по 11 день цикла, включительно, подкожно вводится 150 ЕД Менопура ( 75 ед ФСГ + 75 ед ЛГ).
- С 7-го дня по 11 день цикла (всего 5 дней) вводится Оргалутран, по 0,25 мг, подкожно, ежедневно.
- На 12 или 13 дни менструального цикла, при достижении размеров доминантного фолликула не менее 14 мм (по данным чХГ УЗИ яичников) вводится триггер овуляции – (Хорионический гонадотропин), в дозе 5000 еД, внутримышечно, однократно.
Проводится 3 цикла стимуляции. Наступление беременности, с ее естественным и выраженным прогестиновым влиянием рассматривается как благоприятный естественный фактор, закрепляющий успех предыдущего лечения.
Альтернативой системному лечению железистой гиперплазии эндометрия прогестинами служит местное воздействие Левонор-гестрелом, которое осуществляется путем внутриматочного введения контрацептива «Мирена».
Выделение Левоноргестрела из контрацептива Мирена позволяет создать высокую локальную концентрацию прогестина в эндоме-трии (468–1568 нг/г), превышающую таковую в плазме крови в несколько тысяч раз (0,15–0,2 нг/г). В этих условиях эндометрий становится не чувствительным к циркулирующему в крови эстрадиолу, так как высокая концентрация прогестина в ткани эндометрия угнетает синтез рецепторов к эстрадиолу. В результате наблюдается выраженный антипролиферативный эффект в слизистой оболочке полости матки.
В обычных условиях пролиферирующий и секреторный эндометрий продуцирует множество высокоактивных соединений (простагландины, эстроген-индуцированные факторы роста и другие биологически активные пептиды). Когда пролиферация эндометрия подавлена прогестинами, продукция этих факторов прекращается.
К настоящему времени в специальной литературе появилось большое число исследований, посвященных изучению морфологических изменений эндометрия при приеме комбинированных стероидных контрацептивов. Интерес исследователей к этому вопросу объяснялся стремлением изучить точный механизм контрацептивного эффекта этих соединений, который частично объяснялся морфологическими изменениями слизистой полости матки под влиянием принимаемых препаратов.
В обобщенной характеристике вызываемых изменений эндометрия под влиянием прогестинов морфологический эффект был обозначен как «желе-зистая регрессия». Основные морфологические признаки этого состояния выражались в псевдодецидуальной реакции стромы, на фоне которой определялось уменьшение числа и размеров же-лез, появлении ранних признаков секреции, которая быстро завершалась секреторным истощением.
Уже к третьему циклу приема препарата эндометрий определялся истонченным, с морфологическими признаками атрофии железистого компонента, сочетавшейся со стромальной реакцией в виде децидуаподобной трансформации стромы или ее фиброзом.
В нашем исследовании, выполненным совместно с Е. Л. Неженцевой и О. Ф. Чепиком (1994), изучались морфолгические изменения эндометрия под влиянием КОК и «чистых» прогестинов (табл. 6.1).
Результаты гормонотерапии больных железистой гиперплазией эндометрия
Лечение проведено у 126 пациенток по поводу железистой гиперплазии эндометрия, осложненной маточным кровотечением. Применявшиеся препараты КОК содержали раз-ное количество эстрогенного и прогестинового компонентов, включая трехфазные КОК, с низким содержанием гормонов, что позволило сделать сравнительную оценку клинического и морфологического эффектов.
Как видно из табл. 6.1, отмечалась высокая частота сочетанного морфологического (устранение железистой гиперплазии эндометрия) и клинического (нормализация менструального цикла) эффектов, у 95 (75,4%) из 126 пролеченных пациенток.
Примечание. Результаты гормонотерапии оценивались после 6–8 циклов лечения по следующим критериям: I — наличие клинического и морфологического эффектов; II — клинический эффект без морфологического; III — морфологическая нормализация эндометрия, отсутствие клинического эффекта; IV — отсутствие клинического и морфологического эффектов.
Состояние эндометрия оценивалось по результатам гистологического исследования соскобов слизистой оболочки, взятых на 20–22-й день менструального цикла.
Нормализация менструального цикла сочеталась с «железистой регрессией» гиперплазии эндометрия одинаково часто у пациенток, получавших трехфазный препарат Тризистон (91,6%) и двухфазный Антеовин (91,0%). Отмечалась меньшая частота клинического и морфологического эффектов у пациенток, которым назначались прогестины без эстрогенного компонента (ацетмепрегенол, норколут) — в 59% наблюдений (р
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе