Для свертывания крови необходимо присутствие
 [Для свертывания крови необходимо присутствие]
[Для свертывания крови необходимо присутствие]
4. Свертывание крови [1976 — — Физиология человека]
Пока кровь течет по неповрежденным кровеносным сосудам, она остается жидкой. Но стоит поранить сосуд, как довольно быстро образуется сгусток. Кровяной сгусток (тромб), словно пробка, закупоривает ранку, кровотечение останавливается, и ранка постепенно заживает. Если бы кровь не свертывалась, то человек мог бы погибнуть от самой маленькой царапины.
Кровь человека, выпущенная из кровеносного сосуда, свертывается в течение 3-4 мин.
Свертывание крови является важной защитной реакцией организма, препятствующей кровопотере и, таким образом, сохраняющей постоянство объема циркулирующей крови.
В основе свертывания крови лежит изменение физико-химического состояния растворенного в плазме крови белка фибриногена. Фибриноген в процессе свертывания крови превращается в нерастворимый фибрин. Фибрин выпадает в виде тонких нитей. Нити фибрина образуют густую мелкоячеистую сеть, в которой задерживаются форменные элементы. Образуется сгусток, или тромб. Постепенно происходит уплотнение кровяного сгустка. Уплотняясь, он стягивает края раны и этим способствует ее заживлению. При уплотнении сгустка из него выдавливается прозрачная желтоватая жидкость — сыворотка. Сыворотка — это плазма крови, из которой удален белок фибриноген. В уплотнении сгустка важная роль принадлежит тромбоцитам, в которых содержится вещество, способствующее сжатию сгустка.
Свертывание крови — сложный процесс. В нем принимают участие соли кальция, находящиеся в плазме крови. Обязательным условием свертывания крови является разрушение кровяных пластинок (тромбоцитов).
Согласно современным представлениям превращение растворенного в плазме крови белка фибриногена в нерастворимый белок фибрин совершается под влиянием фермента тромбина. В крови имеется неактивная форма тромбина — протромбин, который образуется в печени. Протромбин превращается в активный тромбин под влиянием тромбопластина в присутствии солей кальция. Соли кальция есть в плазме крови, а тромбопластина в циркулирующей крови нет. Он образуется при разрушении тромбоцитов или при повреждении других клеток тела. Образование тромбопластина также сложный процесс. Кроме тромбоцитов, в образовании тромбопластина принимают участие еще некоторые белки плазмы крови. Отсутствие в крови некоторых белков резко сказывается на процессе свертывания крови. Если в плазме крови отсутствует один из глобулинов (крупномолекулярных белков), то наступает заболевание гемофилия, или кровоточивость. У людей, страдающих гемофилией, резко понижена свертываемость крови. Даже небольшое ранение может вызвать у них опасное кровотечение.
Чаще гемофилией болеют мужчины. Это заболевание передается по наследству.
Процесс свертывания крови регулируется нервной системой и гормонами желез внутренней секреции. Он может ускоряться и замедляться.
Если при кровотечениях важно, чтобы кровь свертывалась, то не менее важно, чтобы она, циркулируя в кровеносной системе, оставалась жидкой, не свертывалась.
В организме образуются вещества, препятствующие свертыванию крови. Такими свойствами обладает гепарин, находящийся в клетках легких и печени. В сыворотке крови обнаружен белок фибринолизин — фермент, растворяющий образовавшийся фибрин. В крови, таким образом, одновременно имеются две системы: свертывающая и противосвертывающая. При определенном равновесии этих систем кровь внутри сосудов не свертывается. При ранениях и некоторых заболеваниях равновесие нарушается, что приводит к свертыванию крови. Тормозят свертывание крови соли лимонной и щавелевой кислот, осаждая необходимые для свертывания соли кальция. В шейных железах медицинских пиявок образуется гирудин, обладающий мощным противосвертывающим действием. Противосвертывающие вещества широко применяют в медицине.
Как осуществляется свертывание крови?
Как осуществляется свертывание крови?
Свертывание крови — сложный процесс. В нем участвует 13 факторов, имеющихся в плазме крови, а также вещества, освобождающиеся при разрушении тромбоцитов и при повреждении тканей.
Свертывание крови происходит в несколько стадий:
1. В первой стадии из поврежденных тромбоцитов и клеток тканей выделяется предшественник тромбопластина. Это вещество, взаимодействуя с белками плазмы крови, преобразуется в активный тромбопластин. Для образования тромбопластина необходимо присутствие Са2+, а также белков плазмы, в частности антигемолитического фактора Если в крови антигемолитический фактор отсутствует, кровь не свертывается. Это состояние получило название гемофилии.
2. Во второй стадии белок плазмы крови протромбин при участии тромбопластина превращается в активный фермент тромбин.
3. Под действием тромбина растворимый в плазме белок фибриноген превращается в нерастворимый фибрин. Фибрин образует сгусток,состоящий из сплетений тончайших волоконец. В их сети оседают клетки крови, образуя тромб.
Свертывание крови предохраняет организм от кровопотерь.
На этой странице искали :
- для осуществления свертывания крови необходимы вещества
- для свертывания крови необходимо присутствие
- для свертывания крови необходимы вещества
Сохрани к себе на стену!
Для свертывания крови необходимо присутствие железа йода кальция или калия
СИСТЕМА СВЕРТЫВАНИЯ КРОВИ
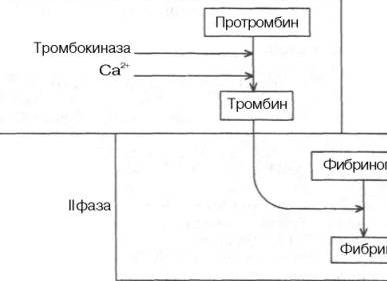
Способность крови свертываться с образованием сгустка в просвете кровеносных сосудов при их повреждении была известна с незапамятных времен. Создание первой научной теории свертывания крови в 1872 г. принадлежит А.А. Шмидту. Первоначально она сводилась к следующему: свертывание крови – ферментативный процесс; для свертывания крови необходимо присутствие трех веществ: фибриногена, фибринопластического вещества и тромбина. В ходе реакции, катализируемой тромбином, первые два вещества, соединяясь между собой, образуют фибрин. Циркулирующая в сосудах кровь не свертывается по причине отсутствия в ней тромбина. В результате дальнейших исследований А.А. Шмидта и его школы,а также Моравица, Гаммарстена, Спиро и др. было установлено, что образование фибрина происходит за счет одного предшественника – фибриногена. Проферментом тромбина является протромбин, для процесса свертывания необходимы тромбокиназа тромбоцитов и ионы кальция. Таким образом, через 20 лет после открытия тромбина была сформулирована классическая ферментативная теория свертывания крови, которая в литературе получила название теории Шмидта–Моравица. Протромбин переходит в активный фермент тромбин под влиянием тромбокиназы, содержащейся в тромбоцитах и освобождающейся из них при разрушении кровяных пластинок, и ионов кальция (I фаза). Затем под влиянием образовавшегося тромбина фибриноген превращается в фибрин (II фаза). Сравнительно простая по своей сути теория Шмидта–Моравица в дальнейшем необычайно усложнилась, обросла новыми сведениями, «превратив» свертывание крови в сложнейший ферментативный процесс.
Современные представления о свертывании крови
При повреждении кровеносного сосуда кровотечение может продолжаться различное время. Если сосуд небольшой, то кровотечение быстро прекращается, происходит гемостаз. Выделяют 4 фазы гемостаза.
Первая фаза– сокращение поврежденного сосуда.
Вторая фаза– образование в месте повреждения рыхлой тромбоцитарной пробки, или белого тромба. Имеющийся в участке повреждения сосуда коллаген служит связующим центром для тромбоцитов. При агрегации тромбоцитов освобождаются вазоактивные амины, например серотонин и адреналин, а также метаболиты простагландинов, например тромбоксан, которые стимулируют сужение сосудов.
Третья фаза– формирование красного тромба (кровяной сгусток).
Четвертая фаза– частичное или полное растворение сгустка.
Различают три типа тромбов, или сгустков. Белый тромб образуется из тромбоцитов и фибрина; в нем относительно мало эритроцитов. Формируется он в местах повреждения сосуда в условиях высокой скорости кровотока (в артериях). Второй вид тромбов – диссеминированные отложения
фибрина в очень мелких сосудах (в капиллярах). Третий вид тромбов – красный тромб. Он состоит из эритроцитов и фибрина. Морфология красного тромба сходна с морфологией сгустков, образующихся в пробирке. Красные тромбы формируются in vivo в областях замедленного кровотока при отсутствии патологических изменений в стенке сосуда или на измененной стенке сосуда вслед за инициирующей тромбоцитарной пробкой.
Установлено, что в процессе свертывания крови участвуют компоненты плазмы, тромбоцитов и ткани, которые называются факторами свертывания крови. Факторы свертывания, связанные с тромбоцитами, принято обозначать арабскими цифрами (1, 2, 3 и т.д.), а факторы свертывания,
находящиеся в плазме крови,– римскими цифрами (I, II, III и т.д.).
Фактор I (фибриноген)– важнейший компонент свертывающей системы крови, так как биологической сущностью процесса свертывания крови является образование фибрина из фибриногена. Фибриноген состоит из 3 пар неидентичных полипептидных цепей, которые связаны между собой дисульфидными связями. Каждая цепь имеет олигосахаридную группу. Соединение между белковой частью и углеводными компонентами осуществляется посредством связи остатка аспарагина с N-ацетилглюкозамином. Общая длина молекулы фибриногена 46 нм, мол. масса 330000–340000. Синтезируется данный белок в печени, концентрация его в плазме кровичеловека составляет 8,2–12,9 мкмоль/л.
Фактор II (протромбин)является одним из основных белков плазмы крови, определяющих свертывание крови. При гидролитическом расщеплении протромбина образуется активный фермент свертывания крови – тромбин . Концентрация протромбина в плазме крови 1,4–2,1 мкмоль/л. Он является гликопротеином, который содержит 11–14% углеводов, включая гексозы, гексозамины и нейраминовую кислоту. По электрофоретической подвижности протромбин относится к α2-глобулинам, имеет мол. массу 68000–70000. Размеры большой и малой осей его молекулы соответственно 11,9 и 3,4 нм. Изоэлектрическая точка очищенного протромбина лежит в пределах рН от 4,2 до 4,4. Синтезируется данный белок в печени, в его синтезе принимает участие витамин К. Одна из специфических особенностей молекулы протромбина – способность связывать 10–12 ионов Са2+ ,при этом наступают конформационные изменения молекулы белка.Превращение протромбина в тромбин связано с резким изменением молекулярной массы белка (с 70000 до 35000). Есть основания считать, что тромбин является большим фрагментом молекулы протромбина.
Фактор III (тканевый фактор, или тканевый тромбопластин)образуетсяпри повреждении тканей. Это комплексное соединение липопротеиновойприроды, отличается очень высокой мол. массой – до 167000000.
Фактор IV (ионы Са2+). Известно, что удаление из крови ионов Са2+(осаждение оксалатом или фторидом натрия), а также перевод ионов Са2+в неионизированное состояние (с помощью цитрата натрия) предупреждает свертывание крови. Следует также помнить, что нормальная скорость свертывания крови обеспечивается лишь оптимальными концентрациями ионов Са2+. Для свертывания крови человека, декальцинированной с помощью ионообменников, оптимальная концентрация ионов Са2+ определена в 1,0–1,2 ммоль/л. Концентрация ионов Са2+ выше и ниже оптимальной обусловливает замедление процесса свертывания. Ионы Са2+ играют важную роль почти на всех фазах (стадиях) свертывания крови: они необходимы для образования активного фактора X и активного тромбопластина тканей, принимают участие в активации проконвертина, образовании тромбина, лабилизации мембран тромбоцитов и в других процессах.
Фактор V (проакцелерин)относится к глобулиновой фракции плазмы крови. Он является предшественником акцелерина (активного фактора). Фактор V синтезируется в печени, поэтому при поражении этого органа может возникнуть недостаточность проакцелерина. Кроме того, существует врожденная недостаточность в крови фактора V, которая носит название парагемофилии и представляет собой одну из разновидностей геморрагических диатезов.
Фактор VII (антифибринолизин, проконвертин)– предшественник конвертина. Механизм образования активного конвертина из проконвертина изучен мало. Биологическая роль фактора VII сводится прежде всего к участию во внешнем пути свертывания крови. Синтезируется фактор VII в печени при участии витамина К. Снижение концентрации проконвертина в крови наблюдается на более ранних стадиях заболевания печени, чем снижение уровня протромбина и проакцелерина.
Фактор VIII (антигемофильный глобулин А)является необходимым компонентом крови для формирования активного фактора X. Он очень лабилен. При хранении цитратной плазмы его активность снижается на 50% за 12 ч при температуре 37°С. Врожденный недостаток фактора VIII
является причиной тяжелого заболевания – гемофилии А – наиболее частой формы коагулопатии.
Фактор IX (антигемофильный глобулин В, Кристмас-фактор) принимает участие в образовании активного фактора X. Геморрагический диатез, вызванный недостаточностью фактора IX в крови, называют гемофилией В. Обычно при дефиците фактора IX геморрагические нарушения носят менее выраженный характер, чем при недостаточности фактора VIII.
Фактор X (фактор Стюарта–Прауэра)назван по фамилиям больных, у которых был впервые обнаружен его недостаток. Он относится к α-глобулинам, имеет мол. массу 87000. Фактор X участвует в образовании тромбина из протромбина. У пациентов с недостатком фактора X увеличено время свертывания крови, нарушена утилизация протромбина. Клинически недостаточность фактора X выражается в кровотечениях, особенно после хирургических вмешательств или травм. Фактор X синтезируется клетками печени; его синтез зависит от содержания витамина К в организме.
Фактор XI (фактор Розенталя)– антигемофильный фактор белковой природы. Недостаточность этого фактора при гемофилии С была открыта в 1953 г. Розенталем. Фактор XI называют также плазменным предшественников тромбопластина.
Фактор XII (фактор Хагемана)участвует в пусковом механизме свертывания крови. Он также стимулирует фибринолитическую активность, кининовую систему и некоторые другие защитные реакции организма. Активация фактора XII происходит прежде всего в результате взаимодействия его с различными «чужеродными» поверхностями: кожей, стеклом, металлом и др. Врожденный недостаток данного белка вызывает заболевание, которое назвали болезнью Хагемана по фамилии первого обследованного больного, страдавшего этой формой нарушения свертывающей функции крови: увеличенное время свертывания крови при отсутствии геморрагии.
Фактор XIII (фибринстабилизирующий фактор)является белком плазмы крови, который стабилизирует образовавшийся фибрин, т.е. участвует в образовании прочных межмолекулярных связей в фибрин-полимере. Мол. масса 330000–350000. Белок состоит из трех полипептидных цепей, каждая из которых имеет мол. массу 110000.
Кроме факторов плазмы крови и тканей, в процессе свертывания крови принимают участие факторы, связанные с тромбоцитами. В настоящее время известно около 10 отдельных факторов тромбоцитов. Приводим некоторые из них.
Фактор 1тромбоцитов представляет собой адсорбированный на поверхности тромбоцитов проакцелерин; с тромбоцитами связано около 5% всего проакцелерина крови.
Фактор 3– один из важнейших компонентов свертывающей системы крови. Вместе с рядом факторов плазмы он необходим для образования тромбина из протромбина.
Фактор 4является антигепариновым фактором, тормозит антитромбо-пластиновое и антитромбиновое действие гепарина. Кроме того, фактор 4 принимает активное участие в механизме агрегации тромбоцитов.
Фактор 8 (тромбостенин)участвует в процессе ретракции фибрина, очень лабилен, обладает АТФазной активностью. Освобождается при склеивании и разрушении тромбоцитов в результате изменения физико-химических свойств поверхностных мембран.
«Внешний» и «внутренний» пути свертывания крови
Свертывание крови может осуществляться с помощью двух механизмов, тесно связанных между собой,– так называемых внешнего и внутреннего путей свертывания (рис. 17.8). Инициация образования сгустка в ответ на повреждение ткани осуществляется по «внешнему» пути свертывания, а формирования красного тромба в области замедленного кровотока или на аномальной сосудистой стенке при отсутствии повреждения ткани – по «внутреннему» пути свертывания. На этапе активации фактора X происходит как бы объединение обоих путей и образуется конечный путь свертывания крови. На каждом из путей последовательно образующиеся ферменты активируют соответствующие зимогены, что приводит к превращению растворимого белка плазмы фибриногена в нерастворимый белок фибрин, который и образует сгусток. Это превращение катализируется протеолитическим ферментом тромбином. В нормальных условиях тромбина в крови нет, он образуется из своего активного зимогена – белка плазмы протромбина. Этот процесс осуществляется протеолитическим ферментом, названным фактором Ха, который также в обычных условиях отсутствует в крови; он образуется при кровопотере из своего зимогена (фактора X). Фактор Ха превращает протромбин в тромбин только в присутствии ионов Са2+ и других факторов свертывания. Таким образом, свертывание крови включает эффективно регулируемую серию превращений неактивных зимогенов в активные ферменты, что в итоге приводит к образованию тромбина и превращению фибриногена в фибрин. Заметим, что «внутренний» путь свертывания крови – медленный процесс, поскольку в нем участвует большое число факторов свертывания. Принято считать, что фактор III, переходящий в плазму крови при повреждении тканей, а также, по-видимому, фактор 3 тромбоцитов создают предпосылки для образования минимального (затравочного) количества тромбина (из протромбина). Этого минимального количества тромбина недостаточно для быстрого превращения фибриногена в фибрин и, следовательно, для свертывания крови. В то же время следы образовавшегося тромбина катализируют превращение проакцелерина и проконвертина в акцелерин (фактор Va) и соответственно в конвертин (фактор VIIa).В результате сложного взаимодействия перечисленных факторов, а также ионов Са2+ происходит образование активного фактора X (фактор Ха). Затем под влиянием комплекса факторов: Ха, Va, 3 и ионов Са2+ (факторVI) – происходит образование тромбина из протромбина. Далее под влиянием фермента тромбина от фибриногена отщепляются 2 пептида А и 2 пептида В (мол. масса пептида А – 2000, а пептида В – 2400).Установлено, что тромбин разрывает пептидную связь аргинин–лизин. После отщепления пептидов, получивших название «фибрин-пептиды», фибриноген превращается в хорошо растворимый в плазме крови фибрин-мономер, который затем быстро полимеризуется в нерастворимый фибрин-полимер. Превращение фибрин-мономера в фибрин-полимер протекает с участием фибринстабилизирующего фактора – фактора XIII в присутствии ионов Са2+. Известно, что вслед за образованием нитей фибрина происходит их сокращение. Имеющиеся в настоящее время данные свидетельствуют, что ретракция кровяного сгустка является процессом, требующим энергии АТФ. Необходим также фактор 8 тромбоцитов (тромбостенин). Последний по своим свойствам напоминает актомиозин мышц и обладает АТФазной активностью. Таковы основные стадии свертывания крови.
ПРОТИВОСВЕРТЫВАЮЩАЯ СИСТЕМА КРОВИ
Кровь в живом организме находится в жидком состоянии, несмотря на наличие очень мощной свертывающей системы. Многочисленные исследования, направленные на выяснение причин и механизмов поддержания крови в жидком состоянии во время циркуляции ее в кровяном русле, позволили в значительной степени выяснить природу противосвертывающей системы крови. Оказалось, что в образовании ее, так же как и в формировании системы свертывания крови, участвует ряд факторов плазмы крови, тромбоцитов и тканей. К ним относят различные антикоагулянты: антитромбопластины, антитромбины, а также фибринолитическую систему крови. Считается, что в организме существуют специфические ингибиторы для каждого фактора свертывания крови (антиакцелерин, антиконвертини др.). Снижение активности этих ингибиторов повышает свертываемость крови и способствует образованию тромбов. Повышение активности ингибиторов, наоборот, затрудняет свертывание крови и может сопровождаться развитием геморрагии. Сочетание явлений рассеянного тромбоза и геморрагии может быть обусловлено нарушением регуляторных взаимоотношений свертывающей и противосвертывающей систем. В кровеносных сосудах имеются хеморецепторы, способные реагировать на появление в крови активного тромбина. Хеморецепторы связаны с нейрогуморальным механизмом, регулирующим образование антикоагулянтов. Таким образом, если тромбин появляется в циркулирующей крови в условиях нормального нейрогуморального контроля, то в этом случае он не только не вызывает свертывания крови, но, напротив, рефлекторно стимулирует образование антикоагулянтов и тем самым выключает свертывающий механизм. Наиболее быстро действующими компонентами противосвертывающей системы являются антитромбины. Они относятся к так называемым прямым антикоагулянтам, так как находятся в активной форме, а не в виде предшественников. Предполагают, что в плазме крови существует около шести различных антитромбинов. Наибольшая антитромбиновая активность присуща антитромбину III; он сильно активируется в присутствии гепарина, обладающего большим отрицательным зарядом. Гепарин способен связываться со специфическим катионным участком антитромбина III,вызывая конформационные изменения его молекулы. В результате этого изменения антитромбин III приобретает возможность связываться со всеми сериновыми протеазами (большинство факторов свертывания крови представляют собой сериновые протеазы). В системе свертывания крови антитромбин III ингибирует активность тромбина, факторов IXa, Xa, XIa и ХIIа. Известно, что небольшое количество гепарина находится на стенках сосудов, вследствие этого снижается активация «внутреннего» пути свертывания крови. У лиц с наследственной недостаточностью антитромбина III наблюдается склонность к образованию тромбов. Гепарин часто используется в качестве препарата, предотвращающего свертывание крови. Действие гепарина в случае его передозировки можно устранить связыванием его рядом веществ – антагонистов гепарина. К ним относится прежде всего протамин (протамина сульфат). Протамин – сильно катионный полипептид, конкурирует с катионными участками антитромбина III за связывание с полианионным гепарином. Не менее важно применение так называемых искусственных антикоагулянтов . Например, витамин К стимулирует синтез в печени протромбина, проакцелерина, проконвертина, фактора X; для снижения активности свертывающей системы крови назначают антикоагулянты типа антивитаминов К. Это прежде всего дикумарин, неодикумарин, пелентан, синкумар и др. Антивитамины К тормозят в клетках печени синтез перечисленных ранее факторов свертывания крови. Этот способ воздействия дает эффект не сразу; а спустя несколько часов или даже дней.
В организме существует мощная фибринолитическая система, обеспечивающая возможность растворения (фибринолиз) сформировавшихся кровяных сгустков – тромбов. Ретрагированный сгусток фибрина в организме человека и животных под влиянием протеолитического фермента плазмы крови – плазмина подвергается постепенному рассасыванию с образованием ряда растворимых в воде продуктов гидролиза – пептидов. В норме плазмин находится в крови в форме неактивного предшественника – плазминогена. Превращение плазминогена в плазмин сопровождается отщеплением от полипептидной цепи 25% аминокислотных остатков. Катализируется эта реакция как активаторами крови, так и активаторами тканей *. Ведущая роль в этом процессе принадлежит кровяным активаторам. В норме активность кровяных активаторов плазминогена очень низкая, т.е. они находятся в основном в форме проактиваторов. Весьма быстрое превращение кровяного проактиватора в активатор плазминогена происходит под влиянием тканевых лизокиназ, а также стрептокиназы. Стрептокиназа вырабатывается гемолитическим стрептококком и в обычных условиях в крови отсутствует. Однако при стрептококковой инфекции возможно образование стрептокиназы в большом количестве, что иногда приводит к усиленному фибринолизу и развитию геморрагического диатеза. Необходимо также иметь в виду, что наряду с фибринолитической системой крови человека имеется и система антифибринолитическая. Она состоит из различных антикиназ, антиплазмина и других антиактиваторов. В практической медицине в лечебных целях ферментные препараты и их ингибиторы широко используются при нарушении свертывающей и противосвертывающей систем крови. Так, при тромбоэмболической болезни применяют ферменты, способствующие либо лизису образовавшегося тромба, либо снижению повышенной свертываемости крови. При состояниях, сопровождающихся развитием фибринолиза, используются ингибиторы ферментов. Исследования последних лет дают основание считать, что введение плазмина в сочетании с гепарином (антитромбином) может быть эффективным не только при лечении тромбоза легочной артерии, тромбофлебитов, но и при лечении инфаркта миокарда, если вводить эти препараты в первые часы после начала болезни. В качестве фибринолитических препаратов при инфаркте миокарда можно использовать также активаторы плазминогена –урокиназу и стрептокиназу. Новое перспективное направление – использование иммобилизованных ферментов (стрептодеказа и др.). Такие формы ферментов полностью сохраняют каталитическую активность, действие их в организме более длительно, а антигенность снижена. Следует помнить, что терапия тромболитическими препаратами требует хорошо организованного лабораторного контроля, так как протеолитическое действие плазмина не является строго специфическим только для фибрина – основного компонента тромба: введение плазмина может вызвать нежелательное расщепление многих важных для свертывания крови веществ, что в свою очередь может привести к серьезным осложнениям,в частности к развитию геморрагического диатеза.
Читайте также: Билирубин у новорожденных норма
По материалам studfiles.net
Трудно переоценить роль и значение макро- и микроэлементов в нашем организме. Подавляющее количество всех встречающихся в природе химических элементов (81) обнаружены в организме человека. Все минеральные вещества принято делить на две группы — макроэлементы и микроэлементы. Макроэлементы присутствуют в организме человека в относительно большом количестве. Двенадцать из них являются структурными, т.к. они составляют 99 % элементного состава человеческого организма (С, О, Н, N, Ca, Mg, Na, K, S, P, F, Cl). Четыре из них (азот, водород, кислород и углерод) являются основным строительным материалом. Остальные элементы, находясь в организме в незначительных по объему количествах, играют важную роль, влияя на здоровье и состояние нашего организма.
Минералы вместе с водой обеспечивают постоянство осмотического давления клеточных и внеклеточных жидкостей, кислотно-щелочного равновесия, процессов всасывания, секреции, кроветворения, костеобразования, свертывания крови, определяют состояние водно-солевого обмена; без них были бы невозможны функции мышечного сокращения, нервной проводимости, внутриклеточного дыхания. Большое значение имеют минеральные вещества для образования и формирования белка. Микроэлементы действуют в организме путем вхождения в той или иной форме и в незначительных количествах в структуру биологически активных веществ, главным образом ферментов (энзимов).
Теории, связывающие развитие многих болезней с дефицитом макро- и микроэлементов, относятся к самым современным научным разработкам. Нарушение минерального обмена приводит к развитию тяжелых патологических состояний — остеопорозу, остеомаляции, рахиту, повышению нервно-мышечной возбудимости и др. Повышение или понижение содержания определенных минеральных веществ в организме характерно для многих заболеваний.
В природе минералы присутствуют в почве, откуда переходят в корни растений, задерживаются во фруктах, овощах и проходят через пищевую цепочку в организме животных. Поскольку организм не способен вырабатывать какие-либо минеральные вещества самостоятельно, он должен получать их с пищей. К сожалению, в результате экологической обстановки, наши земли оскудели и не содержат достаточного количества необходимых для растений веществ, а значит и наши овощи и фрукты не столь богаты полезными и необходимыми для нас питательными веществами. Поэтому, актуальным и важным фактором восполнения и сбалансированности макро- и микроэлементов является поступление их с биологически активными добавками (БАДами).
Общее содержание кальция в организме человека составляет примерно 1,9% общего веса человека, при этом 99% всего кальция приходится на долю скелета и лишь 1% содержится в остальных тканях и жидкостях организма. Кальций в пище, как растительной, так и животной, находится в виде нерастворимых солей. Всасывание их в желудке почти не происходит. Абсорбция кальциевых соединений происходит в верхней части тонкого кишечника, главным образом в 12-перстной кишке. Здесь на всасывание оказывают большое влияние желчные кислоты. Физиологическая регуляция уровня кальция в крови осуществляется гормонами паращитовидных желез и витамином D через посредство нервной системы.
Кальций участвует во всех жизненных процессах организма. Нормальная свертываемость крови, происходит только в присутствии солей кальция. Кальций играет важную роль в нервно-мышечной возбудимости тканей. При увеличении в крови концентрации ионов кальция и магния нервно-мышечная возбудимость уменьшается, а при увеличении концентрации ионов натрия и калия — повышается.
При избытке кальция наблюдаются: Хронический гипертрофический артрит, кистозная и фиброзная остеодистрофия, мышечная слабость, затруднение координации движений, деформация костей позвоночника и ног, самопроизвольные переломы, переваливающаяся походка, хромота. Тошнота, рвота, боли в брюшной полости, дизурия, хронический гломерулонефрит, полиурия, частые мочеиспускания. При избытке кальция наблюдаются сильные сердечные сокращения и остановка сердца в систоле.
Избыток кальция может приводить к дефициту цинка и фосфора, в то же время препятствует накоплению свинца в костной ткани.
При недостатке кальция наблюдаются: Тахикардия, аритмия, боли в мышцах; Рвота, запоры, почечная или печеночная колика; Повышенная раздражительность, дезориентация, галлюцинации, спутанность сознания, потеря памяти; Волосы — делаются грубыми и выпадают; Ногти — становятся ломкими; Кожа — утолщается и грубеет; Зубы — дефекты в дентине, на эмали зубов появляются ямки, желобки; Хрусталик — теряет прозрачность.
Белок, входящий в рацион влияет на усвояемость кальция. При высокобелковом рационе около 15% кальция, полученного орально, всасывается; а при низкобелковом рационе усваивается около 5%.
Кальций усваивается лучше, если принимать его не натощак, а после легкой еды.
Кофе увеличивает выделение кальция почками.
Магний может уменьшить усвояемость кальция из кишечного тракта, при этом, однако, резкая недостаточность магния также может вызвать снижение содержания кальция в крови.
Железо может способствовать усвоению кальция.
На усвояемость кальция влияют какао, соевые бобы и пища с высоким содержанием фосфатов, в том числе и газированные напитки кола.
Стресс и иммобилизация могут уменьшить способность усваивать кальций из желудочно-кишечного тракта.
Некоторые антибиотики, такие как пенициллин и неомицин, могут способствовать усвоению кальция в кишечнике.
Лекарства типа кортизона (кортизон и родственные ему препараты), противосудорожные препараты и тиреоидин могут уменьшать усвояемость кальция в кишечнике.
Кальций содержится в:Сыре, твороге, молоке, мягких костях лосося и сардин, пшеничны отрубях, белокочанной капусте, овсяной крупе, крапиве, орехах (грецкий, фундук), капусте цветной, перловой крупе, спарже, листовых овощах, яичных желтках, хлебе с отрубями, укропе, морской рыбе, мясе и субпродуктах, петрушке, шпинате, свекле.
Существенной функцией калия является его участие в регуляции возбудимости мышц, прежде всего сердечной мышцы. Калию свойственна способность, разрыхлять клеточные оболочки, делая их проницаемыми для прохождения солей. Калий поддерживает осмотическое давление в крови. Он необходим для ясности ума, избавления от шлаков, лечения аллергии. Калий — важный клеточный элемент, в отличие от натрия, он не способствует задержке воды в организме и оказывает диуретическое действие, препятствует развитию соль — индуцированной артериальной гипертензии. Калий принимает участие в транспортировке различных веществ в клетку, обеспечивая этим ее функционирование. Калий участвует в регуляции кислотно-щелочного равновесия в крови и других органах. Он участвует в активации ферментов и синтезе коллагена.
Общее содержание калия в организме человека составляет примерно 250г. Суточная потребность в калии составляет 1,5-2 г.
Недостаток Калия проявляется: замедлением роста организма и нарушением половых функций, возникновением судорожных сокращений скелетных мышц, снижению сократимости сердечной мышцы и нарушению ритма сердечной деятельности (сердечная аритмия).
При недостаточном поступлении калия, организм может в течение некоторого времени восполнять создавшийся дефицит путем мобилизации его из тканевых депо. Тканевым депо для калия являются мышцы.
Избыток калия может привести к дефициту кальция (Ca).
При применении внутрь даже больших доз калия, его токсическое действие не проявляется за исключением случаев почечной недостаточности.
Калий содержится в: Мясе и субпродуктах, смородине черной, овсяной крупе, черносливе, арбузе, кукурузе, тыкве, бобовых, пшенной крупе, петрушке, изюме, цитрусовых, пшеничных отрубях, пивных дрожжах, перловой крупе, томатах, картофеле, листьях мяты, гречневой крупе, бананах, рисе, моркове, орехах (грецкий, фундук), топинамбуре, абрикосе, капусте, вишне, сливе, твороге, чернике, рябине, укропе, тыкве, свекле, бруснике, шиповнике, зверобое, землянике,калине, облепихе, крапиве.
Общее содержание магния в организме человека составляет примерно 21 г. Большая часть магния находится в составе костной ткани и мышцах. В плазме крови, в эритроцитах и в мягких тканях он в основном содержится в ионизированном состоянии. Магний является необходимой составной частью всех клеток и тканей, участвуя вместе с ионами других элементов в сохранении ионного равновесия жидких сред организма. Он входит в состав ферментов (приблизительно 300), в т. ч. АТФ — зависимых. Магний активирует фосфатазу плазмы и костей и участвует в процессе нервно-мышечной возбудимости. Он обладает спазмолитическим и сосудорасширяющим свойствами. При инфаркте миокарда, улучшая его кислородное обеспечение, ограничивает зону повреждения. Магний способствует снижению артериального давления. Кроме того, он способен стимулировать перистальтику кишечника и повышать выделение желчи.
Оказывает положительное влияние на состояние репродуктивной системы. У беременных женщин магний предотвращает недостаточность развития плода (вместе с фолиевой и пантотеновой кислотами), развитие токсикозов, преждевременные роды и выкидыши. Во время менопаузы у женщин обеспечивает снижение отрицательных проявлений этого состояния.
При сахарном диабете магний предотвращает сосудистые осложнения и в сочетании с цинком, хромом, селеном улучшает функцию бета — клеток поджелудочной железы. При заболеваниях органов дыхания способствует расширению бронхов и снятию бронхоспазма.
Избыток магния оказывает в основном слабительных эффект (особенно сульфат магния), а также может приводить к дефициту кальция и фосфора.
При снижении концентрации магния в крови, наблюдаются симптомы возбуждения нервной системы вплоть до судорог. Уменьшение магния в организме приводит к увеличению содержания кальция. Недостаток этого минерала в организме приводит к иммунодефициту и хроническому грибковому поражению кишечника.
Минеральный обмен и потребность в минеральных веществах взаимосвязаны. Особенно отчетливо это установлено в отношении кальция, фосфора и магния. Магния требуется меньше чем кальция, их оптимальным соотношением в рационе считается 0,6:1.
Магний поступает в организм с пищей, водой и солью. Ежедневная потребность в магнии — 0,250-0,350 г. Магний является составной частью хлорофилла, содержится во всех продуктах растительного происхождения. Особенно богаты магнием — необработанные зерновые, фиги, миндаль, орехи, темно-зеленые овощи, бананы, инжир. Мясные и молочные продукты характеризуются низким содержанием магния.
Источником натрия для человеческого организма служит поваренная соль. Значение ее для нормальной жизнедеятельности очень велико. За счет поваренной соли, находящейся в пище, восполняется расход хлорида натрия, входящего в состав крови и соляной кислоты желудочного сока.
Натрий участвует в регуляции осмотического давления, обмена веществ, в поддержке щелочно-кислотного равновесия. Он необходим для нормального функционирования нервно-мышечной системы, активации ферментов.
Натрий, наряду с калием, магнием, кальцием выполняют важную роль в регуляции функции сердечной и скелетных мышц.
Натрий также как и Калий важен для нормального роста и состояния организма. Натрий и Калий принимают участие в транспортировке различных веществ в клетку, обеспечивая этим ее функционирование. Кровь человека содержит 0,32% натрия и 0,20% калия. Натрий и калий являются антагонистами, т.е. повышение содержания натрия приводит к уменьшению калия. И, наоборот, на выделение хлористого натрия из организма, а, следовательно, и на потребность в нем влияет количество солей калия, получаемое организмом.
При дефиците натрия происходит нарушение усвоения углеводов, возможны невралгии, отчасти понижение давления. Пониженное содержание натрия в волосах у взрослых обычно встречается при нейроэндокринных нарушениях, хронических заболеваниях почек и кишечника и как следствие черепно-мозговых травм.
Повышенное содержание натрия в волосах отражает, как правило, нарушение водно-солевого обмена, дисфункцию коры надпочечников. Может встречаться при избыточном потреблении поваренной соли, сахарном диабете, нарушении выделительной функции почек, склонности к гипертонии, отекам, неврозам. Люди, особенно дети, с избытком натрия часто легковозбудимы, впечатлительны, гиперактивны, у них может быть повышена жажда, потливость. Иногда возможно накопление натрия в волосах при длительном контакте с морской водой и отдельными видами моющих средств.
Нормы суточного потребления не существует, однако считается, что потребность взрослого человека составляет около 500 мг хлорида натрия (поваренной соли) в сутки.
Натрий и калий находятся во всех растительных и животных продуктах. В растительных продуктах больше калия, в животных больше натрия. Много натрия, по сравнению с другими растительными продуктами, содержится в ежевике сизой, крыжовнике.
После кислорода кремний — самый распространенный элемент на земле. В виде кремнезема кремний содержится во всех растениях. Они поглощают его из почвы и используют при строительстве прочной основы для своих клеток. Твердость, эластичность и прочность стеблей растений зависят от содержания в них кремнезема. Кремний в виде кремнезема содержится в организме морских животных, пресноводных рыб, птиц и млекопитающих. Он входит в состав скелетных образований у животных. Кремний содержится постоянно в курином яйце. Общее содержание кремнезема в теле человека — около 0,001%, среднее содержание SiO2 в крови человека составляет от 5,9 до 10,6 мг в 1 мл. Источником его является вода и растительные пищевые продукты.
В организме человека кремний обнаружен во всех органах и тканях: в легких, в волосах, гладких мышцах желудка, в надпочечниках, щитовидной железе, гипофизе, в фибрине. Кремний находится в плазме крови, как и железо, он нужен для образования эритроцитов. Кремнезем необходим для прочности и эластичности эпителиальных и соединительно-тканных образований, которые имеют важное значение для продления здоровья, молодости и жизнеспособности организма. Эластичность кожи, сухожилий, стенок сосудов обусловлена в значительной степени содержащимся в них кремнием. Он способствует биосинтезу коллагенов и образованию костной ткани (после перелома количество кремния в костной мозоли увеличивается почти в 50 раз). Кремнезем играет роль в сохранении кожей нормального тургора, что связано со способностью коллоидов, содержащих кремнезем, к набуханию.
Дистрофия, эпилепсия, ревматизм, ожирение, атеросклероз — вот перечень болезней, которые сегодня можно успешно лечить, увеличив в своем рационе количество растений, богатых кремнеземом. В отличие от железа и кальция кремнезем легко усваивается организмом даже в пожилом возрасте. Хорошо действует кремний на капилляры, уменьшая их проницаемость и предупреждая появление хрупкости (о чем свидетельствуют так называемые синяки).
При недостатке кремния могут наблюдаться: слабая деятельность лейкоцитов при инфекционном процессе, плохое заживление ран, снижение аппетита, кожный зуд, снижение эластичности тканей, снижение тургора кожи, повышение проницаемости сосудов и как следствие — геморрагические проявления.
С возрастом содержание кремния в организме уменьшается. Ломкость костей в пожилом возрасте объясняется дефицитом не только кальция, но и кремнезема. Кремний способствует росту — он помогает «строить» кости независимо от витамина D. Поэтому он необходим и детям, и старикам, и взрослым — здоровым и больным, так как оказывает благоприятное воздействие на работу сердца, состояние зубов, костей, волос, ногтей.
Синергисты. Избыток алюминия в организме может вызывать снижение содержания кремния. При потреблении рафинированных пищевых продуктов уровень кремния в организме снижается, а при рационе, богатом пищевыми волокнами – возрастает. Для правильного обмена веществ необходимо сочетание кремния с кальцием и магнием.
Соединения кремния нетоксичны. Кремнезем токсично действует на организм человека, попадая в легкие при вдыхании пыли с его содержанием. Пыль кремнийсодержащих неорганических соединений может вызвать развитие заболевания легких — силикоз.
Повышенное поступление кремния в организм может вызвать нарушение фосфорно-кальциевого обмена, образование мочевых камней.
Самые богатые источники кремния – неочищенное зерно с высоким содержанием волокон, продукты из хлебных злаков и корнеплоды овощей. Много кремния в топинамбуре, водорослях, отрубях, лесных ягодах, зелени.
Большое количество кремния содержится в фруктах: абрикосах, бананах, вишнях, клубнике, землянике, овсе, огурцах, пророщенных зернах злаков, в цельном зерне пшеницы, просе. В лекарственных растениях кремний содержится в: хвоще полевом, крапиве, листьях одуванчика.
Железо является составной частью гемоглобина, сложных железобелковых комплексов и ряда ферментов, усиливающих процессы дыхания в клетках. Железо стимулирует кроветворение. Оно важно не только для обеспечения организма кислородом, но и функционирования дыхательной цепи и синтеза АТФ, процессов метаболизма и детоксикации эндогенных и экзогенных веществ, синтеза ДНК, инактивации токсических перекисных соединений. Железосодержащие соединения играют важную роль в функционировании иммунной системы, прежде всего, клеточного звена. Железо входит в состав протоплазмы всех клеток.
Его общее содержание в организме человека составляет около 4,25 г. Из этого количества 57% находится в гемоглобине крови, 23% — в тканях и тканевых ферментах, а остальные 20% — депонированы в печени, селезенке, костном мозге и представляют собой «физиологический резерв». Средний пищевой рацион человека должен содержать не менее 20 мг, а для беременных — 30 мг железа. Важно помнить, что в течение месяца женщины теряют железа почти вдвое больше, чем мужчины.
В овощах, фруктах, ягодах железа сравнительно мало, но они служат ценным источником этого минерала, так как содержащееся в них железо легко усваивается организмом человека. Его всасыванию из пищевых продуктов способствуют лимонная, аскорбиновая кислоты и фруктоза, которые содержатся во фруктах, ягодах, их соках.
В зерновых и бобовых продуктах и некоторых овощах содержатся фосфаты, фитины и щавелевая кислота, препятствующие всасыванию железа. При добавлении мяса или рыбы к этим продуктам усвоение железа улучшается, при добавлении молочных продуктов — не меняется, при добавлении яиц — ухудшается. Подавляет усвоение железа крепкий чай, кофе.
Вопросы обеспеченности организма железом занимают одно из центральных мест в общей проблеме полноценного питания. Это обусловлено специфической ролью железа в организме, и тем обстоятельством, что железодефицитные состояния являются одними из наиболее распространенных видов пищевой недостаточности даже в высокоразвитых странах.
При дефиците железа в организме, прежде всего, ухудшается клеточное дыхание, что ведет к дистрофии тканей и органов и нарушению состояния организма еще до развития анемии. Наблюдается бледность кожных покровов, инъекция сосудов склер, дисфагия, повреждаются слизистые оболочки полости рта и желудка, истончаются и деформируются ногти.
Выраженный дефицит железа ведет к гипохромной анемии. Причина гипохромной анемии в недостаточном поступлении железа с пищей или преобладание в рационе продуктов, из которых оно плохо усваивается. Развитию железодефицитных состояний способствует недостаток в питании животных белков, витаминов, кроветворных микроэлементов. Дефицит железа в организме возникает при острых и хронических кровопотерях, заболеваниях желудка и кишечника (резекция желудка, анацидный гастрит, энтерит), некоторых глистных инвазиях. Поэтому при многих заболеваниях потребность в железе увеличивается.
Читайте также: Ушиб поясницы: признаки, первая помощь, лечение
В случаях дефицита железа прием железосодержащих препаратов и БАД нужно совмещать с приемом антиоксидантов: витаминов С и Е, а также меди.
Избыток железа в организме может привести к дефициту меди, цинка, хрома и кальция, а также к избытку кобальта.
Присутствие селена в организме оказывает антиоксидантное действие, замедляя старение, способствует предупреждению роста аномальных клеток, укрепляет иммунную систему. В сочетании с витаминами А, С и Е предохраняет от возникновения онкологических заболеваний, помогает при артрите, разрушает вредные для организма вещества (защищает организм от тяжёлых металлов). Увеличивает выносливость организма благодаря увеличению поступления кислорода к сердечной мышце. Селен необходим для образования белков; поддерживает нормальную работу печени, щитовидной железы, поджелудочной железы. Является одним из компонентов спермы, важным для поддержания репродуктивной функции.
Селен влияет на нормальное развитие и функционирование суставных тканей. От его содержания в организме зависит перенос и встраивание серы в состав хряща.
Селен принимает участие в обмене серосодержащих аминокислот и предохраняет витамин Е, являясь его синергистом, от преждевременного разрушения, защищает клетки от свободных радикалов.
Избыток селена может вызывать увеличение печени до 3-х см и боли в правом подреберье, боли в конечностях, судороги, чувство онемения; может привести к дефициту кальция. Одним из признаков передозировки селеном является специфичный (чесночный) запах изо рта.
При дефиците селена в организме усиленно накапливаются мышьяк и кадмий, которые, в свою очередь, усугубляют дефицит селена. Недостаток селена приводит к ослаблению антиоксидантного статуса, антиканцерогенной защиты, обусловливает миокардиодистрофию, нарушение сексуальной функции, иммунодефициты. При дефиците селена снижается устойчивость организма к вирусным инфекциям.
Суточные нормы составляют: 50 мкг — для женщин, 70 мкг — для мужчин, 65 мкг — для беременных и 75 мкг — для кормящих грудью.
Основной причиной дефицита являются почвы, обеднённые селеном. И соответственно недостаточное поступление селена с пищей, особенно с хлебом и хлебобулочными и мучными изделиями.
Селен содержится в пшеничных зародышах, отрубях, луке, помидорах, капусте брокколи, морепродуктах, почках, печени.
Приглашаю к сотрудничеству, а также на обучение программам сохранения и восстановления здоровья с применением натуральных препаратов.
Дополнительная информация по тел.: 8-967-197-76-37 или по E-Mail
Врач Восстановительной медицины Шипова Елена Игоревна
По материалам www.vita-club.ru
Результаты клинических исследований современных ученых указывают на то, что различные микроэлементы прямым или опосредованным образом влияют на систему гемостаза организма человека. Не является исключением и железо, которое также влияет на свертываемость крови. Дефицит микроэлемента приводит к повышенному риску тромбооразования, то есть активируются факторы, приводящие к агрегации, или как его еще называют – склеиванию форменных элементов. Ученые занялись изучением изменения факторов свертывания крови. Результаты несколько удивили, поскольку лица, имеющие наследственную предрасположенность к тромботическим патологиям, также страдали от железодефицита.
Система гемостаза нашего организма создана для того, чтобы предотвратить кровопотерю или же устранить закупорки сосудов. По своей сути коагуляция или свертываемость крови представляет собой некий внутренний защитный механизм. Согласно статистике, по состоянию на сегодняшний день каждый второй житель планеты страдает от нарушения работы системы гемостаза.
Именно они приводят к таким тяжелым состояниям, как массивные кровотечения, ишемические катастрофы – инфаркты, инсульты, тромбозы магистральных артерий. Если человеку не была оказана неотложная медицинская помощь, то вероятность летального исхода достигает 20-30%.
Важно учитывать, что большинство этих пациентов попросту не знают о том, что у них есть нарушения работы свертывающей системы. Поэтому каждый врач должен обследовать своих больных, а также знать, ионы каких микроэлементов влияют на работу этой жизненно важной системы организма.
Такой микроэлемент, как кальций, является одним из важнейших минералов для нас. Он не только участвует в процессе коагуляции, но и в других реакциях для поддержания нормального гемостаза, формировании физиологического состояния и содержания коллоидных и кристаллоидных элементов. Влияние кальция на усвояемость других металлов также очень высокое.
Другая его важнейшая функция заключается в регуляции проницаемости мембран клеточной стенки, кровеносных сосудов. Он способствует их уплотнению и снижению проницаемости. Натрий и калий в данном случае обладают обратным эффектом. Здесь необходимо сделать важный вывод о том, что все микроэлементы тесно связаны друг с другом, и дисбаланс одного из них повлечет за собой изменение концентрации другого, а коррекция этого состояния будет состоять не из одного шага.
Кальций играет роль в нормальном содержании протромбина, из которого формируется тромбинфермент. Этот процесс происходит исключительно тогда, когда в крови содержится достаточное количество кальция. Его избыток можно считать одним из факторов, повышающих свертывание.
Также необходимо отметить то, что этот микроэлемент крайне важен для нормальной возбудимости тканей и нервных волокон. Чрезмерная активность мышц приводит к гиповолемии и дисбалансу микроэлементов за счет повышенной потери жидкости и расходу минералов. Следующим этапом этого патогенетического механизма будет гиперкоагуляция, которая почти всегда протекает на фоне гиперкальциемии.
Помимо железа и кальция, существуют и другие минералы, влияющие на состояние сосудов, системы гемостаза. Одним из таких считается магний. Воздействие на коагуляцию происходит за счет выведения холестерина и растворения холестериновых бляшек, что способствует снижению свертывания крови. Этот элемент жизненно необходим пациентам, которые страдают патологиями сердечно-сосудистой системы, гипертонической болезнью, нарушениями обмена веществ – дислипидемией, сахарным диабетом. Существуют витаминные комплексы, применяемые для профилактики тромбоза. Они практически всегда содержат магний. Элемент противопоказан при любых кровотечениях, связанных или не связанных с его дисбалансом.
Среди других полезных свойств минерала следует отметить стимуляцию нормальной работы органов пищеварения, уменьшение образования камней мочеполовой системы.
Врачу необходимо понимать, что без магния невозможна нормальная усвояемость витаминов группы В, а также кальция, влияние которого на гемостаз было описано выше. Гипомагниемия способна спровоцировать отложение солей кальция на стенках кровеносных сосудов, усугубляя течение гиперхолестеринемии, атеросклероза магистральных артерий, способствуя повышению артериального давления и увеличению риска развития сосудистых катастроф.
Микроэлемент также является антагонистом кальция. Его нормальное содержание препятствует формированию кальциевого парадокса, который негативно влияет на мышечную ткань, миокард в частности. При деструкции клеток мышечной ткани запускается выход калия в кровяное русло, что также влечет за собой изменения работы системы коагуляции.
На систему свертывания ионы калия влияют очень опосредованно. Повышенная проницаемость сосудов, которая встречается при увеличении содержания микроэлемента, способствует агрегации форменных элементов. Система свертывания не всегда способна быстро реагировать на этот момент, поэтому механизм, стимулирующий пролиферацию клеток, тромбоцитов в частности, останавливается с опозданием. Это влечет за собой формирование кровяных сгустков, способных закупорить мелкий сосуд.
Тромбы, сформировавшиеся из тромбоцитов, начинают свое увеличение по причине агрегации эритроцитов. Если вовремя не принять меры относительно их лизиса, могут возникнуть сосудистые катастрофы. Чтобы не допустить повышенной свертываемости, доктора должны отслеживать уровень содержания калия в плазме крови.
При высвобождении ионов калия из клетки во внеклеточное пространство при повреждении тканей организма развивается ацидоз. Этот процесс запускается по причине травматического повреждения мышц, внутреннего кровоизлияния или гемолиза красных кровяных телец. Другим пусковым механизмом служит прием некоторых лекарственных препаратов – аргинина, холинов, сердечных гликозидов, антигипертензивных средств (ингибиторов АПФ или бетаблокаторов).
Ацидоз провоцирует явления гиперосмолярности всех жидких сред организма и дефицит гормона, отвечающего за нормальный уровень сахара крови – инсулина. Следствием всех этих механизмов является увеличение коагуляции крови. Если вовремя не оказать пациенту помощь, не провести коррекцию ацидоза, развивается паралич, летальный исход.
Из всех вышеперечисленных элементов, железо имеет самое большое влияние на свертываемость крови. Оно обусловлено тем, что микроэлемент участвует в синтезе гема, поэтому его применяют для лечения анемии. Феррум способствует поддержанию нормальной концентрации гемоглобина в крови, эритроцитов в крови.
Также отмечается его влияние на кроветворение и свертывание крови за счет продукции новых форменных элементов. Благодаря дополнительному введению витамина В12 (внешнего фактора Касла) и фолиевой кислоты терапия анемии проходит намного быстрее. Исходя из этого можно сделать вывод, что влияние железа на гемостаз заключается в поддержании нормальной концентрации минерала.
Прежде, чем назначать препараты, врачу следует изучить причину, которая послужила пусковым механизмом дестабилизации системы кроветворения. Лечение анемий проводится при помощи препаратов железа, витаминных комплексов и фолиевой кислоты. Иногда к терапии добавляют магний, который зачастую содержится в средствах, обогащенных витаминами.
Для поддержания нормальной усвояемости микроэлементов, лечение включает кальций. Важно учитывать, что применение любого средства должно проводится под контролем анализа крови на содержания минералов для адекватной коррекции дозировок, недопущения выраженного дефицита или переизбытка.
По материалам gemato.ru
Кровь движется в нашем организме по кровеносным сосудам и имеет жидкое состояние. Но в случае нарушения целостности сосуда, она за достаточно малый промежуток времени образует сгусток, который называют тромб или «кровяной сгусток». С помощью тромба ранка закрывается, и тем самым останавливается кровотечение. Рана со временем затягивается. В противном случае, если процесс свертывания крови по каким-либо причинам нарушен, человек может погибнуть даже от небольшого повреждения.
Свертывание крови является очень важной защитной реакцией организма человека. Оно препятствует потере крови, при этом сохраняется постоянство ее объема, находящегося в организме. Механизм свертывания запускается при помощи изменения физико-химического состояния крови, которое основано на растворенном в ее плазме белке фибриногене.
Фибриноген способен превращаться в нерастворимый фибрин, выпадающий в виде тоненьких нитей. Эти самые нити могут образовывать густую сеть с мелкими ячейками, которая задерживает форменные элементы. Вот так и получается тромб. Со временем кровяной сгусток постепенно уплотняется, стягивает края раны и тем самым способствует ее скорейшему заживлению. При уплотнении сгусток выделяет желтоватую прозрачную жидкость, которая называется сывороткой.
В свертывании крови участвуют также тромбоциты, которые уплотняют сгусток. Этот процесс похож на получение творога из молока, когда сворачивается казеин (белок) и так же образуется сыворотка. Рана в процессе заживления способствует постепенному рассасыванию и растворению сгустка фибрина.
А. А. Шмидт в 1861 году выяснил, что процесс свертывания крови является полностью ферментативным. Он установил, что превращение фибриногена, который растворен в плазме, в фибрин (нерастворимый специфический белок), происходит при участии тромбина – особого фермента.
У человека в крови постоянно имеется немного тромбина, который находится в неактивном состоянии, протромбине, как его еще называют. Протромбин образуется в печени человека и превращается в активный тромбин под воздействием тромбопластина и солей кальция, имеющихся в плазме. Нужно сказать, что тромбопластин не содержится в крови, он образуется только в процессе разрушения тромбоцитов и при повреждениях других клеток организма.
Возникновение тромбопластина – это довольно сложный процесс, так как кроме тромбоцитов в нем участвуют некоторые белки, содержащиеся в плазме. При отсутствии в крови отдельных белков свертывание крови может быть замедлено или вообще не происходить. Например, если в плазме недостает одного из глобулинов, то развивается всем известное заболевание гемофилия (или по другому – кровоточивость). Те люди, которые живут с этим недугом, могут потерять значительные объемы крови вследствие даже небольшой царапины.
Таким образом, свертывание крови – это поэтапный процесс, который состоит из трех фаз. Первая считается самой сложной, в процессе которой происходит образование комплексного соединения тромбопластина. В следующей фазе для свертывания крови необходимы тромбопластин и протромбин (неактивный фермент плазмы). Первый оказывает действие на второй и, тем самым превращает его в активный тромбин. И в заключительной третьей фазе тромбин, в свою очередь, оказывает воздействие на фибриноген (белок, который растворен в плазме крови), превращая его в фибрин – нерастворимый белок. То есть с помощью свертывания кровь переходит из жидкого в желеобразное состояние.
Выделяют 3 типа кровяных сгустков или тромбов:
- Из фибрина и тромбоцитов образуется белый тромб, он содержит относительно небольшое количество эритроцитов. Обычно появляется в тех местах повреждения сосуда, где кровоток обладает большой скоростью (в артериях).
- В капиллярах (очень маленьких сосудах) образуется диссеминированные отложения фибрина. Это и есть второй тип тромбов.
- И последние – это красные тромбы. Они появляются в местах замедленного кровотока и при обязательном отсутствии изменений в стенке сосуда.
Образование тромба является очень сложным процессом, в нем участвуют многочисленные белки и ферменты, которые находятся в плазме крови, тромбоцитах и ткани. Это и есть факторы свертывания крови. Те из них, которые содержатся в плазме, принято обозначать римскими цифрами. Арабскими указываются факторы тромбоцитов. В организме человека имеются все факторы свертываемости крови, находящиеся в неактивном состоянии. При повреждении сосуда происходит быстрая последовательная активация их всех, в результате этого кровь сворачивается.
Для того чтобы определить, нормально ли сворачивается кровь, проводят исследование, которое называется коагулограммой. Сделать такой анализ необходимо, если у человека есть тромбозы, аутоиммунные заболевания, варикозное расширение вен, острые и хронические кровотечения. Также обязательно его проходят беременные женщины и те, кто готовится к операции. Для такого рода исследования обычно берут кровь из пальца или вены.
Время свертывания крови – это 3-4 минуты. По прошествии 5-6 минут она полностью сворачивается и становится студенистым сгустком. Что касается капилляров, то тромб образуется за время около 2-х минут. Известно, что с возрастом время, затрачиваемое на свертывание крови, увеличивается. Так, у детей от 8 до 11 лет этот процесс начинается через 1,5-2 минуты, а заканчивается уже по истечении 2,5-5 минут.
Протромбин – это белок, который отвечает за свертывание крови и является важным составляющим элементом тромбина. Его норма 78-142%.
Протромбиновый индекс (ПТИ) вычисляется как отношение ПТИ, принятого за стандарт, к ПТИ обследуемого пациента, выражается в процентах. Нормой является 70-100%.
Протромбиновое время – это период времени, за который происходит свертывание, в норме 11-15 секунд у взрослых и 13-17 секунд у новорожденных. С помощью этого показателя можно диагностировать ДВС-синдром, гемофилию и контролировать состояние крови при приеме гепарина. Тромбиновое время является самым главным показателем, в норме оно составляет от 14 до 21 секунды.
Фибриноген является белком плазмы, он несет ответственность за образование тромба, его количество может сообщить о воспалении в организме. У взрослых его содержание должно быть 2,00-4,00 г/л, у новорожденных же 1,25-3,00 г/л.
Антитромбин – это специфический белок, который обеспечивает рассасывание образовавшегося тромба.
Конечно, при кровотечениях очень важна быстрая свертываемость крови, чтобы свести кровопотери к нулю. Сама же она всегда должна оставаться в жидком состоянии. Но существуют патологические состояния, приводящие к свертыванию крови внутри сосудов, а это представляет большую опасность для человека, чем кровоточивость. Такие заболевания, как тромбозы венечных сердечных сосудов, тромбозы легочной артерии, тромбозы сосудов головного мозга и др., связаны с этой проблемой.
Известно, что в организме человека сосуществуют две системы. Одна способствует скорейшему свертыванию крови, вторая же всячески этому препятствуют. Если же обе эти системы находятся в равновесии, то кровь будет сворачиваться при внешних повреждениях сосудов, а внутри них будет жидкой.
Ученые доказали, что нервная система может оказать влияние на процесс образования кровяного сгустка. Так, время свертывания крови уменьшается при болевых раздражениях. Условные рефлексы могут также оказать влияние на свертывание. Такое вещество, как адреналин, которое выделяется из надпочечников, способствует скорейшему свертыванию крови. Одновременно с этим он способен сделать артерии и артериолы более узкими и таким образом снизить возможные кровопотери. В свертывании крови участвуют также витамин К и соли кальция. Они помогают скорейшему протеканию этого процесса, но есть и другая система в организме, которая препятствует ему.
В клетках печени, легких имеется гепарин – особое вещество, прекращающее свертывание крови. Оно не дает образовываться тромбопластину. Известно, что содержание гепарина у юношей и подростков после работы уменьшается на 35-46%, у взрослых же не изменяется.
Сыворотка крови содержит белок, который получил название фибринолизин. Он участвует в растворении фибрина. Известно, что боль средней силы может ускорить свертываемость, однако сильная боль замедляет этот процесс. Препятствует свертыванию крови низкая температура. Оптимальной считается температура тела здорового человека. На холоде кровь сворачивается медленно, иногда этот процесс вообще не происходит.
Увеличивать время свертывания могут соли кислот (лимонной и щавелевой), осаждающие необходимые для быстрого свертывания соли кальция, а также гирудин, фибринолизин, лимоннокислый натрий и калий. Медицинские пиявки могут вырабатывать с помощью шейных желез особое вещество – гирудин, которое обладает противосвертывающим эффектом.
В первую неделю жизни новорожденного свертываемость его крови происходит очень медленно, но уже в течение второй недели показатели уровня протромбина и всех факторов свертывания приближаются к норме взрослого человека (30-60%). Уже через 2 недели после появления на свет содержание фибриногена в крови сильно возрастает и становится как у взрослого человека. К концу первого года жизни у ребенка приближается к норме взрослого содержание остальных факторов свертывания крови. Они достигают нормы к 12 годам.
По материалам www.syl.ru
Для свертывания крови необходимо присутствие — Лечение гипертонии
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день…
Читать далее »
Одно из самых важных проявлений защитной функции крови – это её свертываемость, способность сохранения «красной жидкости» внутри организма, и такая сложная система состоит из множества элементов, которые носят название «факторы свертывания крови». Конечно, с самого детства каждый знает, что именно кровь переносит все необходимые организму для развития вещества по телу, но наряду с полезными, по крови перемещаются и вредные бактерии. И такой процесс, как свёртываемость, позволяет дать этим возбудителям сильный отпор.
Свертываемость крови: понятие и система
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
Система такого процесса представляет собой некую последовательность этапов, в которых конечный продукт первого в обязательном порядке является детерминирующим фактором следующего. Результатом такого процесса является «создание» белка фибрина, который, в свою очередь, образует сгусток. Чтобы проще понять это явление, необходимо привести пример: после небольшого пореза из раны идет кровь, но в один момент ранка как бы закупоривается ее сгустком — он образует корочку. Это и есть процесс свертываемости крови, который не дает этой жидкости покинуть организм.
Считается, что вся эта реакция состоит из 3-х основных этапов:
- На первом этапе происходит образование «протромбиназы».
- На втором этапе формируется вышеназванный белок фибрин.
- На третьем — из фибрина образуется тромбин.
Стоит отметить, что весь процесс свертывания крови получил название «гемостаз». И прежде чем перейти дальше, нужно выделить основные компоненты этого понятия.
Итак, к ним относят:
- кровеносные сосуды (их стенки);
- некоторые элементы крови (тромбоциты);
- ферментная система, а именно способность плазмы крови к свертыванию.
Именно при взаимодействии и активной деятельности этих факторов происходит образование фибрина. Существуют общепринятые мировые нормы написания и обозначения: все элементы нумеруются только при помощи римских цифр. Есть и исключение: 3 элемента, которые являются именными.
- Фибринoген. Нaзывaют фaктором I. Он образуется в костном мозге человека, а также в его печени, селезенке. Такой белок после взаимодействия с тромбином распадается и преобразуется в фибрин.
- Прoтрoмбин. Этот белок носит название фактор II. Он также может синтезироваться в клетках главного фильтра внутренней среды — печени, но уже только при участии витамина К. Если существует недостаток этого витамина, то происходит образование неполноценного протромбина. Однако, функция свертываемости крови может быть нарушена только в том случае, когда количество неполноценного протромбина составляет более 40%. В стандартных условиях существования и при связи с ионами кальция и с таким веществом, как тромбопластин, данный белок преобразуется в тромбин. Этот процесс является сложным, так как на промежуточных этапах образовываются тромбины разного вида: тромбин E, тромбин A, и только лишь тромбин C является основным итогом всей реакции.
- Тромбопластин (его называют тканевым). Он носит название уже вышеупомянутого тромбопластина. Этот белок может находиться в различных органах человеческого организма: в мозге, в легких, в печени и почках. При активном «общении» с факторами VII и IV может спровоцировать синтезирование фактора Х, а также активно участвует в первом этапе всей системы свертывания и играет важную роль в процессе преобразования конечного результата.
- Ионы кальция. Этот элемент является распространённым и частым помощником для остальных. Он играет активную роль в процессах преобразования итогового продукта, а также на протяжении всех этапах свертывания крови. Важно отметить, что он не выводится из организма, и поэтому его можно найти в сыворотке. При низких показателях кальция в крови процесс не нарушится, однако может наблюдаться синдром судороги.
- Проакцелерин. Сложное название V фактора не соответствует его простым функциям. Этот белок также созревает в клетках главного фильтра, но в отличие от многих других, он независим от витамина К и поэтому его можно назвать самостоятельным белком. Фактор влияет на активизацию другого – фактора Х. Также играет большую роль в процессе преобразования и формирования итогового вещества.
- Акцелерин. Этот элемент называют производным от предыдущего, так как он является его активной базой. Не случайно перед предыдущим стоит приставка «про». Существует мнение, что его исключили из общепринятого списка факторов и признают лишь его неактивную форму. Однако, официально не было никаких заявлений, и он продолжает играть существенную роль в превращении сгустка.
- Проконвертин. Еще один белок, который также синтезируется в клетках фильтрационного органа и при участии того же витамина К. Этот элемент надолго задерживается в крови человека и начинает активно проявлять себя только при смачивании поверхности. Вместе с III и с IV фактором образуют фактор Х. Необходимо отметить, что нарушение системы гемостаза может начаться только при содержании проконвертина менее 5-ти % от нужной нормы.
- Антигемофильный глобулин (типа А). Фактор, отмеченный особой буквой А, синтезируется все в том же фильтре, а также в селезенке, почках и лейкоцитах. Такой элемент называют сложным «гликопротеидом». Для нормального функционирования необходимо содержания антигемофильного глобулина от 0,01 до 0, 02 г/л. Для правильной системы гемостаза необходимо не менее 30-ти % от нормы. Этот белок активно участвует в первом этапе системы свертывания крови и взаимодействует с иными факторами.
- Антигемофильный глобулин (типа В). Фактор имеет еще и именную форму: фактор имени Кристмаса. Синтезируется все также в печени при участии витамина К. Обладает термоустойчивостью. Надолго сохраняется в плазме крови и в её сыворотке. Антигемофильный белок типа В является бета-глобулином. Он принимает участие в образовании итогового продукта, а при связи с иными элементами активирует фактор Х.
- Тромбопоэтин. Еще один именной фактор: элемент Стюарта-Прауэра. Он развивается в неактивной фазе клетками важнейшего фильтра организма — печени. Является гликопротеидом. Участвует в образовании конечного результата гемостаза. Этот фактор называют витаминозависимым от витамина К. Именно он больше всего связан с этим элементом. Х фактор является важнейшим звеном первого этапа. При взаимодействии с иными факторами меняет свою неактивную форму на активную.
- Плазменный предшественник тромбопластина. Или по-другому — элемент Розенталя. Имеет и 3-е название: антигемофильный фактор типа С. Является активатором предыдущего элемента.
- Контактная активация. Элемент Хагемана. Его еще называют контактным фактором. Синтезируется по-прежнему клетками фильтрационной печени. Нарушение системы свертывания не вызывает даже отсутствие данного элемента или при показателе менее 1-го %. от нормы. В чем же заключается его контактная активация? Все просто. Именно этот фактор запускает процессы свертывания крови и является локализующим толчком этого процесса.
- Фибриназа (плазменная). Фибриностабилизирующий элемент «закрывает» перечень факторов. Находится в стенках тромбоцитов, эритроцитов, лейкоцитов, а также в мышцах и легких. Переход из неактивной формы в активную может быть только после взаимодействия с тромбином. Этот фактор является главным в формировании кровяного сгустка, а значит, напрямую связан с таким явлением, как коагуляция.
Факторы, не имеющие номера и являющиеся именными
Выше были представлены 12 элементов, нумерация которых является общепринятой в мире медицины. Но существуют 3 немаловажных, которые не обладают своей цифрой, но имеют свое имя.
Такие факторы наряду с вышеназванными вносятся в единую таблицу факторов свертывания крови:
- элемент имени Флетчера;
- элемент имени Фицджеральда;
- элемент имени Виллебранда.
Первый из них содержится и синтезируется в «фильтре» организма. Активно участвует в запуске деятельности фактора Х. Примечательно, что даже при содержании этого элемента менее 1-го %, процесс коагуляции не будет нарушен. Второй фактор также синтезируется клетками вышеназванного органа. Так же, как и предыдущий, не вызывает нарушения в системе гемостаза при малом наличии в организме человека. Фактор отвечает за активацию элемента под номером ХI. Последний именной фактор синтезируется в эндотелии, он содержится в тромбоцитах. Этот элемент носит название «антигеморрагический фактор сосудистого типа». Его наличие позволяет повысить концентрацию необходимого VII элемента при различных повреждениях ткани, тем самым усиливая воздействие и функцию антигемофильного фактора типа А.
Повышенная свертываемость крови: причины возникновения, проявления, диагностика, лечение
Кровь – жидкая ткань нашего тела, которая выполняет массу крайне разнообразных функций, одной из которых является гемостаз или остановка кровотечения. Адекватное выполнение данной задачи достигается тонким балансом между двумя сложными, многокомпонентными, разнонаправленными по своей сути механизмами – свертывающей и противосвертывающей системами организма.
У человека поддержание баланса свертываемости крови в норме оказывает непосредственное влияние на целый ряд процессов:
- Сохранение крови в жидком состоянии;
- Остановка кровотечений;
- Заживление ран;
- Течение нормального воспалительного процесса;
- Проницаемость сосудистой стенки;
- Поддержка гемодинамики (нормальной скорости тока крови в сосудах, уровня артериального давления);
- Работа системы иммунитета и общей сопротивляемости организма.
Нарушение работы системы гемостаза может протекать в двух направлениях:
- Повышенная свертываемость крови или гиперкоагуляция – такое состояние организма, при котором наблюдается патологически увеличенная активность свертывающей системы крови.
- Пониженная свертываемость крови или гипокоагуляция – такое состояние организма, при котором наблюдается патологически увеличенная активность противосвертывающей системы крови.
Далее мы детально рассмотрим высокую свертываемость крови или гиперкоагуляционный синдром.
Причины повышенной свертываемости крови
Гиперкоагуляционный синдром может быть первичным, то есть представлять собой самостоятельный патологический процесс, обусловленный наследственными факторами предопределившими дефект системы свертывания крови. Такие состояния называют тромбофилии, их причинами могут являться:
- Чрезмерная активность и/или повышенное образование факторов свертываемости крови:
- фактора Виллебранда;
- проконвертина;
- фактора Хагемана;
- плазменного предшественника тромбопластина;
- антигемофильного глобулина;
- Сниженная активность и/или недостаточное образование факторов свертываемости крови:
- антитромбина III;
- антикоагулянтов С и S;
- плазминогена и его активаторов;
- кофактора гепарина II.
Вторичный гиперкоагуляционный синдром является следствием и проявлением какого-либо заболевания, либо специфического состояния. К патологическим состояниям, которые проявляются повышенной свертываемостью крови, относятся:
- Опухоли системы крови доброкачественные или злокачественные, затрагивающие как саму жидкую кровь, так и костный мозг, вырабатывающий компоненты крови. Часто течение гематологических опухолей сопровождается повышенной, либо пониженной свертываемостью крови, к таким заболеваниям относятся эритремия, миеломная болезнь, различные лейкозы и прочие.
- Аутоиммунные заболевания – характеризуются образованием антител (белков системы иммунитета) к компонентам своих же клеток. Антитела являются агрессивными белками, которые оседая на компонентах клеток собственного организма, вызывают их повреждение, что приводит к повышенному тромбообразованию. К таким заболеваниям относятся системная красная волчанка, антифосфолипидный синдром и прочие.
- Наследственные заболевания – генетически предопределенные заболевания, которые не оказывают прямого влияния на факторы свертываемости крови, а действуют опосредованно, не являясь при этом тромбофилиями (серповидно-клеточная анемия, наследственная гиперлипопротеидэмия и прочие).
- Атеросклероз – обширный, распространенный атеросклероз, особенно на поздних стадиях, повреждает стенки сосудов, что приводит к образованию пристеночных тромбов артерий в местах локализации бляшек с последующей возможностью развития инфарктов различных органов.
- Повышенный уровень гормонов надпочечников – длительная высокая активность коры надпочечников при патологическом стрессе или опухоли приводит к повышению образования фибриногена, одного из важных компонентов системы свертывания крови.
- Печеночная и (или) почечная недостаточность – приводят к снижению образования в печени антитромбина III, что повышает свертываемость крови.
- Гемоконцентрация – такое состояние крови, когда нарушается нормальное соотношение клеточных элементов крови и ее жидкой части в сторону увеличения клеточной составляющей, что приводит к сгущению крови. Данное состояние может развиваться вследствие ряда патологических состояний: рвота, понос, потеря жидкости в жарком климате без достаточного питья, мочеизнурение (сахарный и не сахарный диабет), обширные ожоги.
- Септические состояния – в норме кровь человека стерильна, в случае присутствия в крови микроорганизмов (бактерий, грибков, вирусов) развивается состояние, которое называется «сепсис», одним из проявлений которого может быть повышенная свертываемость крови.
- Вынужденное положение тела – лежачее либо малоподвижное положение тела по причине заболевания, травмы, либо операции, приводит к значительному замедлению тока крови особенно в глубоких венах конечностей, что предрасполагает к тромбообразованию в данных сосудах.
- Особенности конституции и образа жизни – вредные привычки (курение, употребление алкоголя, некоторых наркотиков), ожирение и малоподвижный образ жизни приводят к сгущению крови, повреждению стенок сосудов и повышению свертываемости крови.
- Побочные эффекты медицинских препаратов – например, гормональные контрацептивы, содержащие в себе гормоны эстрогены, сами по себе повышают свертываемость крови.
- Инородное тело в сосудистом русле – искусственный клапан сердца, протез сосуда, длительное нахождение катетера в просвете сосуда.
- Травмы – обширные повреждения мягких тканей сопровождаются попаданием в кровь веществ повышающих свертываемость крови.
- Длительное взаимодействие крови с чужеродным объектом – при проведении операций с применением устройств заменяющих работу сердца и легких, при гемодиализе (фильтрации крови «искусственной» почкой) и прочих медицинских вмешательствах сопряженных с обширным контактом крови с инородным предметом.
- Идиопатическая гиперкоагуляция – такое состояние, когда весь комплекс необходимых диагностических манипуляций был проведен, а достоверно установить причину высокой свертываемости крови не удалось.
Симптомы и проявления повышенной свертываемости крови
Течение данного патологического состояния до развития сосудистой катастрофы не имеет специфических клинических проявлений, нередко протекает скрытно и сводится к общим симптомам: повышенной утомляемости, чувству постоянной усталости, слабости, апатии, сонливости, рассеянности, частым головным болям, ощущению покалывания, онемения в кончиках пальцев, кончике носа, в области ушных раковин и прочим, неприятным и клинически малозначимым проявлениям.
Одним из признаков, позволяющих заподозрить гиперкоагуляционный синдром до развития тяжелых клинических проявлений, является сворачивание крови «на игле», когда забор крови из вены произвести затруднительно, поскольку сразу после пункции (прокола) происходит сворачивание крови внутри иглы и прекращается ее поступление в шприц, что вынуждает производить повторные пункции. Также кровь, помещенная в пробирку сразу после ее забора, быстро сворачивается с образованием рыхлого свертка. При нахождении в стационаре может обратить на себя внимание быстрый выход из «рабочего состояния» установленных венозных катетеров как центрального (подключичная, яремная вены), так и периферического (вены предплечья, кисти) по причине их закупорки тромботическими массами, невзирая на соответствующий уход за ними.
Отсутствие своевременной диагностики и лечения повышенной свертываемости крови может стать причиной тяжелых сосудистых катастроф в виде закупорок артериальных и венозных сосудов с самыми неблагоприятными последствиями:
- Инфаркт миокарда;
- Ишемический инфаркт головного мозга (инсульт);
- Инфаркт кишечника;
- Инфаркт легкого;
- Инфаркт почки;
- Гангрена конечностей;
- Тромбозы вен конечностей;
- Тромбоэмболия легочной артерии.
При наличии подозрения на повышенную свертываемость крови необходимо в кратчайшие сроки обратится за медицинской помощью, выполнить все диагностические назначения и строго придерживаться назначенного лечения. Внимательное отношение к данной патологии поможет продлить жизнь и избежать тяжелых, порой крайних последствий.
Диагностика
Существуют показания для проведения диагностических исследований (в том числе и генетических) с целью направленного обнаружения высокой свертываемости крови:
- Случаи наличия тромбоэмболий у близких родственников;
- Наличие тромбозов (венозных или артериальных) в возрасте до 50-ти лет;
- Повторяющиеся тромбозы любой локализации;
- Длительное применение гормональных препаратов содержащих эстрогены, гормоны надпочечников;
- Длительное применение препаратов влияющих на гемостаз, для оценки их эффективности;
- Нормально протекающая беременность;
- Осложненный акушерский анамнез (невынашивание беременности, плацентарная недостаточность, преждевременные роды и прочее);
- Массивные хирургические вмешательства как предстоящие, так и произведенные;
- Длительная иммобилизация (нахождение в вынужденном положении, чаще лежа);
- Злокачественные новообразования.
Для определения состояния системы гемостаза проводят комплексный анализ крови взятой из локтевой вены, который называется коагулограмма или гемостазиограмма и включает в себя определение целого ряда параметров:
- Время свертываемости крови (по Ли-Уайту, а также Масс и Магро);
- Время кровотечения (по Дюку, Айви, Шитковской)
- Протромбиновое время по Квику (ПВ);
- Международное нормализованное отношение (МНО);
- Активированное время рекальцификации (АВР);
- Растворимые фибрин-мономерные комплексы (РФМК);
- Фибриноген;
- Протромбиновый индекс (ПТИ);
- Тромбиновое время (ТВ);
- Активированное частичное тромбопластиновое время (АЧТВ);
- Тромбиновое время;
- Антитромбин III (АТ III);
- D-димер.
Также существенное значение для диагностики состояния гемостаза имеют показатели общего анализа крови, гематокрита и кислотно-щелочного взаимоотношения крови.
Проведение вышеперечисленных анализов крови даст общее представление о состоянии системы гемостаза, при этом изначальные причины, вызвавшие патологию системы свертывания крови, могут остаться не диагностированными и потребовать более широкого обследования, объем и методы которого, определяет врач.
Повышенная свертываемость крови при беременности
Будучи в состоянии беременности женский организм претерпевает ряд кардинальных физиологических (не являющихся патологией) изменений, которые отражаются на системе свертывания крови в виде угнетения противосвертывающей системы крови и активации свертывающей. Данные изменения начинают отмечаться со второго триместра беременности (с 4-го 5-го месяцев) и играют важнейшую защитную роль, как для организма матери, так и ребенка. Изменения в системе гемостаза при беременности обусловлены тем, что кровоснабжение места прикрепления плаценты к матке очень интенсивное и система гемостаза подстраивается таким образом, чтобы не вызвать тромбообразования в матке при вынашивании беременности, а также обеспечить быструю остановку кровотечения во время родовой деятельности и непосредственно после нее.
Бдительный контроль системы гемостаза при беременности жизненно необходим и достигается регулярными исследованиями свертываемости крови. Внимательно относится к назначениям врача и регулярно сдавать анализы с целью диагностики состояния свертывающей системы крови необходимо, чтобы с одной стороны вовремя обнаружить патологически повышенную свертываемость крови и предотвратить возможную плацентарную недостаточность, а с другой стороны оценить возможность остановки кровотечения собственными силами организма для того, чтобы роды прошли без угрозы жизни матери.
Особенно внимательно к состоянию системы гемостаза следует отнестись будущим мамам, у которых есть факторы риска:
- Беременность в возрасте старше 40-ка лет;
- Беременность в возрасте до 18-ти лет;
- Сахарный диабет;
- Заболевания почек, печени, сердечно-сосудистой системы;
- Наличие наследственных заболеваний у беременной, отца и близких родственников;
- Тяжелые санитарно-бытовые условия матери;
- Частые стрессы.
Несмотря на то, что вынашивание ребенка не является заболеванием, а относится к физиологическим состояниям, беременная женщина и ее ближайшее окружение, должны внимательно относится к назначениям врача, выполнять все рекомендации, бережно следить за здоровьем будущей мамы и ни в коем случае не заниматься самолечением.
Лечение повышенной свертываемости крови
Терапия гиперкоагуляционного синдрома производится с учетом причин его обусловившего:
- В случае наличия верифицированного (подтвержденного) генетического дефекта производится заместительная терапия – введение недостающего компонента извне, либо удаление избыточного или дефектного компонента свертывающей системы крови методом аппаратного очищения крови.
- В случае эритремии избыточные эритроциты удаляются эритроцитоферезом.
- При повышенной склонности тромбоцитов к агрегации применяют антиагреганты (аспирин, тиклид, дипиридамол).
- При повышенной склонности тромбоцитов к коагуляции применяют низкомолекулярные гепарины (фраксипарин, клексан, фрагмин).
- При повышенной свертываемости крови вызванной инфекционным процессом, назначают этиотропное, направленное на возбудителя, лечение (антибиотики, противогрибковые и прочие препараты), а также введение нефракционированного гепарина.
- При патологии связанной с образованием иммунных комплексов на фоне различных видов плазмафереза применяют низкомолекулярные гепарины.
- При аутоимунных заболеваниях совместно применяются плазмоферез, антикоагулянты (гепарин), антиагреганты (тиклид или плавикс) стероидные противоваспалительные препараты (дексометазон) и цитостатики (винкристин, циклофосфан).
- При поражении сосудов атеросклерозом на фоне стандартного лечения ишемической болезни сердца применяются антиагреганты (аспирин, тиклид, плавикс), нередко данные препараты назначают в комбинациях (аспирин + плавикс) в корректных дозах под контролем состояния гемостаза.
- При длительном контакте с чужеродными объектами профилактически назначают антикоагулянты (синкумарин, варфарин) и антиагреганты (ацетилсалициловую кислоту, плавикс).
- В случае частого применения аппаратных методов очищения крови (диализ, фильтрация, различные виды ферезов) преимущественно применяют гепарин.
- В случае сгущения крови связанной с обширными травмами для стабилизации системы гемостаза применяют переливание свежезамороженной донорской плазмы и солевых растворов, поскольку данное состояние имеет риск развития ДВС-синдрома.
Также, особенно в легких случаях гиперкоагуляционного синдрома, не стоит сбрасывать со счетов народную медицину. Гирудотерапия (лечение пиявками), апитерапия (лечение укусами пчел), фитотерапия (лечение растениями) могут оказывать достаточно выраженный и продолжительный эффект, при этом, следует помнить, что указанные виды народной медицины имеют клинически доказанную эффективность, а также ряд противопоказаний, следовательно, контролировать состояние организма и свертывающей системы крови необходимо также тщательно, как и при лечении официнальными (промышленными) препаратами.
Зачастую бывает так, что повышенная свертываемость крови есть, а ее причина не установлена, либо нет времени и возможности ее установить. В подобных ситуациях, оправдано, с целью снижения риска развития сосудистой катастрофы и по жизненным показаниям, лечение проявления болезни – самой повышенной свертываемости крови, а не причины ее вызвавшей.
Видео: программа о гемостазе, свертываемости крови
К сожалению, научно-технический прогресс имеет свои минусы. Темп жизни стал намного интенсивнее. Человек много времени проводит в офисах, а прогулкам на свежем воздухе предпочитает тот же компьютер, только в домашних условиях. На всё это остро реагирует организм человека, в частности, сердечно-сосудистая система.
Всё чаще молодые люди жалуются на головные боли и плохое самочувствие. В основном причиной этому является вегетососудистая дистония (ВСД), артериальная гипер- и гипотензия. Поэтому каждый должен не только постоянно контролировать кровяное давление, но и уметь правильно это делать.
Тонометр не показывает давление
Артерии и методы измерения давления
Артерии – это сосуды, по которым кровь движется от сердца к органам. Основная задача артерий – нести кровь, поступающую из сердца под определенным давлением. Чтобы выполнить эту цель, артерии имеют специальное строение.
Стенка артериального сосуда состоит из трех слоев:
- Эндотелий или внутренний слой (контролирует компоненты свертывания крови);
- Средняя оболочка. Состоит из мышечных и эластичных волокон. Мышечные волокна корректируют артериальное давление путем вазоконстрикции (сужения просвета сосуда) и вазодилятации (расширения просвета сосуда). Эластичные волокна создают условия для распространения волны давления (пульсовой волны);
- Адвентициальный слой (прикрепляет сосуд к прилегающим тканям).
Сила, с которой кровь давит на стенки сосудов, называется кровяным давлением.
Этот показатель можно измерить на разных участках сердечно-сосудистой системы, в связи с этим различают такие виды давления:
- капиллярное;
- внутрисердечное;
- артериальное;
- венозное;
- центральное артериальное и венозное.
Когда тонометр перестал показывать давление
Особую диагностическую ценность представляет артериальное давление (АД). При несложной методике измерения, оно сполна характеризует текущее состояние здоровья человека и позволяет вовремя реагировать на все негативные изменения.
В наше время артериальное давление измеряют двумя основными способами:
- Инвазивный метод;
- Неинвазивные способы.
Инвазивная методика
Дает постоянную и истинную информацию об артериальном давлении. Позволяет исследовать газовый и кислотно-щелочной состав крови, поэтому она считается «золотым стандартом» в измерении АД.
Эта методика нашла свое применение во время операций, при создании так называемой управляемой гипотонии. Делает возможным также в режиме реального времени контролировать эффективность терапевтических действий при неотложных состояниях (шок, приступ бронхиальной астмы).
Система для инвазивного измерения давления состоит из:
- Катетера или канюли;
- Магистрали высокого давления (система трубочек, по которым кровь идет к датчикам);
- Трансдьюсера (устройство, преобразующее физические или химические сигналы в электрические импульсы);
- Монитора, на который выводится кривая давления и газовый состав крови.
Распространенные ошибки при измерении давления
Чаще всего катетеризация проводится в лучевой артерии, так как она расположена поверхностно и имеет много коллатералей.
Равным образом можно использовать такие артерии:
- локтевую;
- плечевую;
- подмышечную;
- бедренную;
- тыльную артерию стопы.
Механизм действия
Кровь по катетеру и системе трубочек попадает в трансдьюсер. В трансдьюсере происходит ее анализ. Проанализированная информация подается на монитор в виде кривой линии (для артериального давления) и отображает цифры показателей газового и кислотно-основного состояния крови пациента.
Осложнения
К возможным осложнениям относят:
- гематома;
- тромбоэмболия или воздушная эмболия;
- повреждение нервов;
- тромбоз артерии;
- инфекция.
Если тонометр показывает те самые 120/80
Неинвазивные способы
- Электронные. В основе электронного измерения артериального давления лежит регистрация и анализ датчиками различных параметров сосудов. В зависимости от того какие данные кровяного сосуда используются для вычисления давления, различают такие методы:
- осциллометрический (измеряется изменения объема сосуда);
- тахоосциллографический (анализируется скорость распространения пульсовой волны);
- компенсационный (оценивается эластичность и объем сосудов пальца).
Преимущества:
- для использования этого метода не требуется специальных навыков;
- человеческий фактор (невнимательность, плохое зрение) не влияет на результат, так как измерение осуществляется с помощью электронных датчиков;
- позволяет измерять давление через тонкую одежду;
- дает достоверный результат при шумовых нагрузках;
- делает возможным измерять АД при слабых тонах, в случаях аускультативных провалов или когда возникает бесконечный тон;
- показывает более точные данные в режиме суточного мониторинга, чем аускультативный метод.
Недостатки:
- неэффективен при аритмиях;
- результат зависит от неподвижности руки;
Как избежать проблем с тонометром
- компенсационный метод рационально использовать на пациентах до 45 лет. Так как точность измерения этим методом сильно зависит от эластичности сосуда. У пациентов после 45 лет намного выше процент изменения стенки сосуда атеросклерозом, чем у молодых людей.
- Аускультативный (механический) метод Короткова. С начала XX века, когда он был впервые предложен Н. С. Коротковым, до наших дней методика не претерпела серьезных изменений. Для того чтобы провести измерения давления, используют фонендоскоп и манометр. Фонендоскоп предназначен для выслушивания тонов сердечной деятельности.
Тонометр имеет такие части:
- манометр (ртутный или пружинный);
- манжета, соединённая с резиновой «грушей»;
- «груша», предназначенная для нагнетания воздуха;
В основе метода лежит полное пережатие плечевой артерии раздутой манжетой и аускультация шумов, возникающих после постепенного уменьшения давления воздуха в манжете. Появление первого звукового толчка соответствует значению систолического давления, зафиксированному на шкале манометра, а момент исчезновение тонов – диастолическому значению.
- является наилучшей неинвазивной методикой диагностирования артериального давления;
- устойчив к движениям руки пациента.
Тонометр Nissei измеряет давление дважды
- зависит от зрения и слуха человека, проводящего измерение;
- затруднено его использование в шумной обстановке;
- чувствителен к расположению головки фонендоскопа по отношению к центру артерии.
Типичные ошибки
Ошибка № 1. Неправильный выбор манжеты
Чаще всего в практике используют запястные или плечевые тонометры. Тонометр с плечевой манжетой подходит для большинства людей.
Запястные тонометры менее универсальны. Точность их результата много в чем зависит от состояния сосудов пациента. С возрастом или под влиянием атеросклероза сосуды теряют свою эластичность и проходимость, вследствие чего слабее передают пульсовую волну.
Поэтому не советуют использовать этот вид тонометров таким категориям людей:
- страдающим ожирением;
- старше 40 лет;
- больным сахарным диабетом.
В связи с этим рекомендуется выбирать аппарат с манжетой, которая надевается на плечо. Это позволит использовать тонометр всем членам семьи.
Ошибка № 2. Неправильный размер манжеты
Как правильно выбрать манжету для тонометра
Важным является также правильный размер манжеты. Так как в случае если манжета по длине большая, показатели давления будут занижены, при маленькой манжете – завышены.
Различают три категории манжет по длине окружности конечности:
- детские (от 8 до 19 см);
- взрослые (от 17 до 40 см);
- манжеты для измерения артериального давления на бедре (от 38 до 50 см).
Чтобы выбрать оптимальную по размеру манжету, нужно придерживаться таких правил:
- длина манжеты должна составлять не менее 4/5 от длины окружности плеча;
- ширина должна быть равна примерно 2/5 от длины окружности плеча.
Ошибка № 3. Неправильное положение тела
Измерение давления проводят в положении лежа или сидя.
Точность результата много в чем зависит от соблюдения таких правил:
- Нельзя скрещивать ноги или сгибать спину во время измерения АД. Так как этим вы повышаете внутрибрюшное давление, увеличивая тем самым показатели АД.
- Недопустимо держать руку, на которой проводится измерение, на весу.
- Рука, на которой наложена манжета, должна быть на уровне сердца. В положении сидя – на высоте нижнего конца грудины. В положении лежа – вдоль тела. Каждое отклонение на 10 см ведет к погрешности результата на 8 мм рт. ст. Соответственно, когда рука будет выше сердца, результат измерения будет повышен, если ниже – снижен.
Как правильно надевать манжету тонометра
Ошибка № 4. Неправильное наложение манжеты
Недопустимо накладывание манжеты поверх одежды. Во-первых, одежда создает дополнительное давление на сосуды, что ведет к неправильным результатам.
Во-вторых, через ткань хуже проводится звук. То есть, тот, кто измеряет давление, попросту может не услышать первый и последний толчок.
Нужно также учитывать, что на разных участках тела разное давление.
К примеру, давление у одного и того же пациента в норме:
- при измерении на плечевой артерии – 120/80 мм рт. ст.;
- при измерении на запястной артерии – 110/75 мм рт. ст.;
- при измерении на бедре – 140/85 мм рт. ст.
Общие рекомендации
- Манжета должна соответствовать размеру руки по длине и ширине.
- Проводите измерения в тихом и комфортном помещении.
- Расположитесь удобно, так, чтобы ноги не были скрещены. Рука, на которой проводится измерение, не должна быть на весу. А также нужно, чтобы одежда не сковывала конечность.
- Нижний край манжеты необходимо наложить на 3 см выше локтевой ямки.
- Разместите головку стетоскопа над локтевой ямкой. Нужно, чтобы мембрана располагалась вплотную с кожей. Но не переусердствуйте, процедура измерения давления не должна вызывать болевых ощущений у обследуемого.
Правила измерения артериального давления
- Удерживайте руку на уровне нижнего конца грудины. Для этого под локоть можно подложить кулак другой руки или подушку.
- Энергично накачивайте воздух в манжету.
- Выпускать воздух из манжеты нужно медленно. Примерно 3–4 мм рт. ст. в секунду. При такой скорости удастся более точно услышать момент появления первого и последнего ударов.
- При проведении измерения, желательно не разговаривать и не делать резких движений.
- Если тонометр не показывает давления, проверьте, не пропускает ли воздух манжета или система трубок. Причина поломки может также скрываться в манометре. В этом случае рекомендуется обратиться к специалисту.
- Повторное исследование давления рекомендуется проводить с интервалом в 10 минут.
Основные правила подготовки к замеру
Как и любое медицинское исследование, измерение давления, имеет свои особенности подготовки.
К этим особенностям относят:
- За полчаса до начала измерения АД нужно прекратить курение и физические нагрузки.
- Нужно учитывать, что алкоголь, крепкий чай или кофе изменяют артериальное давление. То же самое относится к приему ванны или душа, независимо – холодного или горячего.
- Наполненный мочевой пузырь повышает внутрибрюшное давление, а оно, в свою очередь, общее артериальное. Поэтому рекомендуется опустошить мочевой пузырь перед замером АД.
- Предварительно нормализуйте дыхание. Для этого сделайте 10 глубоких вдохов.
- Некоторые люди имеют скрытое волнение перед сотрудниками медицины – так называемый синдром белого халата. Это может отразиться в повышенных показателях АД. В связи с этим следует подождать некоторое время (5–10 минут), чтобы человек успокоился.
Заключение
Артериальное давление является одним из важных показателей деятельности организма. Его отклонение от нормы (диапазон от 100/60 до 139/89 мм рт. ст.) ведет ко многим патологическим состояниям или является их следствием. По данным ВОЗ, каждый год смертность в связи с заболеваниями сердечно-сосудистой системы составляет 50% от числа всех смертей. Сердечно-сосудистые заболевания считаются «эпидемией» двадцать первого века.
В связи с этим за показателями давления нужно следить не только людям из групп риска (страдающих ожирением, сахарным диабетом, плохой наследственностью), но и каждому человеку. Описанные выше рекомендации и правила помогут свести к минимуму ошибки при измерении артериального давления. Такой подход позволяет значительно увеличить качество и длительность жизни. Ведь лучшее лечение – это профилактика.
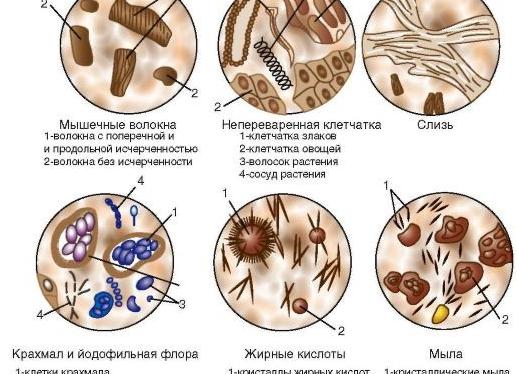

Комментарии 0