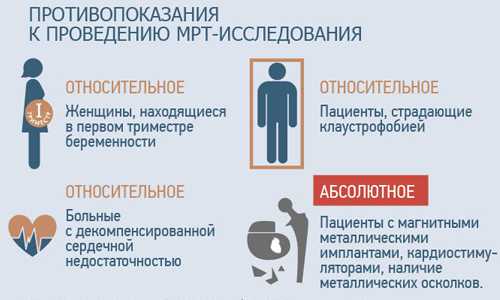
Что такое эрадикационная терапия
Эрадикация – что это такое, цели и задачи терапии, использование медикаментов и народных рецептов, диета
Язвенная болезнь доставляет пациентам много неприятностей. Чтобы справиться с патологией, используют комплекс мероприятий. Эрадикация – это метод лечения, главная задача которого – устранение инфекции, восстановление организма. Стоит разобраться, какие препараты при этом используются, как проводятся процедуры.
Эрадикационная терапия направлена на уничтожение в организме вирусов или бактерий. Поскольку огромной проблемой в медицине является поражение органов ЖКТ бактериями Helicobacter Pylori, разработана методика противодействия этим микроорганизмам. В такой ситуации показаниями для эрадикации могут быть:
- гастроэзофагальный рефлюкс (заброс в пищевод содержимого желудка);
- предраковые состояния;
- последствия операции по удалению злокачественной опухоли;
- язвенная болезнь желудка, двенадцатиперстной кишки;
- MALT-лимфома желудка (опухоль лимфоидных тканей).
Эрадикация Helicobacter Pylori назначается пациентам, у которых планируется длительное лечение нестероидными противовоспалительными препаратами. Показанием для применения методики нередко становятся:
- хронический атрофический гастрит;
- гастропатия (воспалительные заболевания слизистых оболочек, сосудов желудка от воздействия лекарств);
- аутоиммунная тромбоцитопения (отторжение иммунной системой собственных тромбоцитов);
- железодефицитная анемия;
- профилактика людям, имеющим родственников, у которых в анамнезе рак желудка.
Эрадикация Хеликобактер пилори – особый способ лечения. Он направлен на создание больному благоприятной атмосферы для проведения процедур. Методика ставит несколько целей:
- сократить продолжительность лечения;
- создать комфортные условия для соблюдения режима;
- ограничить количество наименований употребляемых лекарств – применяются комбинированные средства;
- устранить необходимость соблюдения строгой диеты;
- предотвратить развитие побочных эффектов;
- ускорить заживление язв.
Экадикация пользуется популярностью у врачей и пациентов благодаря экономичности – применяются недорогие препараты, и эффективности – состояние улучшается с первых дней терапии. Процедуры преследуют такие цели:
- сократить число приемов препаратов за сутки – назначаются лекарства с пролонгированным действием, увеличенным периодом полувыведения;
- преодолеть устойчивость бактерий к антибиотикам;
- предоставить альтернативные схемы эрадикации при наличии аллергии, противопоказаний, в отсутствие результатов лечения;
- снизить токсическое воздействие лекарств.
Требования к эрадикации, рекомендованные ВОЗ
Медики всего мира, занимающиеся вопросами инфекций, вызванных Хеликобактер пилори, пришли к международным соглашениям. Они включают создание стандартов и схем, повышающих эффективность диагностических и лечебных методик, именуются Маастрихт. Информация регулярно обновляется, на сегодняшний день содержит такие требования к эрадикации:
- наличие положительных результатов лечения у 80% пациентов;
- длительность терапии не больше 14 дней;
- применение лекарств с низким уровнем токсичности.
Рекомендации Маастрихт содержат такие требования к проведению лечебных процедур:
- взаимозаменяемость лекарственных средств;
- сокращение частоты приема препаратов;
- небольшая резистентность (устойчивость) штаммов Хеликобактер пилори к лекарствам;
- простота использования схем терапии;
- появление побочных эффектов не больше, чем у 15% больных, их действие не должно мешать проведению лечебных процедур.
Медики пришли к выводу, что предлагаемые методики уменьшают количество возникающих осложнений. Рекомендованы две линии проведения эрадикации, которые требуют соблюдения такой последовательности:
- Процесс лечения начинают со схем первой линии.
- При отсутствии положительных результатов переходят на вторую.
- Контроль лечения проводят через месяц после выполнения курса всех мероприятий.
Препараты
Для эрадикации используют несколько групп медикаментозных препаратов. Они входят в схемы проведения лечебных мероприятий. Для противодействия бактерии Helicobacter Pylori обязательным является применение антибиотиков. Врачи назначают лекарства с учетом противопоказаний и побочных действий. Результативностью отличаются такие препараты из групп противобактериальных средств:
- пенициллины – Амоксиклав, Амоксициллин;
- макролиды – Азитромицин, Кларитромицин;
- тетрациклины – Тетрациклин;
- хлорфторинолы – Левофлоксацин;
- ансамицины – Рифаксимин.
Во вторую группу препаратов, применяемых при эрадикации Хилобактер пилори, входят противоинфекционные медикаментозные средства. Они отличаются высокой токсичностью, врачи должны учитывать противопоказания для применения. Схема проведения эрадикации включает такие лекарственные препараты:
- Метронидазол;
- Нифурател;
- Тинидазол;
- Макмирор.
Высокую результативность по противодействию бактерии Helicobacter Pylori показывают висмутсодержащие средства. Эти лекарства устойчивы к влиянию кислой среды желудка, образуют на слизистой оболочке защитную пленку, ускоряют рубцевание изъязвлений. Препараты, используемые при эрадикации, имеют минимум побочных эффектов и противопоказаний. В эту группу входят такие средства:
- Субсалицилат висмута;
- Де-Нол;
- Субнитрат висмута.
В схему лечения язвенной болезни методом эрадикации включают ингибиторы протонного насоса (ИПН). Эти препараты уменьшают агрессивное действие кислотной среды на слизистые оболочки. Лекарства создают губительные условия для существования микроорганизмов. ИПН оказывают антацидное действие – нейтрализуют соляную кислоту. Средства уничтожают бактерии, которые в ней комфортно существуют. Группа включает такие препараты:
- Рабепразол;
- Омепразол (Омез);
- Пантопразол (Нольпаза);
- Эзомепразол;
- Лансопразол.
Схемы эрадикации Хеликобактер пилори
Методики лечения язвенной болезни желудка и двенадцатиперстной кишки постоянно совершенствуются. Это происходит благодаря исследованиям, проводимым медиками всего мира. Первые схемы эрадикации Хеликобактер пилори включали два способа:
- Монотерапия. В этой методике предполагается использование антибиотиков или висмутсодержащих средств. Из-за низкой эффективности она применяется редко.
- Двухкомпонентная схема эрадикации. Отличается использованием обеих групп лекарств из первой методики, имеет результативность 60%.
Исследования ученых-медиков привели к созданию новых схем эрадикации, которые были предложены на Маастрихтских конференциях. Современные методы включают:
- Трехкомпонентную терапию, характеризующуюся эффективностью 90%. К двойной схеме лечения добавляются противоинфекционные средства.
- Четырехкомпонентную эрадикацию, которая содержит как дополнение к предыдущему варианту ингибиторы протонного насоса. Метод достигает положительных результатов в 95% случаев.
Схема эрадикации Хеликобактер пилори может быть использована в нескольких версиях. Лечение начинают с первой линии. Врачи подбирают лекарства в зависимости от состояния пациента, длительность лечения может быть увеличена до двух недель. Стандартная трехкомпонентная схема включает применение таких средств:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| ИПН по выбору врача: Омепразол, Рабепразол | 40 | 2 | 7 |
| Кларитромицин | 500 | 2 | |
| Амоксициллин | 4 |
Если есть необходимость, то врачи назначают четырехкомпонентную схему эрадикации. Она предполагает использование таких лекарств:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
|
Висмута трикалия дицитрат | 120 | 4 | 10-14 |
| Кларитромицин | 500 | 2 | |
| Амоксициллин | 4 | ||
| Эзомепразол или Омепразол | 40 | 2 |
Если у пациента в результате анализов при диагностике выявлена атрофия слизистых оболочек, используется методика эрадикации без применения ингибиторов протонного насоса. Схема включает такие лекарства:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| Висмута трикалия дицитрат | 120 | 4 | 10-14 |
| Кларитромицин | 500 | 2 | |
| Амоксициллин | 4 |
Если лечение язвы желудка, вызванной бактерией Хеликобактер пилори, требуется пациентам пожилого возраста, используется усеченная схема эрадикации. Она включает применение таких медикаментозных средств:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| Висмута трикалия дицитрат | 120 | 4 | 14 |
| Амоксициллин | 500 | 4 | |
| Ленсопразол или Пантопразол | 40 | 2 |
Если применяемые схемы эрадикации не дали результатов, назначаются следующие варианты лечения. Вторая линия подразумевает использование трех схем, все они четырехкомпонентные. Первая схема включает такие лекарства:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| Висмута трикалия дицитрат | 120 | 4 | 14 |
| Тетрациклин | 500 | 4 | |
| Омепразол или Пантопразол | 40 | 2 | |
| Метронидазол | 500 | 3 |
Прежде чем назначить препараты, врачи проводят анализы, выявляют возбудителя и его чувствительность к антибиотикам. Вторая схема эрадикации предполагает комбинацию таких средств:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| Висмута субсалицилат | 120 | 4 | 14 |
| Амоксициллин | 500 | 4 | |
| ИПН – Омепразол или Эзомепразол | 40 | 2 | |
| Нуфантел | 400 | 2 |
Во всех вариантах эрадикации врачи дополнительно назначают витаминные комплексы. Схема №3 – четырехкомпонентная терапия, которая включает такие лекарства:
| Препарат | Дозировка, мг | Количество приемов в день | Длительность лечения, дни |
| Висмута трикалия дицитрат | 120 | 4 | 14 |
| Тетрациклин | 500 | 4 | |
| Индикаторы протонного насоса по выбору врача | 40 | 2 | |
| Рифаксимин | 500 | 3 |
Питание при лечении
Во время эрадикации не требуется соблюдение специальной диеты. Исключение составляют кровотечение в желудке, прободения язвы. В остальных случаях диетологи рекомендуют включить в рацион:
- домашние сухари;
- нежирные супы;
- речную рыбу;
- макароны;
- нежирное мясо;
- каши на молоке и на водной основе;
- растительное масло;
- овощи – отварные или запеченные – картофель, морковь, кабачки, свеклу;
- компоты из ягод;
- кисели;
- чай.
В период эрадикации желательно использовать блюда в теплом виде – горячие или холодные действуют на желудок раздражающе. Под запретом находятся:
- острые, жирные соусы;
- алкоголь;
- жареные блюда;
- жирные бульоны;
- копчености;
- консервы;
- маринады;
- жирная рыба, мясо;
- острые приправы;
- фрукты, овощи в сыром виде (в период обострения);
- грибы;
- перец;
- сладости;
- торты;
- чеснок;
- лук;
- крепкий кофе, чай.

Народные средства
Домашнее лечение не может заменить эрадикацию, назначенную врачом. Народные средства будут дополнением к схемам терапии. Важно согласовать их с доктором. Чтобы ускорить заживление язвы, принимают отвар льняного семени, который обладает обволакивающим действием на слизистую желудка. Для его приготовления потребуется:
- Взять чайную ложку семян.
- Залить их стаканом кипящей воды.
- Настоять под крышкой 2 часа.
- Взболтать, чтобы семя отделилось от слизи.
- Процедить.
- Выпить в течение дня за 4 приема.
Народные целители рекомендуют при язвенной болезни применять раз в сутки, перед завтраком, сырые куриные яйца. Курс лечения – две недели. Противомикробным действием обладает отвар из зверобоя и тысячелистника. Для его приготовления необходимо:
- Взять по 100 грамм каждой травы.
- Добавить литр кипятка.
- Настоять 30 минут.
- Процедить.
- Принимать по 100 мл до еды трижды в день.
- Курс терапии – месяц.
При лечении язвенной болезни, вызванной бактериями Хеликобактер пилори, рекомендуют использовать прополис. Лечение необходимо согласовать с врачом. Прополис является природным антибактериальным средством, регулирует кислотность желудка. Народные целители рекомендуют такой рецепт:
- Заморозить 50 г прополиса, чтобы легче было измельчить.
- Взять 0,5 литра молока.
- Добавить измельченный прополис.
- Поставить на водяную баню на 30 минут.
- Положить ложку меда.
- Пить по стакану в теплом виде на ночь.
- Можно хранить в холодильнике 48 часов.
- Продолжительность лечения – от двух недель.
Нормализация микрофлоры после эрадикации
Применение антибиотиков приводит к нарушению микрофлоры кишечника. Чтобы восстановить состояние после процедуры эрадикации, используют препараты двух групп. Одна из них – пробиотики, которые содержат в составе живые микроорганизмы – бифидобактерии, лактобактерии. Врачи назначают такие препараты:
- Энтерол;
- Линекс;
- Аципол;
- Биоспорин;
- Бифиформ;
- Лактобактерин;
- Бификол;
- Лактоферон;
- Споробактерин;
- Флорадофилус;
- Витанар;
- Гиалакт;
- Колибактерин;
- Бифидумбактерин.

Вторая группа – пребиотики, которые создают условия для размножения полезных микроорганизмов. Препараты останавливают развитие патогенных бактерий, восстанавливают биологическую среду кишечника. После прохождения эрадикации пациенты принимают такие препараты:
- Порталак;
- Хилак-Форте;
- Дюфалак.
Видео
Выбор схемы эрадикационной терапии при helicobacter pylori в случае необходимости повторного лечения
КомментарииОпубликовано в журнале: «Врач», 2008, №4, с. 64-67
Т. Лапина, кандидат медицинских наук, ММА им. И. М. Сеченова
Лечение при инфекции Helicobacter pylori (Hp) можно считать детально разработанным: по комбинации лекарственных средств, их дозам и продолжительности курса оно стандартизировано. В России эта терапия утверждена в соответствующих стандартах медицинской помощи и Формулярной системе. Национальные рекомендации многих европейских стран и отечественные стандарты по диагностике и лечению при Нр основаны на алгоритмах, разработанных под эгидой Европейской группы по изучению этой инфекции. Поскольку первые конференции по выработке данного консенсуса прошли в Маастрихте, рекомендации носят название Маастрихтских (конференции проходили в 1996, 2000 и 2005 гг.).
Схемы эрадикационной терапии строго регламентированы, кажется, что такое лечение не должно вызывать вопросов. Однако выполнение любого стандарта на практике не всегда сопровождается стопроцентной эффективностью. Большинство наиболее острых вопросов касаются выбора схемы лечения после неудачи первой (а иногда второй и третьей) попытки.
Почему же при Нр иногда требуется проведение повторного курса эрадикационной терапии (в англоязычной литературе для его обозначения используют термин «терапия второй, третьей линии»)? В качестве показателя, свидетельствующего об оптимальности схемы лечения, все Маастрихтские рекомендации [9, 16, 17] называют 80% эрадикацию Нр. Это означает, что процент эрадикации микроорганизма по критерию intention-to-treat должен быть равен или превышать 80%. Этот «целевой» процент успешной эрадикации предложен на основании анализа данных множества клинических исследований различных схем лечения, их доступности и переносимости; он учитывает и характеристики Нр (чувствительность микроорганизма к лекарственным средствам, особенности среды обитания). Стабильно высокий процент уничтожения микроорганизма должен быть легко воспроизводим при лечении в разных популяциях и разных регионах и странах.
Решающее значение имеет, безусловно, терапия первой линии, которая должна быть нацелена на достижение эрадикации Hр у максимального числа больных. В качестве терапии первой линии Маастрихтские рекомендации III предлагают следующие трехкомпонентные схемы лечения (табл. 1): ингибитор протонной помпы в стандартной дозировке 2 раза в день+кларитромицин – 500 мг 2 раза в день+амоксициллин – 1000 мг 2 раза в день или метронидазол – 400 или 500 мг 2 раза в день. Минимальная продолжительность тройной терапии – 7 дней, однако оказалось, что для данной схемы более эффективен 14-дневный курс лечения (на 12%; 95% доверительный интервал – ДИ: 7–17%) [12]. Тем не менее 7-дневная тройная терапия может быть признана приемлемой, если местные исследования показывают, что она высокоэффективна. Рекомендуется одинаковая терапия первой линии для всех стран, хотя в разных странах могут быть одобрены разные дозы лекарственных средств [17].
Таблица 1. Схемы стандартной тройной терапии при Нр
| 1-й компонент | 2-й компонент | 3-й компонент |
| Ингибитор протонной помпы: лансопразол – 30 мг 2 раза в день или омепразол – 20 мг 2 раза в день или пантопразол – 40 мг 2 раза в день или рабепразол – 20 мг 2 раза в день или эзомепразол – 20 мг 2 раза в день | Кларитромицин – 500 мг 2 раза в день | Амоксициллин – 1000 мг 2 раза в день или Метронидазол – 400 или 500 мг 2 раза в день |
Четырехкомпонентная схема лечения включает в себя ингибитор протонной помпы в стандартной дозе 2 раза в день+висмута субсалицилат/трикалия дицитрат – 120 мг 4 раза в день+метронидазол – 500 мг 3 раза в день+тетрациклин – 500 мг 4 раза в день (табл. 2). В Маастрихтских рекомендациях II за четырехкомпонентной схемой была закреплена позиция терапии второй линии [16]. Одно из новых положений Маастрихтских рекомендаций III – возможность применения такой схемы в определенных клинических ситуациях, как терапии первой линии (альтернативная терапия первой линии) [17].
Таблица 2. Схемы четырехкомпонентной эрадикационной терапии при Нр
| 1-й компонент | 2-й компонент | 3-й компонент | 4-й компонент |
| Ингибитор протонной помпы: лансопразол – 30 мг 2 раза в день или омепразол – 20 мг 2 раза в день или пантопразол – 40 мг 2 раза в день или рабепразол – 20 мг 2 раза в день или эзомепразол – 20 мг 2 раза в день | Висмута субсалицилат/ субцитрат – 120 мг 4 раза в день | Метронидазол – 500 мг 3 раза в день | Тетрациклин – 500 мг 4 раза в день |
Почему претерпели изменения представления об оптимальной терапии первой линии в Маастрихтских рекомендациях? Почему поиск лучших режимов лечения не прекращается? Появились результаты клинических исследований стандартной тройной терапии (ингибитор протонной помпы +амоксициллин+кларитромицин) в разных странах, согласно которым «целевая» эрадикация не достигается, т.е. она ниже 80% [14]. Наиболее значимая причина снижения эффективности стандартной эрадикационной терапии – резистентность микроорганизма к антимикробным агентам. В Маастрихтских рекомендациях III большое внимание уделено вопросам планирования лечения в зависимости от чувствительности Hp к антибактериальным средствам. Так, комбинация «ингибитор протонной помпы+кларитромицин+амоксициллин или метронидазол» остается рекомендуемой терапией первой линии для популяций с частотой резистентных штаммов к кларитромицину менее 15–20%. В популяциях с частотой резистентности к метронидазолу менее 40% предпочтительнее схема «ингибитор протонной помпы+кларитроми-цин+метронидазол» [17].
Остановимся подробнее на проблеме резистентности Hp к антибиотикам. Согласно международным данным, резистентность Нр к амоксициллину либо равна 0, либо она менее 1%. Имеются крайне редкие сообщения о формировании резистентности из-за мутации pbp-1A-гена. Таким образом, резистентность к амоксициллину – крайне редкое явление, не имеющее клинического значения. Такую же редкость представляет собой резистентность к тетрациклину, которая во многих странах вообще не описана. Она обусловлена мутацией 3 смежных нуклеотидов в гене 16S rRNA (AGA 926–928→TTC). По экспериментальным данным, если мутация возникает лишь в 1 или 2 из этих нуклеотидов, резистентность клинически незначима; лишь тройственная мутация приводит к стабильной резистентности, которая способна оказать влияние на исходы лечения [18].
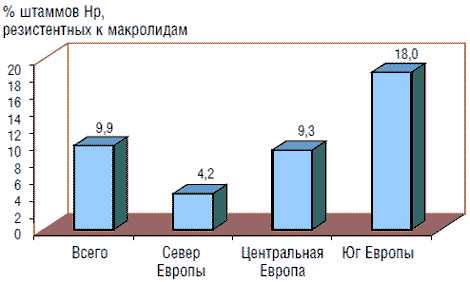
Принципиальное значение имеет чувствительность Hp к кларитромицину и метронидазолу. Количество резистентных штаммов Hp к кларитромицину, по данным мультицентрового европейского исследования, в среднем составляет 9,9% (95% ДИ: 8,3–11,7). Выявлены существенные различия этого показателя: в странах Северной Европы частота резистентности к кларитромицину низкая (4,2%; 95% ДИ: 0–10,8%); в Центральной и Восточной Европе она выше (9,3%; 95% ДИ: 0–22%) и самая высокая – на юге Европы (18%; 95% ДИ: 2,1–34,8%) (рис. 1) [13]. Риск возникновения резистентности к кларитромицину связан с частотой назначения макролидов в данной группе населения. В связи с тем что в ряде европейских стран в педиатрической практике широко назначали макролиды по поводу, например, респираторных заболеваний, частота резистентности штаммов Hp к кларитромицину у детей весьма высока, что делает проблемой выбор тактики эрадикационной терапии.
Рис. 1. Распространенность штаммов Hp, резистентных к макролидам, в европейских странах (по Glupczynski Y. и соавт., 2000)
Ответственна за резистентность к кларитромицину мутация гена 23S rDNA, которая ведет к нарушению пространственной конфигурации рибосомы. Признано, что она способствует развитию перекрестной резистентности к макролидным антибиотикам; вместе с тем не ясно, все ли макролиды, разными путями проникающие в слизистую оболочку желудка, могут приводить к селекции резистентных штаммов in vivo.
Различны и данные о влиянии резистентности к кларитромицину на исходы эрадикационной терапии. Максимальный из описанных эффектов следующий: 87,8% эрадикации Hp при наличии чувствительных штаммов, 18,3% – при наличии резистентных штаммов [18].
Количество штаммов Hp, резистентных к метронидазолу, в Европе и США колеблется от 20 до 40%. Известно, что в развивающихся странах число метронидазолрезистентных штаммов выше. Наибольшее значение для селекции резистентных штаммов имеет применение метронидазола в популяции. Механизм формирования резистентности к метронидазолу до конца не ясен: подозревают изменения гена rdxA, но точные мутации не известны [18].
Наблюдение (1996–2001) за динамикой резистентности к производным нитроимидазола (метронидазол), макролидам (кларитромицин) и β-лактамам (амоксициллин) у штаммов Hp, выделенных в Москве, показало, что она отличается от таковой в Европе (рис. 2). Так, во взрослой популяции уровень первичной резистентности Hp к метронидазолу уже в 1996 г. превысил среднеевропейский показатель (25,5%) и составил 36,1%. На протяжении 1996–1999 гг. отмечалось увеличение числа первично резистентных штаммов Hp к метронидазолу, а затем оно не выявлялось [2].
Рис. 2. Динамика резистентности (в %) к метронидазолу, кларитромицину и амоксициллину у штаммов Hp, выделенных от взрослых в Москве в 1996–2001 гг. (Кудрявцева Л., 2004)
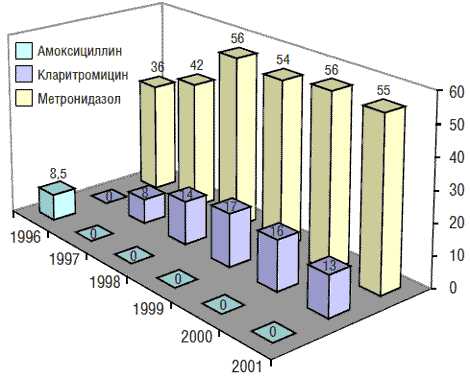
В отличие от данных, полученных в Европе в 1996 г., где во взрослой популяции уровень первичной резистентности Hp к макролидам (кларитромицин) составлял 7,6%, в Москве в то время штаммов Hp, резистентных к этому антибиотику, выявлено не было. Относительный прирост количества штаммов Hp, первично резистентных к кларитромицину, среди взрослой популяции за 1-й год наблюдения составил 8%, за 2-й – 6,4%, за 3-й – 2,7%. В 2000 г. уровень резистентности Hp к кларитромицину несколько снизился: если в 1999 г. он составлял 17,1%, то в 2000 г. – 16,6%. В 2001 г. наметилась явная тенденция к снижению этого показателя (13,8%).
В 1996 г. в Москве было выделено 3 штамма Hp, резистентных к амоксициллину; в дальнейшем такие находки не повторялись, и эти данные можно считать единственными в РФ и уникальными [2].
Последние доступные данные о чувствительности Hp к антибиотикам в Москве относятся к 2005 г. : у взрослых количество резистентных к метронидазолу штаммов составило 54,8%, к кларитромицину – 19,3%; у детей – соответственно 23,8 и 28,5% (Кудрявцева Л., 2006: персональное сообщение).
Таким образом, исходя из последних данных, в России сложились неблагоприятные условия для проведения стандартной тройной терапии вследствие высоких показателей резистентности Нр и к кларитромицину, и к метронидазолу. Тем не менее результаты отечественных клинических исследований свидетельствуют о большем значении для исходов терапии в нашей стране резистентности к метронидазолу, чем к кларитромицину. Чрезвычайное распространение штаммов, резистентных к метронидазолу, значительно ограничивает использование этого антибактериального агента. Так, по данным В. Ивашкина и соавт., в контролируемом исследовании схема «ингибитор протонной помпы+амоксициллин+метронидазол» (одобренная Маастрихтскими рекомендациями I и исключенная их вторым пересмотром) была успешной лишь в 30% случаев [1]. Что же касается резистентности к макролидам, то следует помнить, что контингент больных, из биопсийного материала которых были выделены штаммы для определения резистентности, был особый, в частности среди них было много стационарных пациентов. Кроме того, при анализе штаммов, полученных от лиц, проживающих в разных городах РФ, были выявлены существенные различия. Так, штаммов Hp, резистентных к кларитромицину, в Абакане зарегистрировано не было (табл. 3) [2]. Это заставляет предположить, что их распространенность за пределами Москвы и Санкт-Петербурга ниже среднеевропейского уровня.
Таблица 3. Частота антибиотикорезистентности Hp в разных городах России в 2001 г. (Кудрявцева Л. и соавт., 2004)
| Резистентность штаммов Hp | Города | ||
| Москва | Санкт-Петербург | Абакан | |
| % резистентных штаммов | |||
| К метронидазолу | 55,5 | 40 | 79,4 |
| К кларитромицину | 13,8 | 13,3 | 0 |
| К амоксициллину | 0 | 0 | 0 |
Не следует забывать, что обеспечивают высокий процент уничтожения Нр не только антибактериальные компоненты схемы лечения, но и ингибиторы протонной помпы. Было убедительно доказано, что без ингибитора протонной помпы при применении только 2 тех же антибиотиков в тех же дозировках эрадикация Нр снижается на 20–50%. Именно ингибиторы протонной помпы служат базисными препаратами схемы, обеспечивая путем мощного подавления желудочной секреции благоприятные условия для реализации действия антибиотиков. Если качество ингибитора протонной помпы низкое и он мало влияет на интрагастральный рН, то и процент эрадикации микроорганизма не будет достигать «целевого» рубежа. С другой стороны, высокий антихеликобактерный эффект свидетельствует об успешном контроле желудочной секреции ингибитором протонной помпы и о качестве этого лекарственного средства.
В большом числе отечественных клинических исследований продемонстрирована успешность стандартной тройной терапии даже при ее 7-дневной продолжительности. Так, в работе В. Пасечникова и соавт. (2004) больные с обострением язвенной болезни двенадцатиперстной кишки (92 человека) получали стандартную тройную терапию в течение 7 дней: Омез® (омепразол, «Д-р Редди`с Лабораторис Лтд.») в дозе 40 мг/сут в сочетании с амоксициллином (2000 мг/сут) и кларитромицином (1000 мг/сут). Затем была проведена рандомизация: пациенты 1-й группы продолжали получать омепразол (40 мг/сут) еще 2 нед; пациенты 2-й группы не получали никакого лечения. Эрадикация Hp была успешной у 82,6% больных (intention-to-treat; per protocol – 91,6%). В 1-й группе она составила 84,2% (intention-to-treat; per protocol – 92,8%), во 2-й – 82,2% (intention-to-treat; per protocol – 90,2%). Принципиальное значение имеет тот факт, что заживление язвы достигнуто у 91,5% больных, получавших монотерапию Омезом® после антихеликобактерного курса, и у 93,3% больных, получавших только недельный курс эрадикации Hp и никакого лечения в дальнейшем [4]. Таким образом, в данном исследовании 7-дневная стандартная тройная терапия способствовала достижению «целевого» процента эрадикации и более того – заживлению язвы даже без продолжения монотерапии омепразолом, что косвенно свидетельствует об эффективности антихеликобактерного курса.
Предпринимаются самые разные попытки повысить эффективность стандартной тройной терапии. Так, имеются данные о том, что сочетание антихеликобактерной схемы с пробиотиком приводит к повышению показателя эрадикации Hp и снижает частоту нежелательных явлений [10, 20]. Недавно в Москве было предпринято исследование с добавлением к стандартной тройной терапии пребиотика лактулозы (Нормазе). Омез® (40 мг/сут) в сочетании с амоксициллином (2000 мг/сут) и кларитромицином (1000 мг/сут) назначали на 12 дней и в одной группе больных сочетали с Нормазе. Эрадикация Hp в этой группе достигнута в 85% случаев, в другой – в 90% случаев (различие недостоверно). Несмотря на то что лактулоза не способствовала увеличению эрадикации Hp (процент все же превзошел «целевой» рубеж), она уменьшила частоту нарушений стула и метеоризм [3].
Терапия первой линии – стандартная тройная – не утратила актуальности для России. От точного соблюдения этого стандарта врачом и пациентом зависит успех эрадикации Нр. Чем выше ее показатель, тем меньше вероятность повторного лечения. Наиболее обоснованным способом повышения эффективности стандартной тройной терапии следует признать увеличение ее продолжительности до 14 дней [7, 11, 12].
Как надо планировать терапию второй линии при неудаче применения первой линии? Следует избегать назначения антибиотиков, которые пациент уже получал. Это – один из основополагающих (но не общепризнанных) постулатов, на которых строится такое планирование [7]. С точки зрения экспертов – авторов Маастрихтских рекомендаций III, наиболее правильным выбором в данной ситуации является квадротерапия с препаратом висмута [17]. К такому же выводу пришли и авторы Американских рекомендаций по диагностике и лечению Hp [7]. При анализе нескольких десятков клинических исследований с применением квадротерапии в качестве терапии второй линии средний показатель эрадикации микроорганизма составил 76% (60–100%) [15]. Данная схема доступна, относительно дешева и эффективна. К ее недостаткам относят большое число таблеток и капсул, которые приходится принимать ежедневно (до 18 штук в сутки), четырехкратный режим дозирования и сравнительно часто развивающиеся нежелательные явления [7].
В некоторых странах препараты висмута недоступны, и в качестве схем второй линии Маастрихтские рекомендации III предлагают варианты тройной терапии: ингибитор протонной помпы и амоксициллин, а в качестве антибактериального агента фигурируют тетрациклин или метронидазол [17]. В России нет систематизированного опыта использования таких схем, хотя имеются данные о весьма низкой эффективности 7-дневной тройной терапии: ингибитор протонной помпы+амоксициллин+метронидазол [1].
Как терапию третьей линии Маастрихтские рекомендации III позиционируют тройную терапию с представителем рифамицинов – рифабутином – и хинолонов – левофлоксацином.
В группе больных с неудавшимся курсом стандартной тройной терапии 12-дневное лечение ингибитором протонной помпы в сочетании с амоксициллином и рифабутином (150 мг) привело к эрадикации Hp в 91% случаев, причем доказанная резистентность к метронидазолу и кларитромицину не сказалась на результате [5]. Привлекательная сторона применения рифабутина – очень малая вероятность формирования резистентности к нему Hp (описана лишь в единичных случаях). Механизм формирования резистентности (перекрестной ко всем рифамицинам) – это точечная мутация rpoB-гена [18]. Маастрихтские рекомендации III настаивают на осторожном назначении этого антибиотика, так как его широкое применение может привести к селекции резистентных штаммов Mycobacteria.
Удобной в применении и достаточно эффективной кажется тройная терапия с левофлоксацином: ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с амоксициллином (2000 мг/сут) и левофлоксацином (500 мг/сут). В качестве терапии второй линии после неудачной стандартной тройной терапии эта схема дает высокий результат [8]. Но с применением левофлоксацина связана проблема формирования резистентности к хинолонам вследствие целого ряда мутаций гена gyrA. В недавно опубликованном французском исследовании, в котором изучали большое число штаммов Hp, резистентность выявлена у 17,2% из них [6]. В работе итальянских авторов (с гораздо меньшим числом изученных штаммов) резистентность к левофлоксацину установлена в 30,3% случаев; показатель успешной эрадикации чувствительного к данному антибиотику микроорганизма – 75% против 33,3% при наличии резистентности [19].
В последних рекомендациях экспертов и обзорах по данной проблеме очень пристальное внимание уделяется новой схеме эрадикации Hp – последовательной терапии [7, 10, 11, 14]. Курс последовательной терапии занимает 10 дней: на первые 5 дней назначают ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с амоксициллином (2000 мг/сут); затем в течение еще 5 дней – ингибитор протонной помпы в стандартной дозе дважды в сутки в сочетании с кларитромицином (1000 мг/сут) и тинидазолом (1000 мг/сут). В итальянском исследовании [21] при последовательной терапии эрадикация Hp (intention-to-treat) составила 91 против 78% в группе сравнения (10-дневная стандартная тройная терапия). В группе пациентов, инфицированных штаммами, резистентными к кларитромицину, этот показатель достиг 89 против 29%.
Для исключения неудачи в эрадикации Hp стандартную тройную терапию следует назначать в полном объеме по дозам и при возможности – на 14 дней. Выбор схем лечения в случае неудачи терапии первой линии достаточно широк и позволяет учесть индивидуальные особенности пациента.
ЛИТЕРАТУРА 1. Ивашкин В. Т., Лапина Т. Л., Бондаренко О. Ю. и соавт. Азитромицин в эрадикационной терапии инфекции Helicobacter pylori: итоги клинического испытания и фармако-экономические аспекты // Рос. журн. гастроэнт., гепатол., колопроктол. – 2001; XI: 2 (приложение № 13б); 58–63. 2. Кудрявцева Л. В. Региональные генотипы и уровни резистентности к антибактериальным препаратам Helicobacter pylori. Автореф. … докт. мед. наук. – М., 2004. – С. 40. 3. Минушкин О. Н., Зверков И. В., Ардатская М. Д. и соавт. Эрадикационное лечение с нормазой язвенной болезни двенадцатиперстной кишки, ассоциированной с Helicobacter pylori // Клин. перспективы гастроэнтерологии, гепатологии. – 2007; 5: 21–25. 4. Пасечников В. Д., Минушкин О. Н., Алексеенко С. А. и соавт. Является ли эрадикация Helicobacter pylori достаточной для заживления язв двенадцатиперстной кишки? // Клин. перспективы гастроэнтерологии, гепатологии. – 2004; 5: 27–31. 5. Borody T. J., Pang G., Wettstein A. R. et al. Efficacy and safety of rifabu-tin-containing «rescue-therapy» for resistant Helicobacter pylori infection // Aliment. Pharmacol. Ther. – 2006; 23: 481–488. 6. Cattoir V., Nectoux J., Lascols C. et al. Update on fluoroquinolone resistance in Helicobacter pylori: new mutations leading to resistance and first description of a gyrA polymorphism associated with hypersusceptibility // Int. J. Antimicrob. Agents. – 2007; 29: 389–396. 7. Chey W. D., Wong B. C. Y. et al. American College of Gastroenterology Guideline on the management of Helicobacter pylori infection // Am. J. Gastroent. – 2007; 102: 1808–1825. 8. Cheng H. C., Chang W. L., Chen W. Y. et al. Levofloxacin-containing triple therapy to eradicate the persistent H. pylori after a failed conventional triple therapy // Helicobacter. – 2007; 12: 359–363. 9. Current European concept in the management of Helicobacter pylori infection. The Maasticht Consensus Report. The European Helicobacter pylori study group (EHPSG) // Gut. – 1997; 41: 8–13. 10. Di Mario F., Cavallaro L. G., Scarpignato C. ‘Rescue’ therapies for the management of Helicobacter pylori infection // Dig. Dis. – 2006; 24: 113–130. 11. Egan B. J., Katicic M., O’Connor H. J. et al. Treatment of Helicobacter pylori // Helicobacter. – 2007; 12: 31–37. 12. Ford A., Moayyedi P. How can the current strategies for Helicobacter pylori eradication therapy be improved? // Can. J. Gastroenterol. – 2003; 17 (Suppl. B): 36–40. 13. Glupczynski Y., Megraud F., Lopez-Brea M. et al. European multicenter survey of in vitro antimicrobial resistance in Helicobacter pylori // Eur. J. Clin. Microbiol. Infect. Dis. – 2000; 11: 820–823. 14. Graham D. Y., Lu H., Yamaoka Y. A report card to grade Helicobacter pylori therapy // Helicobacter. – 2007; 12: 275–278. 15. Hojo M., Miwa H., Nagahara A. et al. Pooled analysis on the efficacy of the second-line treatment regimens for Helicobacter pylori infection // Scand. J. Gastroenterol. – 2001; 36: 690–700. 16. Malfertheiner P., Megraud F., O`Morain C. et al. Current concept in the management of Helicobacter pylori infection - the Maasticht 2 – 2000 Consensus Report // Aliment. Pharmacol. Ther. – 2002; 16: 167–180. 17. Malfertheiner P., Megraud F., O`Morain C. et al. Current concept in the management of Helicobacter pylori infection: the Maasticht III Consensus Report // Gut. – 2007; 56: 772–781. 18. Megraud F. H. pylori antibiotic resistance: prevalence, importance, and advances in testing // Gut. – 2004; 53: 1374–1384. 19. Perna F., Zullo A., Ricci C. et al. Levofloxacin-based triple therapy for Helicobacter pylori re-treatment: role of bacterial resistance // Dig. Liver. Dis. – 2007; 39: 1001–1005. 20. Tong J. L., Ran Z. H., Shen J. et al. Meta-analysis: the effect of supplementation with probiotics on eradication rates and adverse events during Helicobacter pylori eradication therapy // Aliment Pharmacol Ther. – 2007; 15: 155–168.
21. Vaira D., Zullo A., Vakil N. et al. Sequential therapy versus standard triple-drug therapy for Helicobacter pylori eradication: a randomized trial // Ann. Intern. Med. – 2007; 146: 556–563.
Что такое эрадикационная терапия — VospalenieKishechnika
Европейскими учеными, которые изучают H.pylori, постоянно проводятся клинические испытания для усовершенствования подходов лечения и диагностики данной инфекции. Последний пятый консилиум был организован в 2015 году. Одни из основных его рекомендаций представлены в таблице:
| № | Описание |
| 1 | В большинстве стран начинает развиваться устойчивость H.pylori к антибиотикам |
| 2 | В регионах, где резистентность к Кларитромицину больше 15%, стандартная первая линия терапии не назначается без предшествующего определения чувствительность к антибиотику у конкретного пациента |
| 3 | Если пациент до лечения принимал основные противохеликобактерные антибиотики, необходимо определить резистентность микроорганизма к ним, несмотря на высокую чувствительность в регионе |
| 4 | В тех популяциях, где уровень резистентности к Кларитромицину более 15%, рекомендована висмутсодержащая квадротерапия. Если использование такой схемы невозможно, то назначается «последовательная» терапия или безвисмутовая квадротерапия. В районах, где имеет место устойчивость бактерий одновременно к Метронидазолу и Кларитромицину, рекомендуется висмутсодержащая квадротерапия |
| 5 | Продолжительность четырехкомпонентной терапии с висмутом должна составлять не менее 14 или 10 дней, если в конкретном регионе она оказалась эффективной |
| 6 | Снижается эффективность тройной и последовательной терапии, если есть резистентность к Кларитромицину, последовательной — при устойчивости к Метронидазолу, комбинированной и сопутствующей при отсутствии чувствительности к обоим антибиотикам |
| 7 | В настоящее время сопутствующая терапия (ИПП, Амоксициллин, Кларитромицин и Метронидазол назначают одновременно) является предпочтительной, поскольку установлена ее значительная эффективность в отношении преодоления антибиотикорезистентности в сравнении с висмутсодержащей квадротерапией |
| 8 | В районах с низкой резистентностью к Кларитромицину тройная терапия рекомендуется как первая линия эмпирического лечения. Четырхкомпонентная с висмутом является альтернативой |
| 9 | Употребление высоких доз ИПП усиливает тройную терапию |
| 10 | Длительность стандартной тройной схемы должна быть продлена до 14 дней, если более короткое лечение было неэффективно на регионарном уровне |
| 11 | В случае неэффективности стандартной трехкомпонентной терапии может быть рекомендована висмутсодержащая квадротерапия или фторхинолонсодержащая тройная или квадротерапия |
| 12 | Если висмутсодержащая квадротерапия оказывается недейственной, то рекомендуется фторхинолонсодержащая тройная или четырехкомпонентная терапия |
Эффективность лечения стандартной тройной терапии повышается при увеличении курса до двух недель.
pancreat.ru
Опасный сосед
В настоящее время не подлежит сомнению высокая степень ассоциации пептических язв с жизнедеятельностью хеликобактер пилори в слизистой желудка. Для лечения используется комплексная эрадикационная терапия – это действия, направленные на полное освобождение от инфекции, которые сводят к минимуму вероятность рецидивирования язв.
В последующие за открытием Н. pylori годы появились сообщения о том, что эта бактерия является этиологическим фактором целого ряда других заболеваний: хронического активного антрального гастрита (типа В), атрофического гастрита (типа А), некардиального рака, MALT-лимфомы, идиопатической железодефицитной анемии, идиопатической тромбоцитопенической пурпуры и анемии, обусловленной дефицитом витамина В12. Продолжается изучение взаимосвязи спиралевидной бактерии с аллергическими, респираторными и другими внежелудочными заболеваниями.
Эрадикационная терапия у детей
Необходимость эрадикации инфекции H. pylori у детей показана в многочисленных клинических исследованиях и их метаанализах, которые послужили основой для составления и регулярного обновления международного согласительного документа, хорошо известного практикующим гастроэнтерологам как Маастрихтский консенсус. В настоящее время вопросы диагностики и лечения хеликобактер-ассоциированных заболеваний регламентируются уже четвертым Маастрихтским консенсусом, принятым в 2010 году.
В развитых странах Европы, Америки и в Австралии, где с момента открытия этиологической роли Н. pylori систематически разрабатывались и внедрялись в практику методы диагностики и лечения данной инфекции, отмечен спад заболеваемости язвенной болезнью и хроническим гастритом. Кроме того, в этих государствах впервые за десятилетия наметилась тенденция к снижению заболеваемости раком желудка, чему также способствует эрадикационная терапия.
«>
Загадочная бактерия
На основании результатов многочисленных рандомизированных плацебо и сравнительных исследований определена эффективность пробиотических средств при различных клинических ситуациях, в том числе и при хеликобактерной инфекции у детей. Однако, несмотря на некоторые достижения в понимании действия пробиотиков на бактерию H. pylori, ее тонкие механизмы остаются малоизученными.
Основным ингибирующим и бактерицидным фактором Lactobacillus является молочная кислота, которую они производят в больших количествах. Молочная кислота ингибирует активность уреазы H. pylori и, как предполагают, оказывает свое антимикробное действие за счет снижения рН в пространстве люмена желудка. Однако было установлено, что молочная кислота, которая производится клетками слизистой желудка (СОШ), способствует росту колонии H. pylori. Кроме молочной кислоты лактобактерии и некоторые другие пробиотические штаммы продуцируют антибактериальные пептиды.
Комплексная терапия
Концепция эрадикационной терапии базируется на комбинировании препаратов. ИПП (ингибиторы протонной помпы) блокируют фермент уреазу и накопление энергии внутри H. pylori, а также повышают pH на слизистой желудка, создавая условия для действия антибактериальных препаратов. Соли висмута, скапливаясь в бактерии, мешают ферментной системе патогена, позволяя иммунной системе ребенка эффективнее справляться с «вторженцем». Наконец, самой разнородной является группа антибактериальных препаратов.
Эрадикационная терапия при язвенной болезни у детей (как и при гастрите) часто предполагает использование нитроимидазолов, макролидов, лактамов, тетрациклина и нитрофуранов. Хеликобактер вырабатывает устойчивость именно к антибактериальным компонентам, что снижает эффективность эрадикационной терапии. И актуальность этой проблемы растет с каждым десятилетием.
«>
Резистентность к антибиотикам
Выработка устойчивости к антибиотикам – общая черта, присущая всем патогенным микроорганизмам. Это эволюционный механизм, который обеспечивает их выживание в изменяющихся условиях. Резистентность Н. pylori подразделяют на:
- Первичную (следствие предшествующего лечения).
- Вторичную (приобретенная мутация микроорганизма, которую «подстегивает» эрадикационная терапия).
Причины устойчивости к лечению
В числе главных причин формирования приобретенной резистентности H. pylori ученые называют:
- Рост назначений антибактериальных препаратов этих же групп по другим показаниям.
- Бесконтрольное самолечение антибиотиками в странах, где они продаются без рецепта.
- Неадекватно назначенная эрадикационная терапия гастрита или язвы (назначение низких доз антибиотиков, сокращение курсов лечения, неправильная комбинация в схеме препаратов).
- Несоблюдение предписаний врача пациентами.
- Появление на фармацевтических рынках препаратов низкого качества.
В результате всего перечисленного рост резистентности H. pylori сокращает и без того ограниченное количество антибиотиков, активных в отношении данного микроорганизма.
Проблема антибиотикорезистентности особенно актуальна для детей, которым показана эрадикационная терапия язвенной болезни. Чаще всего они инфицируются первично резистентными микроорганизмами от родителей и близких родственников.
Кроме того, в детской популяции особенно распространено необоснованное применение антибиотиков для лечения других заболеваний, чаще всего респираторных инфекций, что также способствует селекции первично устойчивых штаммов. Нарушение режима эрадикационной терапии, как и у взрослых, приводит к формированию вторичной резистентности. Развитие устойчивости патогенна также связано с мутациями разных генов хеликобактерии.
«>
Диагностика
Эрадикационная терапия у подростков начинается после всеобъемлющей диагностики. Первичной целью обследования ребенка, у которого наблюдаются гастроинтестинальные симптомы, является определение причины возникновения этих симптомов, а не только наличия H. pylori. При этом проведение тестов на выявление хеликобактера не рекомендуется у детей с функциональной абдоминальной болью. Можно рассмотреть целесообразность проведения тестов на выявление патогена:
- у пациентов, в семейном анамнезе которых есть рак желудка у родственника первой степени родства;
- при рефрактерной железодефицитной анемии (если исключены другие причины заболевания).
Не хватает достаточных практических доказательств причастности H. pylori к среднему отиту, инфекциям ВДП, пародонтиту, пищевой аллергии, синдрому внезапной детской смерти, идиопатической тромбоцитопенической пурпуре, низкому росту. Но подозрения есть.
Диагностические тесты
Эрадикационная терапия при язвенной болезни и гастрите определяется диагностическими тестами. Методика тестирования зависит от многих факторов:
- Для диагностики хеликобактера при проведении эзофагогастродуоденоскопии рекомендуется провести биопсию антрального отдела желудка для дальнейшего гистологического анализа.
- Рекомендуется, чтобы первоначальный диагноз H. pylori был основан на следующих данных: положительное гистологическое исследование и положительный тест на уреазу (как альтернатива – положительные результаты культурального исследования).
- C-уреазный дыхательный тест является надежным неинвазивным методом для определения того, состоялась ли эрадикация H. pylori.
- Иммуноферментный анализ кала также является надежным неинвазивным тестом для определения того, состоялась ли эрадикация бактерии.
- Тесты, основанные на выявлении антител к хеликобактерии в сыворотке, цельной крови, мочи и слюне, наоборот, надежными не являются.
Показания
Какие нужны показания к эрадикационной терапии:
- При наличии язвенной болезни и инфицировании хеликобактером.
- Если язвенной болезни нет, а инфекцию H. pylori выявили по результатам исследования образцов, взятых с помощью биопсии, эрадикация возбудителя необязательна, но возможна.
Кстати, применительно к детям не рекомендуется применять принцип «диагностируй и лечи», необходима определенная осторожность.
Эпидемиология
Определение уровня резистентности в отдельно взятой стране, регионе или популяции – сложная задача, требующая больших материальных и человеческих ресурсов. Еще сложнее сравнивать данные, полученные в разных странах из-за различий в методологии исследований. Например, по материалам длительных исследований в Европе (2003-2011 гг.), устойчивость патогена к «Кларитромицину» составляла от 2 до 64 % в разных странах. По данным российских авторов, резистентность к «Кларитромицину» варьируется от 5,3 до 39 %.
Из препаратов, которые применяются в схемах эрадикации, наименьшую устойчивость к резистентности формирует амоксициллин, а наибольшую – «Метронидазол». Продолжает расти устойчивость Н. pylori к препарату «Кларитромицин».
Проблемы использования «Метронидазола» и «Фуразолидона»
Эрадикационная терапия раньше часто проводилась вышеуказанными препаратами. Однако рост приспосабливаемости бактерий к «Метронидазолу» резко снизил эффективность схем лечения с его использованием. «Метронидазол» по этой причине во многих странах сегодня исключен из схем лечения.
Альтернативой «Метронидазолу» стали препараты нитрофуранового ряда, в частности «Фуразолидон». Эффективность эрадикации на его основе в комбинации с висмутом составляет 86 %. Однако «Фуразолидон» токсичен – в детской терапии во многих клиниках он не используется. К числу недостатков «Фуразолидона» относятся гепато-, нейро- и гематотоксичность, подавление микрофлоры, неудовлетворительные органолептические свойства. Для достижения требуемой концентрации действующего вещества в организме данный препарат приходится принимать четыре раза в день. Эти качества «Фуразолидона» значительно снижают полезное действие всей схемы лечения и, как следствие, эффективность эрадикации.
«>
Препарат нового поколения
Многие лаборатории фармацевтических фирм разрабатывают менее токсичные, но эффективные против хеликобактера лекарства. Настоящим прорывом стал препарат «Макмирор», содержащий в качестве действующего вещества нифуратель. Современная альтернатива «Фуразолидону» разработана и синтезирована научно-исследовательской компанией Polichem (Италия). «Макмирор» обладает широким спектром антибактериального, противогрибкового и антипротозойного действия. Эрадикационная терапия для детей стала более безопасной.
Использование «Макмирора» позволяет усовершенствовать существующие схемы эрадикации хеликобактера у детей, повысить их эффективность и безопасность. «Нифуратель» включен в обновленные протоколы лечения H. pylori — ассоциированного хронического гастрита, гастродуоденита и язвенной болезни у детей.
Использование препарата «Макмирор» сопровождается высоким комплайенсом, так как благодаря двенадцатичасовому периоду полувыведения он может назначаться два раза в сутки. Применяется у детей с шестилетнего возраста, суточная доза при лечении лямблиоза и в схемах эрадикации хеликобактера – 30 мг в сутки на килограмм массы ребенка.
Схемы эрадикационной терапии
Примеры терапии первой линии. Однонедельные тройные схемы с препаратом висмута:
- Коллоидный субцитрат висмута (КСВ) дополняется «Амоксициллином» («Рокситромицином») или «Кларитромицином» («Азитромицином») плюс «Нифуратель» («Фуразолидон»).
- Во второй схеме «Нифуратель» заменяется «Фамотидином» («Ранитидином»), остальные препараты те же.
Однонедельные тройные схемы с ингибиторами протонной помпы:
- «Омепразол» («Пантопразол») дополняется амоксициллином или «Кларитромицином» плюс «Нифуратель» («Фуразолидон»).
- То же самое, но «Нифуратель» заменяется на КСВ.
В качестве лечения второй линии применяется эрадикационная терапия с четырьмя компонентами: КСВ работает вместе с «Омепразолом» («Пантопразолом»), «Амоксициллином» (или «Кларитромицином») и «Нифурателем» («Фуразолидоном»).
«>
Дозы
Протоколами также регламентируются дозы препаратов, которые следует использовать в эрадикационных схемах у детей (ежесуточно на килограмм веса):
- КСВ – 48 мг (максимум 480 мг в сутки).
- «Кларитромицин» – 7,5 мг (максимум 500 мг).
- «Амоксициллин» – 25 мг (максимум 1 г).
- «Рокситромицин» – 10 мг (максимум 1 г).
- «Фуразолидон» – 10 мг.
- «Нифуратель» – 15 мг.
- «Омепразол» – 0,5-0,8 мг (максимум 40 мг).
- «Пантопразол» – 20-40 мг (без учета веса).
- «Ранитидин» – 2-8 мг (максимум 300 мг).
- «Фамотидин» – 1-2 мг (максимум 40 мг).
Особенности лечения
Какое лечение следует применять в той или иной ситуации:
- Детям, инфицированным H. pylori и имеющим в семейном анамнезе рак желудка у родственника первой степени родства, можно назначить эрадикационную терапию.
- Рекомендовано в разных регионах проводить надзор за распространенностью антибиотикорезистентных штаммов Helicobacter.
- В регионах/популяциях, в которых распространенность резистентности Helicobacter к «Кларитромицину» высока (> 20 %), рекомендуется перед началом тройной терапии, предусматривающей применение «Кларитромицина», определять чувствительность к этому антибиотику.
- Рекомендуемая продолжительность тройной терапии – 7-14 суток. При рассмотрении этого вопроса следует учесть расходы, приверженность к лечению и побочные эффекты.
- Для оценки результатов проведенной эрадикационной терапии рекомендуется применить надежные неинвазивные тесты спустя 4-8 недель после лечения.
Если не помогло
В случае неэффективности лечения рекомендуется следующие подходы:
- Эзофагогастродуоденоскопия с последующим культивированием и определением чувствительности к антибиотикам, включая альтернативные, если это не было сделано перед лечением.
- Флуоресцентная гибридизация in situ (FISH) для определения резистентности к «Кларитромицину» с применением образцов, взятых при первой биопсии и залитых в парафин, если определение чувствительности к этому антибиотику не проводилось перед лечением.
- Модификация лечения: добавить антибиотик, назначить другой антибиотик, добавить препарат висмута и/или повысить дозу, и/или увеличить продолжительность терапии.
Вывод
Эрадикационная терапия – это действенное (порой единственное) средство борьбы с опаснейшей бактерией Helicobacter pylori, способной спровоцировать язвы, гастриты, колиты и прочие болезни ЖКТ.
www.syl.ru
Что собою представляет эрадикация
Дословно эрадикация – это ликвидация или уничтожение. В медицинской терминологии это слово применяется к комплексным методам лечения, направленным на устранение вирусов или бактерий в организме.
Терапия такого вида подразумевает специальный режим приема препаратов. В среднем, если назначенные препараты были правильно подобраны, лечение продлится две недели. По истечении этого срока эрадикация хеликобактер пилори, не принесшая результатов, характеризуется как неудачная.
Оптимально подобранное лечение дает исключительно положительные результаты. На самочувствие больного прием антибиотиков и других препаратов не оказывает побочного действия. Окончив прием медикаментов, пациент чувствует себя лучше, вероятность возобновления заболевания сведена к минимуму.
 Чтобы уничтожить вирусы и бактерии, лекарственные препараты должны приниматься по назначению врача
Чтобы уничтожить вирусы и бактерии, лекарственные препараты должны приниматься по назначению врача Максимального результата можно добиться при соблюдении условий:
- Соблюдение режима, своевременный прием препаратов.
- Соблюдение диеты.
- Применение низкотоксичных препаратов, не приводящих к последствиям.
- Наблюдение, установление продуктивности лечения с первого дня терапии.
- Использование доступных медикаментов.
Если у восьми из десяти человек, проходивших лечение, результаты были положительными, то можно сказать, что терапевтическое лечение было успешным.
На видео подробно рассказывается о бактерии хеликобактер пилори:
Подробности заболевания
Впервые выявление в организме человека патологии, спровоцированной бактериями хеликобактер пилори, произошло около 30 лет назад, и сегодня ВОЗ продолжает изучать эту инфекцию и предпринимать новые, более безопасные, методы лечения.
Нахождение в органах пищеварительного тракта этой бактерии говорит о возможных последствиях в виде:
- язвенных поражений двенадцатиперстной кишки и желудка;
- гастрита;
- рака;
- дуоденита.
Уничтожить бактерию, обитающую в самой кислой среде организма непросто. Для этого используется комплекс препаратов, принимаемых по определенным схемам. Еще 70 лет назад, человечество считало, что ни одна бактерия не сможет развиваться и жить в условиях кислоты, находящейся в желудке. Хеликобактер – это уникальный организм, поэтому и терапевтический подход к ее уничтожению особенный.
 Заражение бактерией хеликобактер пилори может привести к язве желудка
Заражение бактерией хеликобактер пилори может привести к язве желудка Особенности эрадикации хеликобактер пилори
Схема эрадикации хеликобактер пилори подбирается индивидуально. Способов лечения много, но все они установлены Всемирной Организацией Здравоохранения, и должны строго соблюдаться.
Отклонение от стандартных схем может возникнуть в случае, если используемая в первую очередь терапия не принесла результатов. Схемы лечения при эрадикации helicobacter pylori будут изменяться до тех пор, пока не получится добиться положительного результата.
Поводом для начала терапевтического вмешательства является ощущение боли в области живота и присутствие язвы или другой болезни.
Прежде чем приступать к приему препаратов, больному назначают обследование на определение воспалительных процессов, среди которых биопсия желудка. Эрадикация helicobacter pylori не может начаться, если во внутренних органах была обнаружена злокачественная опухоль. Без болевых ощущений в области живота, лечение также проводиться не будет.
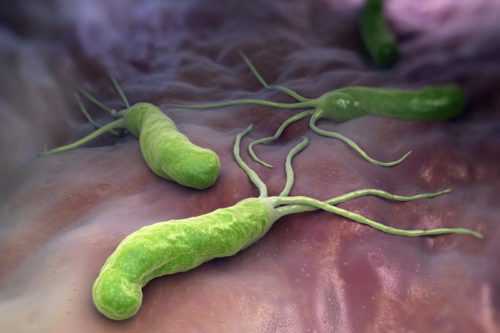 Определить наличие бактерии хеликобактер пилори можно с помощью медицинских исследований
Определить наличие бактерии хеликобактер пилори можно с помощью медицинских исследований Способы проведения
Лечение классифицируется зависимо от препаратов и их количества. Терапия разделяется на виды:
- Монотерапия – применение антибиотиков (Кларитромицина, Амоксициллина), в соединении с висмутом.
- Двойная.
- Триплетная. К указанным в первом случае медикаментам добавляется Метронидазол или Тинидазол.
- Квадриплетная терапия включает еще и ингибиторы. Они способствуют правильной работе желудка.
Схема для эрадикационной терапии хеликобактер пилори первой линии включает три основных медикамента:
- Омез, Омепразол и другие аналогичные препараты;
- антибактериальные средства, в основе которых действующее вещество кларитромицин;
- антибиотики с другим действующим веществом, чаще всего это амоксициллин, метронидазол.
Курс лечения может продолжаться от семи до четырнадцати дней. При наличии атрофии слизистой оболочки желудочно-кишечного тракта схема лечения корректируется. В таком случае препараты на основе омепразола не назначаются, а используется дицитрат висмута.
 Кларитромицин — один из антибиотиков, назначаемых для уничтожения бактерии
Кларитромицин — один из антибиотиков, назначаемых для уничтожения бактерии Выбор схемы лечения производится по результатам бактериологических исследований. В процессе изучается чувствительность бактерии на действие различных антибиотиков.
Схемы лечения дополняются приемом противовоспалительных средств, успокоительных и антигистаминных препаратов, комплекса витаминов.
Лечение народными средствами
Официально ни одно средство растительного происхождения не рекомендуется к лечению этого заболевания, но несколько методик официально запатентованы. К примеру, использование водного раствора прополиса употребляют 3 раза в день на пустой желудок, перед едой.
Также используется настой семян льна, на чашку кипятка используется 1 чайная ложка сырья. Употребление такого чая вместе с семенами позволяет ускорять процессы заживления поврежденной слизистой оболочки ЖКТ. Заживляющим и противовоспалительным действием обладают настои ромашки, облепиховое масло.
 Семена льна — одно из часто применяемых народных средств
Семена льна — одно из часто применяемых народных средств Диета
При заболевании следует соблюдать диету. Запрещено для больного употребление таких продуктов, как:
- жирное мясо, рыба;
- жаренные на масле блюда;
- копченные и консервированные продукты;
- жирные мясные бульоны и супы;
- острые и кислые блюда, специи;
- сладкие блюда, шоколад.
Курение, употребление алкоголя, крепкого кофе или чая могут усугубить заболевание. Поэтому употребление этих напитков и свои вредные привычки нужно ограничивать.
kishechnik.guru
В чем заключается:
 Эрадикационная терапия основана на применение особого лечебного режима, подразумевающего прием медикаментов по определенной схеме. Средний курс эрадикации составляет 14 дней.
Эрадикационная терапия основана на применение особого лечебного режима, подразумевающего прием медикаментов по определенной схеме. Средний курс эрадикации составляет 14 дней.
Если за это время лечение не показывает положительных результатов, эрадикация считается неудачной. Важным является не только соблюдение положенного срока, но и других принципов лечения:
- низкая токсичность принимаемых пациентом препаратов и отсутствие побочных эффектов;
- простота режима (интервалы между приемами лекарств, оптимальная диета);
- экономичность (использование простейших препаратов);
- эффективность (положительная динамика эрадикации должна начать наблюдаться с первых дней режима).
При идеально подобранной схеме эрадикации пациент чувствует себя комфортно на протяжении всего курса терапии. После лечения у него не возникает побочных заболеваний, а риск рецидива минимален.
Применительно к Helicobacter Pylory
Об этой относительно молодой бактерии многие слышали из рекламных роликов о биойогуртах.
Голос за кадром таинственно сообщает, что их продукт способен бороться с Hp и пресекать ее опасную активность.
Ведь этот микроорганизм обитает в различных областях желудка (в частности, в привратнике) и способен провоцировать следующие заболевания:
- язва желудка или двенадцатиперстной кишки;
- гастрит;
- дуоденит;
- рак желудка.
Открытие Helicobacter Pylory позволило ученым понять, что не всегда острая пища или повышенная кислотность являются причинами развития перечисленных выше заболеваний. В большинстве случаев главным фактором становится именно инфицирование Hp.
Показания к терапии
Лечение методом эрадикации проводится для больных с тяжелым течением язвенной болезни. При этом неважно, в какой раз у пациента диагностировано заболевание: впервые или повторно. Главное, чтобы язва была подтверждена исследовательскими методами, например, путем проведения эндоскопии. Если язва не выявлена, то проводить эрадикацию нельзя.
Когда и как проводится
Перед проведением эрадикационной терапии обычно проводится еще одно дополнительное исследование – биопсия желудка на предмет обнаружения злокачественных клеток. Если они отсутствуют, можно начинать эрадикацию.
Лечение проводится несколькими препаратами. От количества применяемых медикаментов зависит основная классификация эрадикации.
- Монотерапия. Подразумевает применение соединений висмута или других антимикробных препаратов (амоксициллин, кларитромицин, Клацид). Используется редко, т.к. не очень эффективна.
- Двойная терапия. Достаточно многообещающий тип эрадикации, предполагающий сочетание обеих видов препаратов из монотерапиию. Результативность может достигать 60%.
- Триплетная терапия. Позволяет достичь высокой степени эрадикации: около 90%. К двум уже известным препаратам добавляются производные имидазола (тинидазол, метронидазол). Идеально подходит для избавления от Helicobacter Pylory, если у пациента не повышена чувствительность к имидазолу.
- Квадриплетная терапия. Добавляются ИПН (ингибиторы протонного насоса), которые тоже помогают бороться с заболеваниями ЖКТ. Квадриплетная эрадикация дает отличные результаты: 95% пациентов выздоравливает.
Применительно к вирусу герпеса (ВПГ)
 Если с Helicobacter Pylory такая терапия способна справиться полностью и уничтожить все бактерии, то вирус герпеса в этом плане более устойчивый.
Если с Helicobacter Pylory такая терапия способна справиться полностью и уничтожить все бактерии, то вирус герпеса в этом плане более устойчивый.
Лечение направлено лишь на частичную эрадикацию, облегчение течения заболевания и укрепление иммунитета.
Один из основных препаратов, использующихся для эрадикационной терапии при вирусе герпеса – изопринозин.
Эрадикация ВПГ проводится с применением иммуномодулирующих препаратов, обладающих интерферонстимулирующими (иначе говоря, антивирусными) свойствами.
Но у интерферонов есть множество других функций, поэтому они невольно «вмешиваются» в ход некоторых процессов организма. Из-за этого эрадикация при вирусе герпеса считается не менее опасной, чем гормонозамещающая терапия.
Актуальность
Этот вид терапии имеет достаточно высокую результативность, поэтому метод довольно часто применяется в стационарах. На домашнее лечение путем эрадикации пациенты не отпускаются, потому что врач должен следить за улучшениями и контролировать состояние больного.
Если организм человека спокойно реагирует на антибиотики, то прогнозы на успешность терапии будут вполне многообещающими.
лечим-грибок.рф
Определение эрадикации
Что такое эрадикация Helicobacter pylori? Фактически это двухнедельный курс консервативного лечения, основной целью которого является уничтожение данной бактерии в организме. При этом антибиотики назначаются с учетом чувствительности микроорганизма, а также их переносимости пациентом. В связи с тем, что хеликобактер постепенно приобретает устойчивость, схемы противомикробной терапии периодически меняются.
Как правило, курс эрадикационного лечения назначает гастроэнтеролог, а в его отсутствии – терапевт или семейный врач. Медикаментозные средства подбираются таким образом, чтобы вероятность уничтожения H. pylori составляла не менее 80 %, а риск развития побочных эффектов от принимаемых средств не превышал порога в 15 %.

Кому нужно проводить эрадикацию
В настоящее время среди специалистов нет однозначного мнения, каким категориям пациентов следует проводить подобное лечение.
- Около 70 % взрослого населения инфицированы этой палочкой.
- Частота повторных заражений на протяжении ближайших 5-7 лет достигает около 90 %.
Тем не менее, считается, что эрадикация хеликобактер пилори однозначно необходима, если у пациента уже имеется:
- язвенная болезнь;
- эрозивный или атрофический гастрит;
- гастроэзофагеальный рефлюкс;
- мальтома желудка (это разновидность лимфомы);
- или у его родственников наблюдались случаи рака данного органа.
Схема проведения эрадикации
Наиболее известные схемы лечения хеликобактер пилори предусматривают использование препаратов трех линий. Эрадикационная терапия обычно начинается с назначения медикаментозных средств первой линии, а при ее неэффективности показаны лекарства второго и третьего порядка.
Как правило, доктор при выборе конкретного средства руководствуется данными лабораторно-диагностического обследования, включающего рН-метрию желудочного сока, ФГДС, уреазный дыхательный тест и т. п. При этом используются препараты следующих групп:
- Антибиотики для эрадикации Helicobacter pylori — амоксициллин, кларитромицин, нифурател, рифаксимин, джозамицин и др.
- Препараты висмута.
- Метронидазол (противомикробное и противопротозойное средство).
- Ингибиторы протонной помпы (ИПП) – например, омепразол, лансопразол, рабепразол.
В качестве дополнительной терапии могут быть назначены пробиотики.

Первая линия
Именно с первой линии гастроэнтерологи рекомендуют начинать проводить эрадикацию H. pylori. Существуют следующие ее схемы:
- ИПП+амоксициллин+кларитромицин/джозамицин/нифурантел.
- ИПП+амоксициллин+кларитромицин/джозамицин/нифурантел+висмут.
- При пониженной кислотности – амоксициллин+кларитромицин/джозамицин/нифурантел+висмут.
- У пожилых – ИПП+амоксициллин+висмут, только висмут на фоне короткого курса ИПП, если есть болевой синдром.
Стандартный курс проводимой эрадикации – 10-14 дней. При ее неэффективности показаны препараты второй линии.
Вторая линия
Вторая линия эрадикации предусматривает назначение метронидазола и антибиотиков нитрофуранового ряда. Классические схемы этой линии:
- ИПП+висмут+метронидазол+тетрациклин.
- ИПП+амоксициллин+нифурател/фуразолидон+висмут.
- ИПП+амоксициллин+рифаксимин+висмут.
Продолжительность курса в среднем составляет 2 недели.
Третья линия
Это индивидуализированная терапия, в случае которой средства подбираются с учетом определения чувствительности H. pylori к антибиотикам. Наиболее часто в эту схему входят кларитромицин или антибиотик фторхинолонового ряда в сочетании с ИПП, висмутом, другими антибактериальными препаратами и т. п.
Если же отсутствует возможность определить чувствительность хеликобактер к антибиотикам, а средства первой и второй линии оказались неэффективными, то прибегают к «терапии спасения». Это высокодозное лечение все 14 дней следующими препаратами:
- ИПП+амоксициллин;
- ИПП+амоксициллин+рифабутин.
В случае аллергии на пенициллины могут использоваться следующие схемы: ИПП+кларитромицин+метронидазол или ИПП+кларитромицин+левофлоксацин.
Применение прополиса

Хотя прополис официально не включен в стандартные схемы эрадикации, он может использоваться в случае отказа больного от антибиотикотерапии или при наличии множественной аллергии к антибактериальным препаратам. С этой целью применяют его водный или масляный 30%-й раствор, а схема выглядит так: прополис+ИПП на протяжении 2-4 недель.
Народные методы эрадикации
Средства народной медицины не могут заменить классического лечения и назначаются доктором лишь в сочетании с курсом стандартной эрадикации. Как правило, для этой цели применяются растения с обволакивающими, противовоспалительными и антисептическими свойствами. При этом наиболее часто используют следующие растения:
- обволакивающее – льняное семя;
- противовоспалительное, ранозаживляющее – облепиховое масло, отвар ромашки, тысячелистника;
- антисептики – лук, чеснок (во время обострения язвы или при наличии эрозий противопоказаны), зверобой, календула и пр.
Диета при проведении лечения
Диета при эрадикации зависит от общего состояния пациента и выраженности симптомов основного заболевания.
Болезни желудка с повышенной кислотностью
Исключаются острые блюда, специи, приправы. Пища подвергается щадящей термической обработке: предпочтительны приготовление на пару, варка, тушение. Исключаются жарка, копчение, маринование. При этом также запрещаются продукты, усиливающие выработку желудочного сока:
- кислые, свежие овощи и фрукты, богатые грубой клетчаткой;
- большинство нешлифованных круп;
- маринады;
- крепкие бульоны;
- наваристые супы;
- жирные продукты.
Так как кофе действует на стенки желудка раздражающе, то на время лечения следует отказаться от всех кофеинсодержащих напитков и очень крепкого чая. Также следует исключить алкоголь.
Разрешены:
- картофельное пюре;
- нежирное отварное диетическое мясо;
- рыба;
- молочные продукты;
- яйца;
- рисовая и овсяная каши;
- йогурты;
- слизистые супы.
При пониженной кислотности
В рацион включаются сокогонные продукты:
- соленья,
- маринады,
- горькие травы,
- специи.
Однако также следует исключать пищу, которая может вызывать обострение воспаления и ухудшение защитных свойств слизистой оболочки желудка. Поэтому на этапе лечения желательно исключить продукты, содержащие разнообразные промышленные примеси и добавки:
- красители,
- консерванты,
- усилители вкуса.
Также не рекомендуется употреблять кофе, алкоголь.
Эффективность лечения
Согласно данным уреазного дыхательного теста, проводимого до и после курса лечения, эрадикационная терапия уже при использовании стандартных схем первой линии эффективна для подавляющего большинства пациентов, особенно тех, кто принимает лечение впервые. Однако с течением времени хеликобактер становится более устойчивой к препаратам, а защитные силы организма требуют восстановления. Эти 2 фактора приводят к тому, что с течением времени успешно используемые схемы уже перестают работать, и необходимо переходить к препаратам второй линии. В целом, первых двух линий эрадикации вполне достаточно, чтобы уничтожить H. pylori.
Среди методов диагностики, с помощью которых желательно оценить качество лечения, наиболее часто используют дыхательные тесты:
Уреазный тест на сегодняшний момент является золотым стандартом выявления хеликобактер и рекомендован не только для первичного обнаружения палочки, но и для обеспечения контроля после проведенной терапии. Его достоверность составляет 95-100 %.
Существенно повысить эффективность эрадикации H. pylori позволяют меры, направленные на:
- укрепление общего и местного иммунитета;
- борьбу со стрессовыми факторами и погрешностями в диете.
gastromedic.ru
Что такое эрадикация - схема лечения
Комплекс двухнедельных терапевтических процедур, направленных на уничтожение определенного вида бактерии, вируса или злокачественных клеток в организме, называют эрадикацией. В большинстве случаев терапия направлена на искоренение бактерии, известной под названием Helicobacter pylori. Этот микроорганизм является одной из основных причин развития язвы, гастрита, рака желудка.
Схема эрадикационной терапии предусматривает прием по четкому графику определенных лекарств, направленных уничтожить патогенные организмы или клетки и заживить нанесенные повреждения. Препараты для эрадикации должны обладать низкой токсичностью и редко давать побочные действия: лечение считается успешным, если осложнения наблюдаются максимум у 15% пациентов.
Эрадикация – это процедура, которая длится не дольше четырнадцати дней и является эффективной, если по истечению этого времени анализы покажут, что популяция вируса или бактерии снизилась на 80% и началось активное заживление пораженных тканей. Для достижения такого эффекта врачи и ученые постоянно разрабатывают новые методы эрадикации, преследуя несколько целей:
- максимальное снижение токсичности принимаемых препаратов;
- экономичность – для эрадикации предпочтение следует отдавать употреблению недорогих лекарств;
- эффективность – улучшение должно происходить с первых дней эрадикации;
- удобство соблюдения режима;
- сокращение количества суточного употребления лекарств за счет приема пролонгированных средств с увеличенным периодом полувыведения;
- краткость курса эрадикации – снижение продолжительности терапии с двух до одной недель;
- уменьшение числа принимаемых лекарственных средств за счет употребления комбинированных препаратов;
- снижение побочных эффектов к минимуму;
- преодоление устойчивости патогенной микрофлоры к антибиотикам;
- разработка альтернативных схем эрадикации при аллергии на лекарства традиционной схемы лечения или при нерезультативности терапии.
Язву желудка, гастриты, дуодениты и другие болезни пищеварительной системы нередко вызывает Helicobacter pylori. Эта бактерия живет и развивается в слизистой оболочке двенадцатиперстной кишки и желудка, хотя уровень кислотности последнего настолько высок, что способен растворить пластмассу. Инфицирование происходит оральным путем (через пищу, поцелуи, при пользовании совместной посудой). Хеликобактер пилори в 90 % случаях не дает о себе знать и активизируется при сбоях в иммунитете, неправильном питании, под влиянием вредных привычек.
Чтобы выжить в кислотной среде, Хеликобактер производит фермент уреазу, который расщепляет мочевину. Во время реакции образуется аммиак, нейтрализующий соляную кислоту и вызывающий раздражение, воспаление слизистой. Это приводит к повышению выделения пепсинов и соляной кислоты, что отрицательно влияет на желудочно-кишечный тракт. В слизистой начинаются деструктивные процессы: она становится рыхлой, затем разрушается, вызывая появление воспаленных зон с формированием язв.
Гастриты, спровоцированные Хеликобактер Пилори, традиционному лечению не поддаются. Бактерия обладает способностью проникать глубоко в ткани, а потому становится недоступной для многих антибиотиков, которые теряют свои способности в кислотной среде. Из-за разрушительных действий микробов в слизистой начинаются необратимые процессы, способные спровоцировать предраковое состояние, стать причиной онкологии. Чтобы не допустить подобного развития событий, применяется эрадикация.

Обнаружить Хеликобактер непросто, поскольку симптомы ее присутствия ничем не отличаются от признаков язв или гастрита, которые вызвали другие причины. Болезнь проявляет себя следующим образом:
- Боль в животе режущего или тупого характера. Может возникать с определенной периодичностью или на голодный желудок, исчезая после приема пищи.
- Отрыжка – сигнализирует об излишней кислотности желудочного сока.
- Регулярная тошнота и рвота.
- Избыточное газообразование в кишечнике, вздутие живота (метеоризм).
- Нарушение стула: понос или запор более 2-3 дней, наличие крови и слизи в кале.
Диагностика хеликобактерной инфекции
При появлении болей в животе, изжоге, поносе или запоре необходимо обратиться к врачу и пройти обследование, направленное определить причину недомогания. В том числе, сдать анализы, позволяющие определить присутствие в организме хеликобактерной инфекции. Среди них:
- Серологическое обследование – иммуноферментный анализ (ИФА), предусматривающий исследование крови на антитела, которые вырабатываются в организме для борьбы с патогеном.
- Анализ кала при помощи метода полимеразной цепной реакции для определения следов присутствия жизнедеятельности микробов.
- Дыхательный тест, направленный определить уровень аммиака в выдохе.
- Цитологическое исследование – способно определить наличие бактерии по ее ДНК.
- Биопсия, во время которой методом эндоскопии на обследование берется ткань слизистых двенадцатиперстной кишки и желудка. Это обследование определяет, в каком состоянии находятся ткани, наличие раковых клеток.
- Уреазный тест (CLO-тест) – образец слизистой помещается в питательную среду с мочевиной и индикатором. Уреаза, которую выделяют бактерии, вступает в реакцию с мочевиной, из-за чего та меняет желтый цвет на красный.
Схемы эрадикации
Назначается эрадикационная терапия больным, у которых была обнаружена язвенная болезнь, предраковое состояние с атрофией тканей, лимфома, атрофический гастрит, пациентам после удаления злокачественной опухоли. В других случаях делать эрадикацию нельзя даже при наличии бактерии, поскольку вред от лечения может превысить пользу. Схема эрадикации Хеликобактер пилори подразумевает использование одного из четырех подходов:
- Монотерапия. Используется редко, поскольку является малоэффективной. Предусматривает использование антимикробных лекарств (Амоксициллина, Кларитромицина, соединений висмута).
- Двойная эрадикация – назначаются два лекарственных средства из монотерапии (висмут + антибиотик). Результативность лечения составляет 60%.
- Триплетная эрадикация. Помимо лекарств, что назначают при двойной терапии, пациенту прописывают употребление производных имидазола (Метронидазол, Тинидазол). При отсутствии аллергии на препараты этого типа результативность лечения составляет 90%.
- Квадриплетная эрадикация – к лекарственным препаратам из триплетной терапии добавляют ингибиторы протонного насоса (ИПН), которые называют блокаторами образования соляной кислоты. После такого лечения 95% больных выздоравливает.
Препараты для эрадикации
Кислотный желудочный сок нейтрализует действие многих лекарств, поэтому для эрадикации используют ограниченное число лекарств. В ходе лечения для уничтожения Хеликобактер пилори применяют антибиотики. Поскольку бактерии обладают способностью со временем к ним приспосабливаться, а сами лекарства вызывают сильные побочные эффекты, стало очевидно, что при эрадикации надо использовать и другие антимикробные средства, которые были бы эффективны, но давали меньше осложнений. К ним относятся:
- противобактериальные и противоинфекционные лекарства;
- препараты с висмутом;
- ингибиторы протонного насоса;
- пробиотики и пребиотики.
В конце прошлого века ученые провели исследования, показавшие, что с колонией Хеликобактер пилори, помещенной в пробирку, без проблем справляются многие антибактериальные средства. В клинических условиях испытания провалились из-за того, что кислота желудочного сока полностью нейтрализует их действие. Кроме того, оказалось, что большинство антибиотиков неспособны глубоко проникнуть в ткани слизистой, где обитает бактерия. По этой причине выбор антибактериальных средств, эффективных в борьбе с бактериями, невелик.
Прежде чем приступить к терапии антибиотиками, обязательно следует убедиться в отсутствии аллергии на препараты назначенной группы. Популярными средствами при эрадикации являются следующие лекарства:
- Амоксициллин (Флемоксин);
- Амоксиклав;
- Азитромицин;
- Кларитромицин.
Амоксициллин относится к препаратам пенициллиновой группы. Хоть лекарство убивает бактерии, оно способно воздействовать лишь на размножающиеся микробы. По этой причине при эрадикации его не прописывают одновременно с бактериостатическими препаратами, которые угнетают деление патогенов. Лекарство не назначают при аллергии, инфекционном мононуклеозе, больным со склонностями к лейкемоидным реакциям. Осторожно прописывают при почечной недостаточности, если женщина ждет малыша, пациент перенес псевдомембранозный колит.
В составе Амоксиклава два активных вещества – антибиотик амоксициллин и клавулановая кислота, обеспечивающая эффективность лекарств пенициллиновой группы по отношению к устойчивым к ним штаммам. При этом она тоже обладает собственной антибактериальной активностью. Благодаря клавулановой кислоте ферменты, разрушающие структуру пенициллина, оказываются связанными и амоксициллин быстро справляется с Хеликобактер. Амоксиклав имеет те же противопоказания, что Амоксициллин, но чаще приводит к дисбактериозу.
Кларитромицин – лекарство эритромициновой группы, препараты которой известны как макролиды. Считается одним из самых эффективных средств в борьбе с Хеликобактер пилори, устойчивость к которому у бактерий возникает редко. Лекарство хорошо совмещается с ИПН, которые используют в квадриплетной эрадикации. Препарат обладает низкой токсичностью: осложнения после его приема были замечены лишь у 2% больных. Среди осложнений – рвота, тошнота, понос, стоматит, воспаление десен, застой желчи.
Азитромицин является макролидом третьего поколения, вызывающим осложнения в 0,7% случаев. Это лекарство способно более концентрировано скапливаться в желудочном и кишечном соке, что способствует его антибактериальному действию. Тем не менее, он не так эффективно справляется с Хеликобактер пилори, как Кларитромицин, поэтому при эрадикации его прописывают, если при употреблении последнего возникают побочные эффекты.
Противобактериальные и противоинфекционные
При эрадикации для уничтожения Хеликобактер пилори могут быть назначены противоинфекционные и противобактериальные средства. Среди них:
- Метронидазол;
- Макмирор или Нифурател.
Метронидазол – противомикробное лекарство из группы нитромидазолов, а потому характеризуется бактерицидным действием. Активное вещество попадает внутрь паразита и распадается на токсические элементы, что приводит к разрушению клеток бактерии. При непродолжительном курсе терапии лекарство редко вызывает осложнения. Среди побочных эффектов – аллергия, рвота, тошнота, ухудшение аппетита, металлический вкус во рту. Препарат придает моче красно-коричневый цвет.
Более эффективным лекарством при эрадикации считается антибактериальное средство Макмирор, действующим веществом которого является нифурател из группы нитрофурана. Препарат препятствует размножению бактерий и угнетает процессы внутри клетки, что приводит к гибели патогенов. При кратковременном курсе лечения осложнения встречаются редко. Макмирор может спровоцировать аллергию, боль в животе, изжогу, тошноту, рвоту.
Эрадикация нередко начинается с использования препаратов висмута, которые способствуют рубцеванию язвы, защищают слизистую от агрессивной среды, образуя на травмированных тканях защитную пленку. Висмутсодержащие препараты продлевают действие пролонгированных лекарств, стимулируют синтез слизи, угнетают формирование пексина, обладают противомикробной активностью по отношению к Хеликобактер пилори на участках, в которые антибиотики плохо проникают.
При эрадикации часто используют противоязвенный препарат Де-нол, активным компонентом которого является висмута субцитрат. Лекарство защищает поврежденные ткани ЖКТ специальной пленкой, активизирует выработку слизи и бикарбонатов, которые снижают кислотность желудочного сока. Под влиянием лекарства в травмированной слизистой ЖКТ скапливаются факторы роста, способствующие быстрому затягиванию язв и эрозии.
Де-Нол хорошо справляется с Хеликобактер пилори, угнетая рост микробов и делая окружающую бактерию среду непригодной для ее обитания. В отличие от многих лекарств висмута Де-Нол хорошо растворяется в желудочном секрете и глубоко просачивается в слизистую желудка и двенадцатиперстной кишки. Здесь он проникает внутрь микробов и разрушает их внешнюю оболочку.
Если препарат назначен кратким курсом, он не оказывает системного влияния на организм, поскольку его основная масса не всасывается в кровоток, а уходит сразу в кишечник. По этой причине основными противопоказанием к употреблению препарата являются аллергия, беременность, период лактации, тяжелое заболевание почек (лекарство выводится с мочой).
Ингибиторы протонного насоса
ИПН избирательно блокируют работу клеток желудка, которые вырабатывают желудочный сок, в состав которого входят такие агрессивные вещества, как соляная кислота и ферменты, которые растворяют белки. Среди таких препаратов можно выделить:
- Омез (Индия). Активный компонент – омепразол. Форма выпуска: капсулы. Эффект достигается в течение часа, действие длится 24 часа.
- Нольпаза (Словения). Действующее вещество: пантопразола натрия сесквигидрат. Эффективность препарата не зависит от приема пищи: в системный кровоток всасывается 77%. Максимальное количество лекарства в крови наблюдается через 2-2,5 часа.
- Рабепразол (выпускают различные производители). Действующее вещество аналогично названию. При язвенной болезни боль стихает в течение суток после первого употребления лекарства, неприятные ощущения полностью исчезают через четыре дня.
- Пантопразол – продается под торговыми марками Санпраз, Нольпаза, Пантап, Улсепан. Активный компонент не только снижает выработку желудочного сока, но и обладает антибактериальной активностью по отношению к Хеликобактер пилори. Лекарство быстро снимает боль, действие длится сутки.
ИПН снижают выработку желудочного сока, что ухудшает условия для нормального развития Хеликобактер пилори и способствует ее уничтожению. Препараты устраняют агрессивное влияние желудочного сока на пострадавшие ткани, способствуя заживлению ран и язв. Снижение кислотности помогает антибиотикам сохранять свою активность внутри желудка и эффективно справляться с бактериями. Все препараты ИПН характеризуются избирательным действием, из-за чего осложнения бывают редко. Побочные эффекты проявляются в мигренях, головокружениях, тошноте, расстройстве стула.
Нормализация микрофлоры после эрадикации
Препараты, обладающие антибактериальным действием, негативно влияют не только на патогенную, но и на полезную флору организма, что может привести к дисбактериозу. Для стабилизации микрофлоры кишечника гастроэнтеролог назначает пробиотики и пребиотики. Препараты отличаются друг от друга тем, что пробиотики являют собой живую культуру полезных микроорганизмов, которые «выращивают» погибшую микрофлору, тогда как пребиотики – синтетические соединения, которые создают необходимые для этого условия.
Одним из таких препаратов является Линекс. Пробиотик содержит три вида живых молочнокислых бактерий, которые необходимы для работы разных отделов кишечника. Молочные бактерии принимают участие в обмене желчных пигментов и кислот, предотвращают развитие патогенной флоры, способствуя увеличению кислотности до уровня, необходимого для подавления вредных бактерий и нормальной работы пищеварительной системы.
Аципол является одновременно пробиотиком и пребиотиком. Препарат содержит в капсулах полезные бактерии (лактобактерии), которые благодаря такой форме доходят до кишечника в невредимом состоянии, минуя агрессивное воздействие желудочного сока. Здесь лактобактерии освобождаются и заселяют кишечник, устраняя дисбактериоз. В составе лекарства присутствуют полисахариды кефирного грибка, которые создают благоприятные условия для развития полезных бактерий.
Бифидумбактерин содержит в своем составе бифидобактерии, которые являются частью нормальной микрофлоры кишечника, а также лактозу, необходимую для их роста после попадания в организм. Пробиотик угнетает развитие патогенной флоры, нормализует баланс между полезными и условно-патогенными бактериями, приводит в порядок работу ЖКТ, стимулирует работу иммунной системы.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе