 [Что такое электролит]
[Что такое электролит]
Электролиты: понятие и свойства
- Магазин реактивов и оборудования
- Блог
- Электролиты: понятие и свойства
-
Электролиты — растворы, содержащие большую концентрацию ионов, обеспечивающих прохождение электрического тока. Как правило, это водные растворы солей, кислот и щелочей.
Это интересно
В организме человека и животных электролиты играют важную роль: к примеру, электролиты крови с ионами железа транспортируют кислород в ткани; электролиты с ионами калия и натрия регулируют водно-солевой баланс организма, работу кишечника и сердца.
Свойства
Чистая вода, безводные соли, кислоты, щелочи ток не проводят. В растворах же вещества распадаются на ионы и проводят ток. Именно поэтому электролиты называют проводниками второго порядка (в отличие от металлов). Электролитами могут быть также расплавы и некоторые кристаллы, в частности диоксид циркония и иодид серебра.
Главное свойство электролитов — способность к электролитической диссоциации, то есть к распаду молекул при взаимодействии с молекулами воды (или других растворителей) на заряженные ионы.
По типу ионов, образующихся в растворе, различают электролит щелочной (электропроводимость обусловлена ионами металлов и ОН-), солевой и кислотный (с ионами Н+ и остатками основания кислоты).
Для количественной характеристики способности электролита к диссоциации введен параметр «степень диссоциации». Эта величина отражает процент молекул, подвергшихся распаду. Она зависит от:• самого вещества;• растворителя;• концентрации вещества;
• температуры.
Электролиты делят на сильные и слабые. Чем лучше реагент растворяется (распадается на ионы), тем сильнее электролит, тем лучше он проводит ток. К сильным электролитам относятся щелочи, сильные кислоты и растворимые соли.
Для электролитов, использующихся в аккумуляторах, очень важен такой параметр, как плотность. От нее зависят условия эксплуатации аккумулятора, его емкость и срок службы. Определяют плотность с помощью ареометров.
Меры предосторожности при работе с электролитами
Самые популярные электролиты, это раствор концентрированной серной кислоты и щелочи — чаще всего гидроксиды калия, натрия, лития. Все они вызывают химические ожоги кожи и слизистых, очень опасные ожоги глаз. Именно поэтому все работы с такими электролитами нужно производить в отдельном, хорошо вентилируемом помещении, используя средства защиты: одежду, маски, очки, резиновые перчатки.• Рядом с помещением, где проводятся работы с электролитами, должна храниться аптечка с набором нейтрализующих средств и кран с водой. • Кислотные ожоги нейтрализуются раствором соды (1 ч.л. на 1 ст. воды).• Ожоги щелочью нейтрализуют раствором борной кислоты (1 ч.л. на 1 ст. воды).• Для промывания глаз нейтрализующие растворы должны быть в два раза слабее.• Поврежденные участки кожи сначала промывают нейтрализатором, а потом мылом и водой.
• Если электролит пролили, его собирают опилками, потом промывают нейтрализатором и вытирают насухо.
При работе с электролитом следует выполнять все требования техники безопасности. Например, кислоту наливают в воду (а не наоборот!) не вручную, а с помощью приспособлений. Куски твердой щелочи в воду опускают не руками, а щипцами или ложками. Нельзя работать в одном помещении с аккумуляторами на разнотипных электролитах, и хранить их вместе тоже запрещается.
Некоторые работы требуют «кипения» электролита. При этом выделяется водород — горючий и взрывоопасный газ. В таких помещениях должна использоваться взрывобезопасная электропроводка и электроприборы, запрещается курение и любые работы с открытым огнем.
Хранят электролиты в пластиковых емкостях. Для работы подходит стеклянная, керамическая, фарфоровая посуда и инструменты.
В следующей статье расскажем подробнее о видах и применении электролита.
Электролит
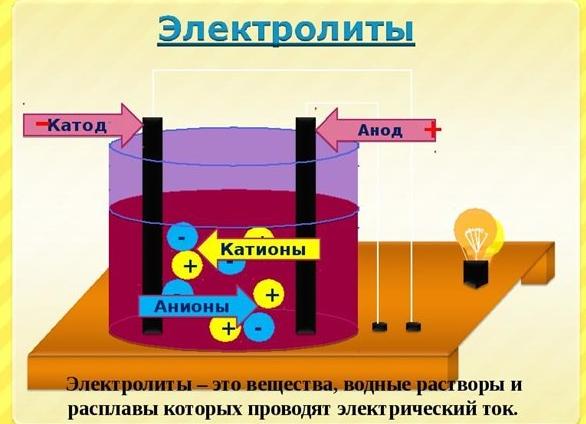
Электролиты – вещества, расплавы или растворы которых проводят электрический ток. К электролитам относятся кислоты, основания и большинство солей.
К электролитам относятся вещества с ионной или сильнополярной ковалентной связью. Первые в виде ионов существуют еще до перевода их в растворенное или расплавленное состояние. К электролитам относятся соли, основания, кислоты.
Рис. 1. Таблица отличие электролитов от неэлектролитов.
Различают сильные и слабые электролиты. Сильные электролиты при растворении в воде полностью диссоциируют на ионы. К ним относятся: почти все растворимые соли, многие неорганические кислоты (например, h3SO4, HNO3, HCl), гидроксиды щелочных и щелочноземельных металлов. Слабые электролиты при растворении в воде незначительно диссоциируют на ионы. К ним относятся почти все органические кислоты, некоторые неорганические кислоты (например, h3CO3), многие гидроксиды (кроме гидроксидов щелочных и щелочноземельных металлов).
Рис. 2. Таблица сильные и слабые электролиты.
Вода также является слабым электролитом.
Как и другие химические реакции, электролитическую диссоциацию в растворах записывают в виде уравнений диссоциации. При этом для сильных электролитов рассматривают процесс как идущий необратимо, а для электролитов средней силы и слабых – как обратимый процесс.
Кислоты – это электролиты, диссоциация которых в водных растворах протекает с образованием ионов водорода в качестве катионов. Многоосновные кислоты диссоциируют ступенчато. Каждая следующая ступень идет все с большим и большим трудом, так как образующиеся ионы кислотных остатков являются более слабыми электролитами.
Основания – электролиты, диссоциирующие в водном растворе с образованием гидроксид-иона ОН- в качестве аниона. Образование гидроксид-иона является общим признаком оснований и обуславливает общие свойства сильных оснований: щелочной характер, горький вкус, мылкость на ощупь, реакцию на индикатор, нейтрализацию кислот и т. д.
Щелочи, даже малорастворимые (например, гидроксид бария Ba(OH)2) диссоциируют нацело, пример:
Соли – это электролиты, диссоциирующие в водном растворе с образованием катиона металла и кислотного остатка. Соли диссоциируют не ступенчато, а нацело:
Электролиты – вещества, подвергающиеся в растворах или расплавах электролитической диссоциации и проводящие электрический ток за счет движения ионов.
Электролитической диссоциацией называется распад электролитов на ионы при растворении их в воде.
Теория электролитической диссоциации (С. Аррениус, 1887) в современном понимании включает следующие положения:
- электролиты при растворении в воде распадаются (диссоциируют) на ионы – положительные (катионы) и отрицательные (анионы). Ионизация происходит легче всего для соединений с ионной связью (солей, щелочей), которые при растворении (эндотермический процесс разрушения кристаллической решетки) образуют гидратированные ионы.
Рис. 3. Схема электролитической диссоциации соли.
Гидратация ионов – экзотермический процесс. Соотношение затраты и выигрыша энергии определяет возможность ионизации в растворе. При растворении вещества с полярной ковалентной связью (например, хлороводород HCl) диполи воды ориентируются у соответствующих полюсов растворяемой молекулы, поляризую связь и превращая ее в ионную с последующей гидратацией ионов. Этот процесс является обратимым и может идти как полностью, так и частично.
- гидратированные ионы устойчивы, беспорядочно передвигаются в растворе. Под действием электрического тока движение приобретает направленный характер: катионы движутся к отрицательному поясу (катоду), а анионы – к положительному (аноду).
- диссоциация (ионизация) – обратимый процесс. Полнота ионизации зависит от природы электролита (соли щелочи диссоциируют практически нацело), его концентрации (с увеличением концентрации ионизация идет труднее), температуры (повышение температуры способствует диссоциации), природы растворителя (ионизация происходит только в полярном растворителе, в частности, в воде).
Электролиты – это соли, кислоты, основания, способные проводить электрический ток. Электролиты бывают сильные и слабые. Также в статье приводится информация кратко о соединениях электролитов.
Средняя оценка: 4.4. Всего получено оценок: 57.
Электролит — это… Что такое Электролит?
Электроли́т — вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований. Электролиты — проводники второго рода, вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов и обладающие вследствие этого ионной проводимостью.
Степень диссоциации
В растворах некоторых электролитов диссоциирует лишь часть молекул. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации[1].
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как: HCl, HBr, HI, HNO3).
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты), основания p-, d-, и f- элементов.
Между этими двумя группами четкой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Использование термина
В естественных науках
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
В технике
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
В электрохимии
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например, электролит золочения).
В источниках тока
Электролиты являются важной частью химических источников тока: гальванических элементов и аккумуляторов.[2] Электролит участвует в химических реакциях окисления и восстановления с электродами, благодаря чему возникает ЭДС. В источниках тока электролит может находиться в жидком состоянии (обычно это — водный раствор), или загущённым до состояния геля.
Электролитический конденсатор
В электролитических конденсаторах в качестве одной из обкладок используется электролит. В качестве второй обкладки — металлическая фольга (алюминий), или пористый, спечённый из металлических порошков блок (тантал, ниобий). Диэлектриком в таких кондесаторах служит слой оксида самого металла, формируемый химическими методами на поверхности металлической обкладки.
Конденсаторы данного типа, в отличие от других типов, обладают несколькими отличительными особенностями:
- Высокая объемная и весовая удельная ёмкость.
- Требование к полярности подключения в цепях постоянного напряжения. Несоблюдение полярности вызывает бурное вскипание электролита, приводящее к механическому разрушению корпуса конденсатора (взрыву).
- Значительные утечки и зависимость электрической ёмкости от температуры.
- Ограниченный сверху диапазон рабочих частот (типовые значения сотни кГц … десятки МГц в зависимости от номинальной ёмкости и технологии).
Примечания
- ↑ Степень диссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита.
- ↑ ГОСТ 15596-82 Источники тока химические. Термины и определения
Что нужно знать об электролите для аккумуляторов
Наверняка значительная часть автомобилистов обладают только поверхностными знаниями об устройстве своего аккумулятора, но иногда так хочется покопаться и узнать, что же там внутри, как в детстве разломать, посмотреть. Ломать не нужно, мы постараемся Вам рассказать.
В пред идущих статьях мы разбирали из чего же состоит АКБ. Если в кратце, то из положительных и отрицательных электродов которые чередуются, а между ними пластмассовые сепараторы. Все остальное пространство заполнено электролитом.
Так что же представляет из себя электролит? Ничего сложного, состав электролита для аккумулятора — это раствор серной кислоты и дистиллированной воды. Итак, по порядку.
Аккумуляторная серная кислота
Серная кислота это тяжелая прозрачная маслянистая жидкость. Она хорошо растворима в воде и не имеет запаха. Процесс растворения кислоты в воде при приготовлении электролита для свинцовых АКБ, сопровождается выделением тепла.
Используется серная кислота согласно ГОСТ 667-83 марки А или серная кислота особой чистоты согласно ГОСТ 142б2-78. Содержание моногидрата серной кислоты нормируется в пределах 92-94 %. Плотность по ГОСТ – 1,830 г/см3. Суммарное содержание примесей — не более 0,03665 %, в их числе марганца — не выше 0,0О01 %, железа — 0,012 %, мышьяка – 0,0001%, хлора — 0,0005 %, окислов азота – 0,0001%.
Дистиллированная вода
Процесс приготовления электролита для свинцовых аккумуляторов невозможен без дистиллированной воды. Не допускается применение технической, питьевой и речной воды. Допускается применение конденсата воды паротурбинных установок с обязательным проведением химического анализа на содержание железа, которое не должно превышать величины 0,0004 %, и меди, с максимально допустимым её содержанием 0,005 %.
Для приготовления дистиллированной воды в лабораториях, на аккумуляторных станциях, в аптеках и лечебных учреждениях обычно применяются электрические дистилляторы.
Дистиллятор модели Д-1 мощностью 4 кВт имеет производительность 5 л/час, модели АД-10 — 10 л/час. Могут применяться и дистилляторы других моделей. При работе с конкретными моделями дистилляторов необходимо руководствоваться их инструкциями по эксплуатации.
Целесообразно не реже 1 раза в полгода проводить анализ воды, получаемой в дистилляторах. Содержание сухих веществ не должно превышать 5 мг/л, аммиака и солей аммония — не более 0,05 мг/л, сульфатов — не более 0,5 «г/л, хлоридов — не более 0,02 мг/л, кальция — не более 1,0 мг/.
Кроме того, полученная вода должна проверяться на содержание железа, тяжелых металлов и нитратов. Результаты сводятся в карту химанализа, на основании которой делается вывод о возможности использования дистиллята для приготовления электролита.
Вода должна соответствовать ГОСТ 6709-72.
Стоимость дистиллированной воды в аптеках и магазинах варьируется от 10 до 20 рублей за 1,5 литра.
Электролит
Электролит для свинцовых батарей представляет собой водный раствор серной кислоты. Серную кислоту и дистиллированную воду применяют с вышеуказанными характеристиками. Для заливки новых стационарных АКБ и вышедших из ремонта, а также для доливки применяется электролит с плотностью 1,18-1,24 г/см3.
Если для приготовления электролита применяется серная кислота с плотностью 1,83 г/см3 — целесообразно работы вести в два этапа. На первом этапе готовится электролит с плотность. 1,4 г/см3. Необходимо обеспечить его остывание до температуры 20С. На втором этапе из электролита с плотностью 1,4 г/см3 готовят электролит необходимой плотности. При двухэтапном процессе степень нагрева раствора серной кислоты будет значительно ниже.
Готовить электролит нужно в чистой эбонитовой, фаянсовой или специальной пластмассовой посуде. Из металлических сосудов можно применять только свинцовые. Применение стеклянной посуды категорически запрещено ввиду возможности разрушения при тепловом ударе.
Вначале в ёмкость вливается мерное количество дистиллированной воды, а потом тонкой струёй, при помешивании стеклянной или эбонитовой палочкой, вливается расчетный объем серной кислоты. Кислоту лучше доливать отдельными порциями.
Необходимо неукоснительно соблюдать следующее правило: лить кислоту в воду, а не наоборот. Оно обусловлено тем, что если вливать воду в кислоту, то вода мгновенно разогревается, вскипает и разбрызгивается, увлекая за собой капли горячей кислоты, падание которых на кожные покровы вызывает ожоги. Именно поэтому все работы необходимо производить в резиновых сапогах, суконном комбинезоне и резиновых перчатках. Так же можно одеть резиновый передник и обязательно защитные очки.
Чтобы приготовить электролит плотностью 1,4 г/см3 из расчета на 1 литр раствора ниже мы приводим таблицу какие пропорции серной кислоты и дистиллированной воды необходимо выдерживать.
Таблицы соотношения серной кислоты и дистиллированной воды
Таблица 1
Для электролита плотностью 1,4 г/см3 нужно выдерживать пропоции из второй таблицы.
Таблица 2
Для приготовлении электролита из плотностью 1,83 г/см3 воспользуйтесь третей таблицей.
Таблица 3
При измерении плотности используют ареометры с пределами измерения 1,1-1,4 г/см3 и ценой деления не грубее 0,005 г/см3 и, поскольку плотность зависит от температуры, термометры на пределы измерения 0÷50С и ценой деления 1С. Термометры не должны иметь деревянных или металлических оправ. Ареометры с указанными пределами измерения и точностью отсутствуют, поэтому применяют набор с более узкими диапазонами измерений.
Как уже упоминалось выше, в процессе приготовления электролита выделяется тепло. В таком случае измерение плотности нагретого электролита будет не корректным, соответственно при измерении необходимо вносить поправку, ну а лучше подождать пока температура станет 20С.
Температурный градиент плотности равен 0,0007 г/см3 на 1С. При температуре электролита выше приведенной, в данном случае 20С, расчетная поправка прибавляется к измеренному значению плотности. Например: температура фактическая равна 30С, разница с приведенной 20С составляет 10С. Градиент 0,0007 х 10 = 0,07 г/см3. К измеренному значению плотности прибавляем поправку, равную 0.007 г/см3.
При фактической температуре 10С разница с приведенной температурой также 10С. Градиент, равный 0,0007 г/см3 умножаем на 10, получаем поправку 0,007 г/см3, но в данном случае поправка вычитается из измеренного значения плотности при температуре 10С.
Необходимо помнить, что заливать электролит температурой выше 25С в аккумуляторы недопустимо.
Физические свойства сернокислотного электролита
Есть еще один физический фактор, который необходимо учитывать, особенно когда приготавливаются большие объемы раствора серной кислоты и дистиллированной воды. Это то обстоятельство, что при смешивании равных объемов серной кислоты и воды, после охлаждении такого раствора его объем будет меньше, чем сумма первоначальных объёмов. Что бы учесть этот фактор нужно обратится к четвертой таблице, в которой указаны величины уменьшения объёмов для растворов серной кислоты различной плотности.
Таблица 4 Сокращение объема раствора
Вязкость
Вязкость это свойство электролита, наиболее существенно влияющее на работоспособность свинцового аккумулятора. Электрохимические процессы, протекающие при работе аккумулятора, носят диффузионный характер. Скорость диффузии, в основном, зависит от вязкости электролита. Именно скоростью диффузии определяется поступление электролита к поверхности и в поры электродов при разряде, особенно при установке жестких (минутных, часовых) режимов разряда.
Чем вязкость выше, тем диффузия медленнее. При понижении температуры на 25С вязкость электролита возрастает в 2 раза, а при температуре в -50С она возрастает почти в 30 раз по сравнению с вязкостью при нормальной температуре. С увеличением вязкости падает ёмкость. Именно поэтому ра6отоспособность свинцовых аккумуляторов при низких температурах ухудшается. Это обстоятельство необходимо учитывать при установке герметичных аккумуляторов с гелевым (загущённым) электролитом.
Удельное сопротивление электролита
Сопротивление электролита, занимающего объем, ограниченный длиной 1 см и сечением в 1 см3, рассчитывается по формуле:
=rS/L
где r – удельное сопротивление Ом см;
L- длина, см.
S — поперечное сечение см2.
Сопротивление изменяется с изменением концентрации и температуры электролита.
Чтобы иметь минимальное внутреннее сопротивление АКБ, желательно применять электролит с наименьшим удельным сопротивлением.
Величины удельных сопротивлений приведены в таблице 5.
Таблица 5. Удельные сопротивления электролита
Удельное сопротивление электролита возрастает при снижении температуры, наиболее значительно при температуре 0С.
Температура замерзания электролита важна, постольку по мере разряда аккумулятора снижается его плотность и, соответственно, температура его замерзания. При замерзании объем электролита увеличивается, что приводит к разрушению сосуда и электродов аккумулятора. Наиболее низкую температуру замерзания имеет электролит плотностью 1,29 г/см3. Стартерные аккумуляторные батареи, эксплуатируемые в суровых условиях, имеют электролит плотностью 1,26-1,30 г/см3, который не замеряет при самых низких возможных температурах.
Для определения температур замерзания электролитов различной плотности следует пользоваться таблицей 6.
Таблица 6. Температура замерзания электролитов
Щелочные электролиты
Обычно для приготовления электролита щелочных аккумуляторов используют едкий калий и едкий литий.
Едкий калий (КОН) — твердое белое кристаллическое вещество, хорошо растворимое в воде. При растворении едкого калия в воде происходит выделение тепла. Согласно ГОСТ 9285-59 калий едкий технический изготовляется трех сортов: высший, А и Б. Содержание едкого калия в высшем сорте не менее 96%, в сорте А — 92% и в сорте Б — 88%. Кроме того, выпускается реактивный едкий калий (ГОСТ 4203-435), содержащий меньше примесей, чем технический едкий калий.
Если электролит приготовляют из едкого калия и едкого лития, то сначала растворяют едкий калий, а затем добавляют едкий литий из расчета 10-20 г на 1 л электролита. Чтобы он остыл после разведения, а также для осаждения примесей необходимо оставить его на 15-20 часов в емкости, закрыв плотно крышкой.
По истечении этого времени очистившийся раствор осторожно сливают в чистую посуду, затем ареометром проверяют плотность, и, если нужно, доводят до нормы, добавляя воду, щелочь или готовый концентрированный электролит.
Рекомендуемую плотность электролита устанавливает завод-изготовитель кадмий-никелевых и железо-никелевых батарей. Если в документации нет жестких рекомендаций, то применяется электролит с плотностью 1,19-1,21 г/см3 при 15С и содержанием 10-20 г/л едкого лития. Раствор с такими параметрами применяется при эксплуатации аккумулятора при температурах не ниже —20С. Если температура ниже, то необходим электролит с плотностью 1,25—1,27 г /см3 без едкого лития.
Для восстановления старых щелочных кадмий-никелевых и железо-никелевых аккумуляторов применяют калиево-литиевый электролит плотностью 1,255—1,279 г/см3 с добавкой 69 г едкого лития на 1 л электролита. Для приготовления электролитов требуемой плотности необходимо руководствоваться таблицей 7.
Таблица 7. Плотность щелочных электролитов
Приготовление щелочных электролитов для железо-никелевых и кадмий-никелевых аккумуляторов
В заключение можно констатировать, что век самостоятельного приготовления электролита в гаражах уже подошёл к концу. В любом автомобильном магазине можно купить готовый и не подвергать себя риску при работе с химическими веществами, например, серной кислотой.