Т форма гемоглобина
Гемоглобин. НАГЛЯДНАЯ БИОХИМИЯ. Ян Кольман, Клаус-Генрих Рем, Юрген Вирт
Гемоглобин
Главная функция эритроцитов (см. с. 268) — транспорт кислорода от легких в ткани и СО2 от тканей обратно в легкие. Высшие организмы нуждаются для этого в специальной транспортной системе, так как молекулярный кислород плохо растворим в воде: в 1 л плазмы крови растворимо только около 3,2 мл О2. Содержащийся в эритроцитах белок гемоглобин (Hb) способен связать в 70 раз больше — 220 мл О2/л. Содержание Hb в крови составляет 140-180 г/л у мужчин и 120-160 г/л у женщин, т. е. вдвое выше по сравнению с белками плазмы (50-80 г/л). Поэтому Hb вносит наибольший вклад в образование рН-буферной емкости крови (см. с. 280).
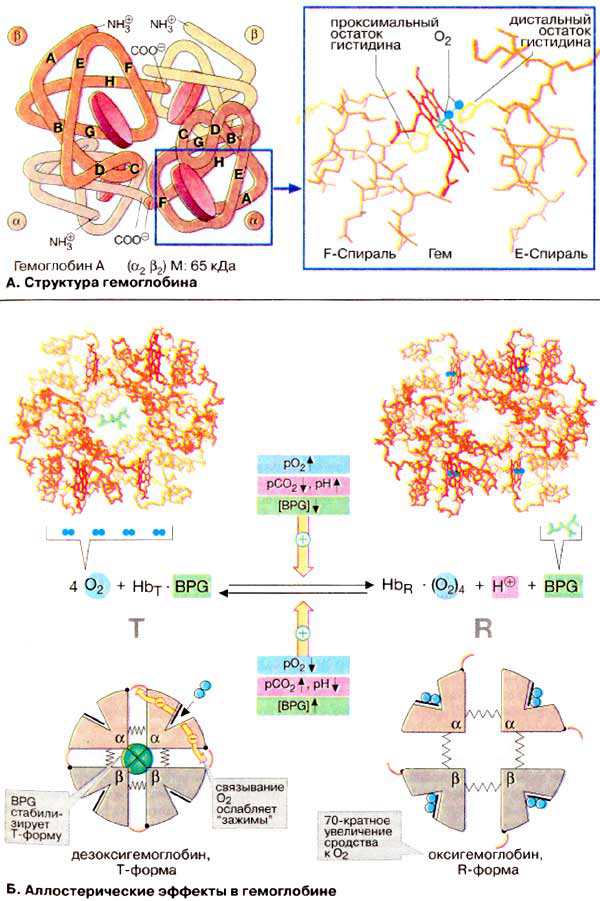
А. Структура гемоглобина
Гемоглобин взрослого организма (HbA, см. ниже) является тетрамером, состоящим из двух α- и двух β-субьединиц с молекулярными массами примерно 16 кДа. α- и β-цепи отличаются аминокислотной последовательностью, но имеют сходную конформацию. Примерно 80% аминокислотных остатков глобина образуют α-спирали, обозначенные буквами А-Н (см. схему). Каждая субъединица несет группу гема (формулу см. на рис. 197) с ионом двухвалентного железа в центре. При связывании O2 с атомом железа в геме (оксигенация Hb) и отщеплении O2 (дезоксигенация) степень окисления атома железа не меняется. Окисление Fe2+ до Fe3+ в геме носит случайный характер. Окисленная форма гемоглобина, метгемоглобин, не способна переносить O2. Доля метгемоглобина поддерживается ферментами на низком уровне и составляет поэтому обычно только 1-2%.
Четыре из шести координационных связей атома железа в гемоглобине заняты атомами азота пиррольных колец, пятая — остатком гистидина глобина (проксимальный остаток гистидина), а шестая — молекулой кислорода в оксигемоглобине и, соответственно, Н2О в дезоксигемоглобине.
Б. Аллостерические эффекты в гемоглобине
Аналогично аспартат-карбамоилтрансферазе (см. с. 118) Hb может находиться в двух состояниях (конформациях): обозначаемых как Т- и R-формы соответственно. Т-Форма (напряженная от англ. tense) обладает существенно более низким сродством к O2 по сравнению с R-формой (на схеме справа). Связывание O2 с одной из субъединиц Т-формы приводит к локальным конформационным изменениям, которые ослабляют связь между субъединицами. С возрастанием парциального давления O2 увеличивается доля молекул Hb в высокоаффинной R-форме (от англ. relaxed). Благодаря кооперативным взаимодействиям между субъединицами с ростом концентрации кислорода повышается сродство Hb к O2, в результате чего кривая насыщения имеет сигмоидальный вид (см. с 276).
На равновесие между Т- и R-формами влияют различные аллостерические эффекторы, регулирующие связывание O2 гемоглобином (желтые стрелки). К наиболее важным эффекторам относятся CO2, Н+ и 2,3-дифосфоглицерат [ДФГ (BPG)] (см. с. 276).
Дополнительная информация
Hb взрослого организма состоит, как упомянуто выше, из двух α- и двух β-цепей (α2β2). Наряду с этой основной формой (HbA1) в крови присутствуют незначительные количества второй формы с более высоким сродством к O2, у второй β-цепи заменены δ-цепя-ми (HbA2, α2δ2). Две другие формы Hb встречаются только в эмбриональном периоде развития. В первые три месяца образуются эмбриональные гемоглобины состава ξ2ε2 и α2γ2. Затем вплоть до рождения доминирует фетальный гемоглобин (HbF, α2δ2), который постепенно заменяется на первом месяце жизни на HbА. Эмбриональный и фетальный гемоглобины обладают более высоким сродством к О2 по сравнению с HbА, так как они должны переносить кислород из системы материнского кровообращения.
Еще по теме:
 ___
___ Дыхательная система: гемоглобин и транспорт газов
ПодробностиДыхательный пигмент гемоглобин играет одну из ключевых ролей в газообмене. Однако существует несолько форм гемоглобина, имеющих разное сродство к кислороду. Также на степень насыщаемости Hb кислородом влияют многие факторы.
1. Кривая насыщения гемоглобина кислородом.При повышении парциального давления кислорода насыщение гемоглобина кислородом прогрессивно увеличивается. При давлении кислорода около 70 мм.рт.ст насыщение гемоглобина практически максимально и далее оно увеличивается совсем незначительно.
2. T- и R- форма гемоглобина.
3. Кривая насыщаемости гемоглобина кислородом в зависимости от температуры, pH, типа гемоглобина (фетальный, нормальный, связанный с 2,3-бисфосфоглицератом).
4. Синтез и метаболизм 2,3-бисфосфоглицерата.
5. Формирование гемоглобина: эмбриональный, фетальный, взрослый минорный и основной.
7. Расположение молекулы 2,3-бисфосфоглицерата в активном центре дезоксигемоглобина.
8. Факторы, влияющие на насыщение гемоглобина кислородом.
9. Транспорт углекислого газа в крови.
10. Каротидное тельце (гломус) реагирует на содержание кислорода в крови и гипоксию (высвобождаются катехоламины и стимулируют языко-глоточный нерв).
11. Горная болезнь и гипокситерапия.
Гипокситерапия - это способ терапии различных заболеваний при помощи создания условий гипоксии для организма. Человек дышит воздухом со сниженным содержанием кислорода. Механизм действия и эффективность метода заключаются в мобилизации скрытых резервов организма, более эффективной работе метаболических систем, активацией антиоксидантной защиты и ускоренным разрушением метаболитов.
Гипокситерапевтический эффект может быть достигнут нахождением человека в горах на высоте 3-4 км.
На больших высотах у неподготовленного человека происходят патологические изменения: вначале обратимые, а затем и необратимые.
Развивается горная болезнь. Патогенез горной болезни связан с механизмами гипобарической гипоксии. Начальные проявления: повышенная утомляемость, головная боль, тошнота, головокружение. Далее поражения становятся более серьезные. У горной болезни два основных органа-минеши: головной мозг и легкие.
Возникает высокогорный отек легких (он может начаться уже на высоте 3000 метров, нарушается дыхание, газообмен сильно затрудняется) и развивается отек мозга, что приводит к галлюцинациям.
12. Клеточный сенсор парциального давления кислорода.
13. Апноэ во время сна: это кратковременная остановка дыхания. Оно может быть связано с обструктивных механизмом и с центральным механизмом.
При обструктивном апноэ возникает препятствие потоку воздуха в дыхательных путях, а ритм дыхательных движений и сокращения дыхательной мускулатуры в норме.
При центральном апноэ страдает дыхательный центр могза, нарушается ритмичная генерация импульсов и как следствие нарушаются ритмичные сокращения дыхательных мышц.
Формы гемоглобина.
Гемоглобин не связанный с кислородом называют: дезокси-гемоглобин, ферро-гемоглобин, восстановленный гемоглобин (Нв). Гемоглобин связанный с кислородом (восстановленный) – это окси-гемоглобин (НвО2). Угарный газ хорошо связывает гемоглобин – карбокси-гемоглобин (НвСО). MetНв – это окисленный гемоглобин, не соединяется ни с кислородом, ни с угарным газом, но легко образует комплексы с цианидами (используется при лечении).
Глобин взрослого человека представляет собой тетрамер (a2- и b2-цепи), соединяются цепи не ковалентными связями поочерёдно. В молекуле гемоглобина 4 полипептидных цепи и каждая из них содержит по одному гему. Значит, каждая молекула гемоглобина связывает 4 молекулы кислорода. Связь гемоглобина с кислородом осуществляется за счёт координационной связи между атомом железа и атомами азот-гистедина в полипептидной цепи. Гемовый карман – это расщелина между спиралями, куда встраивается Гем. Проксимальный гистедин в a-цепи – это 87 остаток, в b-цепи – это 92 остаток. Дистальный остаток гистедина в a-цепи – это 58, в b-цепи – 63. Связывание кислорода происходит только с восстановленным железом!
Гетерогенность гемоглобина связана с различием строения глобина:
1. Нормальные гемоглобины.
2. Аномальные гемоглобины – их наличие сопровождается каким либо заболеванием.
Гемоглобины начинают синтезироваться с 6й недели эмбриогенеза. Нормальные гемоглобины – это те гемоглобины, которые появляются в различные этапы жизни:
- Эмбриональный гемоглобин (НвF) – существует в эмбриональном периоде жизни человека; имеет 2 a-цепи и 2 гамма-цепи. НвF имеет большее сродство к кислороду, чем НвА. Нормальный гемоглобин (НвА) – имеет 2 a-цепи и 2 b-цепи.
- Минорные гемоглобины – это гемоглобины, которые в следовых количествах встречаются и у взрослых людей. Гемоглобин А2 имеет a-цепь и дельта-цепь, его содержание в крови 2-3%; появляется через 9-12 недель после рождения. Другие минорные гемоглобины – Нв1в и Нв1с; их состав: 2 a-цепи и 2 b-цепи – эти цепи модифицированные (эти гемоглобины образуются за счёт не ферментативного присоединения к N-концевым остаткам Валина b-цепей молекулы глюкоза-6-фосфата – его 6%). Нв1с образуется из Нв1в (его 1%).
Аномальные гемоглобины характеризуются недостатком функций гемоглобина и чаще всего – это генетически детерминированные мутации последовательностей аминокислотных цепей. В зависимости от проявления эти гемоглобины делятся:
1. Гемоглобины с изменённой растворимостью. Например, НвS или гемоглобин, вызывающий серповидно-клеточную анемию. У него в 6 положении b-цепи происходит замена АК: с Глутамина на Валин. Такое изменение АК-последовательности приводит к тому, что в дезокси-форме гемоглобин теряет растворимость, молекулы его агрегируют друг с другом, образуя нити и изменяя форму клетки. Лечение: категорическое запрещение тяжелой физической работы и лекарственная терапия.
2. Гемоглобины с изменённым сродством к кислороду – у них замены происходят в областях либо субъединичных контактов, либо в области гемового кармана. Например, НвМ – мутация a-цепи затрагивает остаток Гистидина (58 остаток) – происходит замена на остаток Тирозина. В результате происходит образование MetНв.
3. Гемоглобины с изменённой устойчивостью. Например, НвС также, как и в случае с Нвсb6 – плохо удерживает Гем, в результате чего Гем может выходить и формировать осадок в цитоплазме. В итоге на мембрану налипает осадок и она становиться не устойчивой и разрушается.
Нормальные формы гемоглобина
Существует несколько нормальных вариантов гемоглобина:
HbР – примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7-12 неделями жизни,
HbF – фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев,
HbA – гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина,
HbA2 – гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи,
HbO2 – оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94-98% от всего количества гемоглобина,
HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях, в венозной крови составляет 15-20% от всего количества гемоглобина.
Патологические формы гемоглобина
HbS – гемоглобин серповидно-клеточной анемии.
MetHb – метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. Такая форма обычно образуется спонтанно, в этом случае ферментативных мощностей клетки хватает на его восстановление. При использовании сульфаниламидов, употреблении нитрита натрия и нитратов пищевых продуктов, при недостаточности аскорбиновой кислоты ускоряется переход Fe2+ в Fe3+. Образующийся metHb не способен связывать кислород и возникает гипоксия тканей. Для восстановления ионов железа в клинике используют аскорбиновую кислоту и метиленовую синь.
Hb-CO – карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Он постоянно присутствует в крови в малых концентрациях, но его доля может колебаться от условий и образа жизни.
Угарный газ является активным ингибитором гем-содержащих ферментов, в частности, цитохромоксидазы4-го комплекса дыхательной цепи.
HbA1С – гликозилированный гемоглобин. Концентрация его нарастает при хронической гипергликемии и является хорошим скрининговым показателем уровня глюкозы крови за длительный период времени.
Миоглобин тоже способен связывать кислород
Миоглобин является одиночной полипептидной цепью, состоит из 153 аминокислот с молекулярной массой 17 кДа и по структуре сходен с β-цепью гемоглобина. Белок локализован в мышечной ткани. Миоглобин обладает более высоким сродством к кислороду по сравнению с гемоглобином. Это свойство обуславливает функцию миоглобина – депонирование кислорода в мышечной клетке и использование его только при значительном уменьшении парциального давления О2 в мышце (до 1-2 мм рт.ст).
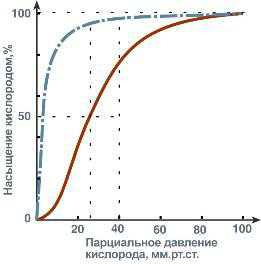
Кривые насыщения кислородом показывают отличия миоглобина и гемоглобина:
одно и то же 50%-е насыщение достигается при совершенно разных концентрациях кислорода – около 26 мм рт.ст. для гемоглобина и 5 мм рт.ст. для миоглобина,
при физиологическом парциальном давлении кислорода от 26 до 40 мм рт.ст. гемоглобин насыщен на 50-80%, тогда как миоглобин – почти на 100%.
Таким образом, миоглобин остается оксигенированным до того момента, пока количество кислорода в клетке не снизится до предельных величин. Только после этого начинается отдача кислорода для реакций метаболизма.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе