Микоплазма гениталиум пцр
Микоплазма (Mycoplasma genitalium)
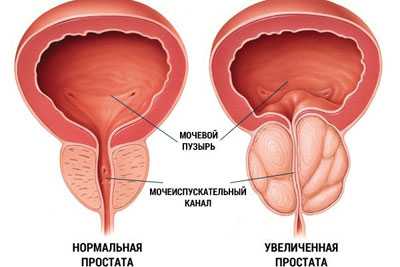
Mycoplasma genitalium – считается самой патогенной из всех микоплазм. Большинство микоплазм (уреаплазм) являются условно патогенными, они могут длительно существовать в организме, но вызывают инфекционно-воспалительные заболевания органов мочеполовой системы только при стрессе, изменении гормонального фона, при снижении иммунитета.
Mycoplasma genitalium была открыта в 1981 году в Лондоне. Она обнаруживается у женщин и у мужчин на слизистых оболочках мочеполовой системы. В отличие от М.hominis, M.genitalium не обнаруживается в составе патогенной флоры у женщин с бактериальным вагинозом.
Доказана роль Mycoplasma genitalium в развитии воспалительных заболеваний органов малого таза. У мужчин она вызывает негонококковый уретрит у мужчин. Прикрепляясь к мембране сперматозоидов, микоплазма снижает их активность, что становится причиной бесплодия. Следует отметить, что для уретритов, вызванных M. genitalium, не характерно бессимптомное течение, чаще эти процессы имеют выраженную клиническую картину.
Вызывать воспалительный процесс в органах малого таза M. genitalium может самостоятельно либо в ассоциации с вирусами или бактериями, чаще всего с трихомонадами.
У женщин выявляется при остром эндометрите или аднексите.
Самым чувствительным методом диагностики микоплазмы (Mycoplasma genitalium) является полимеразная цепная реакция (ПЦР), которая обнаруживает ДНК Mycoplasma genitalium в соскобе из мочеполовых органов – мочеиспускательного канала (уретры), влагалища, цервикального канала.
ПЦР обнаруживает определённые фрагменты ДНК микоплазмы: уникальные, характерные только для Mycoplasma genitalium участки гена P69. Эти фрагменты удваиваются при каждом цикле реакции до определённого количества копий. Копии распознаются методом электрофореза с точным определением, какому микроорганизму принадлежит данный фрагмент ДНК.
Чувствительность анализа высокая – возможно обнаружение Mycoplasma genitalium, если в 5 мкл пробы присутствовало 200 молекул ДНК микоплазмы.
Специфичность анализа – 99%. Это означает, что в 99% случаев реакция не даёт ложноположительного результата, если микоплазма в организме отсутствует.
Показания к выполнению анализа
Выявление причин хронических инфекционных заболеваний органов мочеполовой системы (негонококковый уретрит, острый эндометрит, аднексит).
Планирование беременности (обследование обоих партнёров).
Беременность.
Бесплодие женское и мужское.
Контроль эффективности лечения антибактериальными препаратами (контроль проводится не ранее чем через месяц после окончания лечения).
Подготовка к исследованию
За 4 недели до исследования прекратить приём антибактериальных препаратов.
За 36 часов до взятия соскоба исключить половые контакты.
Туалет половых органов за сутки до анализа выполнять только тёплой водой, без применения средств для интимной гигиены, антибактериального мыла.
Женщинам:
- нельзя сдавать анализ во время менструации и в первых 2 дня после её завершения,
- нельзя спринцеваться, вводить вагинальные свечи,
- временной интервал от последнего мочеиспускания до взятия соскоба не менее полутора часов.
Мужчинам:
- временной интервал от последнего мочеиспускания до взятия соскоба не менее трёх часов.
Материал для исследования
Соскоб из уретры у мужчин или из цервикального канала у женщин.
Интерпретация результатов
Качественный анализ, результат в виде: отрицательно/положительно.
Норма: отрицательный результат («ДНК Mycoplasma genitalium в образце не обнаружена» или «нет инфицирования Mycoplasma genitalium»).
Отрицательный результат возможен и в случае, когда в образце содержится недостаточно ДНК микоплазмы, необходимой для анализа.
Положительный результат: «инфицирование Mycoplasma genitalium» или «в образце обнаружена ДНК Mycoplasma genitalium».
Лечение уретритов, вызванных MYCOPLASMA GENITALIUM
Установлено, что человек является естественным «хозяином» 13 видов микоплазм, из которых возможными возбудителями уретритов могут являться Mycoplasma (M.) hominis, M. genitalium и Ureaplasma (U.) urealyticum. Кроме этих видов микоплазм в урогенитальном тракте также обнаруживают M. fermentans, M. primatum, M. pirum, M. spermatophilum, M. penetrans, M. pneumoniae.
Вопрос о роли генитальных микоплазм в этиологии негонококковых уретритов (НГУ) остается нерешенным из-за широкого распространения этих микроорганизмов и их частого выявления у лиц, не имеющих клинической симптоматики. Мнения исследователей по данному вопросу расходятся. Одни авторы склонны относить микоплазмы к облигатным патогенам, вызывающим уретриты, цервициты, простатиты, послеродовые эндометриты, пиелонефриты, бесплодие, различную патологию беременности и плода. Соответственно, по мнению этих авторов, следует добиваться эрадикации микоплазм в случае их выявления. Другие считают, что микоплазмы являются условно-патогенной флорой урогенитального тракта и лишь при определенных условиях способны вызывать инфекционно-воспалительные заболевания мочеполовых органов. Большинство зарубежных авторов относят все микоплазмы, за исключением M. genitalium, к условно-патогенной флоре. Именно поэтому в МКБ-10 такого заболевания, как микоплазмоз, уреаплазмоз или уреаплазменная инфекция, не зарегистрировано. По мнению многих исследователей, из микоплазм без всяких оговорок к числу патогенов, способных вызывать уретриты, можно отнести только M. genitalium.
Обобщенные данные об эпидемиологии M. genitalium были представлены David Taylor-Robinson (2001) на основе анализа работ 19 наиболее авторитетных исследователей, согласно которым эти микроорганизмы выделяли у 10–50% больных НГУ и у 0–17,7% здоровых лиц. Позже N. Dupin et al. (2003) было показано, что исчезновение этих микроорганизмов из уретры сопровождается разрешением уретрита и, наоборот, рецидив заболевания может быть связан с использованием препаратов, недостаточно активных в отношении M. genitalium.
Клиническая картина уретрита, при котором обнаруживаются микоплазмы, как и при инфицировании хламидиями, не имеет патогномоничных симптомов. M. genitalium чаще обнаруживают у лиц с хроническими уретритами, вероятной причиной рецидивирования которых она является. L. Mena et al. (2002) показали, что пациенты с M. genitalium-ассоциированными уретритами в меньшей степени, чем больные с гонококковыми уретритами, предъявляют жалобы на дизурию и выделения, а выделения у них гораздо реже носят гнойный характер.
Диагностика. Выявление M. genitalium в материале из урогенитального тракта проводится только методом полимеразной цепной реакции (ПЦР). Исследование позволяет очень быстро — в течение суток — выявить ДНК возбудителя в соскобе из урогенитального тракта и определить его видовую принадлежность. Культуральное исследование на селективных средах используется для выявления M. hominis и U. urealyticum.
Лечение
Как и в большинстве случаев выявления условно-патогенной флоры, для микоплазм выделяют ряд факторов, способствующих развитию инфекционно-воспалительных процессов. Наиболее важными из них являются иммунные нарушения, изменения гормонального статуса, массивность колонизации, ассоциации с другими бактериями. Все эти факторы, а также вид возбудителя, давность инфицирования, историю предшествовавшего лечения, наличие сопутствующей патогенной и условно-патогенной флоры следует учитывать при определении тактики ведения больных.
Этиотропное лечение НГУ, вызванных M. genitalium, основывается на применении антибактериальных препаратов различных групп. Активность препаратов в отношении любой инфекции определяется минимальной подавляющей концентрацией (МПК) в исследованиях in vitro. Показатели МПК, как правило, коррелируют с результатами клинического излечения. Оптимальными препаратами считаются антибиотики с наименьшей МПК, но следует помнить о важности таких параметров, как биодоступность, способность к созданию высоких внутритканевых и внутриклеточных концентраций, переносимость лечения и комплаентность больных.
Для выбора схемы адекватной терапии в конкретных случаях рекомендуется лабораторное определение чувствительности выделенных культур к различным антибиотикам. Но проблема заключается в том, что это в основном касается выявленной сапрофитной флоры. Так, многие авторы отмечают способность микоплазм быстро приобретать устойчивость к антибактериальным препаратам при их пассировании in vitro. Следовательно, необходимо тестирование свежевыделенных от больных штаммов. Другая сложность состоит в том, что при выявлении микоплазм чувствительность к антибиотикам in vitro не обязательно коррелирует с положительным эффектом in vivo. Это может быть связано с фармакокинетикой препаратов. Указанные факторы необходимо учитывать при назначении этиотропной терапии, которая во многих случаях может являться частью комбинированной терапии, особенно при смешанных инфекциях.
Европейское (2001) и Американское (2006) руководства по ведению больных с уретритами содержат рекомендации, согласно которым следует проводить лечение НГУ по базовым и альтернативным схемам.
Базовые схемы:
- азитромицин — 1,0 г внутрь, однократно;
- доксициклин — 100 мг 2 раза в день в течение 7 дней.
Альтернативные схемы:
- эритромицин — 500 мг 4 раза в день в течение 7 дней или 500 мг 2 раза в день в течение 14 дней;
- офлоксацин — 200 мг 2 раза в день, или по 400 мг 1 раз в день, или по 300 мг 2 раза в день в течение 7 дней;
- левофлоксацин — по 500 мг 1 раз в день в течение 7 дней;
- тетрациклин — 500 мг 4 раза в день в течение 7 дней.
Из приведенных схем видно, что основными антибиотиками, рекомендованными для лечения НГУ, являются препараты тетрациклинового ряда, макролиды и фторхинолоны.
Если обобщить рекомендации, изложенные в основных отечественных руководствах («Федеральное руководство по использованию лекарственных средств», «Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем» (под ред. акад. РАМН А. А. Кубановой), «Методические материалы по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем, и заболеваний кожи (протоколы ведения больных)», изданных ЦНИКВИ), то можно представить следующие схемы этиотропного лечения НГУ, принятые в России.
Антибиотики тетрациклинового ряда
Основные препараты:
- доксициклин — по 100 мг 2 раза в сутки не менее 7–14 дней. Первая доза при приеме препарата составляет 200 мг.
Альтернативные препараты:
- тетрациклин — по 500 мг 4 раза в сутки в течение 7–14 дней;
- Метациклин — по 300 мг 4 раза в сутки в течение 7–14 дней.
Макролиды
Основные препараты:
- азитромицин — однократный прием 1,0 г или по 250 мг 1 раз в сутки в течение 6 дней. Препарат принимают за 1 ч до еды или через 2 ч после еды;
- джозамицин — по 500 мг 2 раза в сутки в течение 7–14 дней.
Альтернативные препараты:
- эритромицин — по 500 мг 4 раза в день в течение 7–14 дней;
- рокситромицин — по 150 мг 2 раза в сутки в течение 7–14 дней;
- кларитромицин — по 250 мг 2 раза в сутки в течение 7–14 дней;
- мидекамицин — по 400 мг 3 раза в сутки в течение 7–14 дней.
Фторхинолоны
- офлоксацин — по 200–300 мг 2 раза в день в течение 7–14 дней;
- спарфлоксацин — по 200 мг 1 раз в сутки в течение 10 дней (в первый день дозу удваивают);
- левофлоксацин — по 500 мг 1 раз в сутки в течение 10 дней;
- пефлоксацин — по 600 мг 1 раз в сутки в течение 7–14 дней.
Препараты тетрациклинового ряда — самые распространенные лекарственные средства для этиотропного лечения больных НГУ, вызванных M. genitalium. И хотя доксициклин применяется в лечении различной патологии несколько десятилетий, его активность против главных возбудителей НГУ остается высокой (D. Kilic et al., 2004).
Именно поэтому, согласно всем упоминавшимся выше рекомендациям, препаратом выбора при лечении НГУ является доксициклин. Преимуществом его использования является достаточно высокая эффективность и относительно небольшая стоимость лечения. Доксициклин по сравнению с тетрациклином имеет более высокую биодоступность, более длительный период полувыведения и лучше переносится. Кроме того, при использовании доксициклина, в отличие от других тетрациклинов, нет необходимости соблюдать диету, разработанную с учетом возможности связывания тетрациклинов с ионами Са2+. Наиболее частыми побочными эффектами при приеме препаратов тетрациклинового ряда являются тошнота, рвота, диарея, аллергические реакции. Эти реакции значительно менее выражены при использовании доксициклина моногидрата, а не традиционного доксициклина гидрохлорида. Нейтральная реакция доксициклина моногидрата (Юнидокс Солютаб) исключает возникновение эзофагитов, встречающихся при применении других форм доксициклина. Доксициклина моногидрат выпускается в уникальной лекарственной форме таблеток солютаб, которые могут приниматься внутрь целиком, могут быть разделены на части или разжеваны, могут быть растворены в воде с образованием сиропа-суспензии (при растворении в 20 мл воды) или раствора-суспензии (при растворении в 100 мл воды). Биодоступность доксициклина моногидрата в указанной форме составляет 95%, что практически соответствует внутривенной инфузии. Следовательно, удачное сочетание химической формулы (моногидрат) и лекарственной формы (солютаб) делает препарат Юнидокс Солютаб безопасным, а лечение с его помощью — высококомплаентным.
В период лечения препаратами группы тетрациклинов больным необходимо избегать инсоляции из-за возможности фотосенсибилизации.
Этого побочного действия совершенно лишены антибиотики из группы макролидов. Все упомянутые руководства к препаратам выбора при лечении НГУ относят макролидный антибиотик азитромицин. Этому способствуют уникальные фармакокинетические характеристики азитромицина: продолжительный период полувыведения, высокий уровень всасывания и устойчивость к кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, а также возможность проникновения внутрь клетки. Благодаря тому, что высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее 7 сут, с появлением азитромицина впервые возникла возможность эффективного лечения больных хламидийной инфекцией однократным приемом антибиотика внутрь. Оригинальным и наиболее известным препаратом азитромицина является Сумамед, который используется в Российской Федерации с начала 90-х годов прошлого века.
Преимуществами всех современных макролидных антибиотиков перед первым антибиотиком из этой группы эритромицином являются более высокая эффективность, улучшенная фармакокинетика, хорошая переносимость и меньшая кратность приема.
При приеме макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Наиболее благоприятный, по сравнению с другими макролидами, профиль безопасности имеет джозамицин. Частота побочных эффектов при его приеме не превышает 2–4%. Препарат не обладает гепатотоксичностью и почти не изменяет нормальную микрофлору кишечника. На нашем фармацевтическом рынке джозамицин пока представлен единственным препаратом с торговым названием Вильпрафен.
Необходимо обратить внимание: микоплазмы могут быть устойчивы к «старым» макролидам (эритромицин, спирамицин, олеандомицин) и стрептограминам, но высоко чувствительны к новейшим макролидам (джозамицин, азитромицин, кларитромицин) и линкозаминам.
Следующую группу препаратов, обладающих высокой активностью против широкого спектра возбудителей НГУ (и в том числе M. genitalium), составляют фторхинолоны.
Такие фторхинолоны, как офлоксацин и спарфлоксацин, особенно высокоэффективны при НГУ, сопровождающихся массивной колонизацией условно-патогенной сапрофитной флоры, так как обычно эта флора чувствительна к данным антибактериальным препаратам. Их «лидирующее положение» обусловлено широтой антибактериального спектра, высокой бактерицидной активностью, отличными фармакокинетическими характеристиками (быстротой всасывания, высокими концентрациями препарата в тканях, клетках, биологических жидкостях), низкой токсичностью. При лечении спарфлоксацином достигается более высокая комплаентность, так как препарат принимают лишь 1 раз в сутки. По данным Ю. Н. Перламутрова и соавт. (2002), спарфлоксацин высокоэффективен при микоплазменной и уреаплазменной инфекциях. На российском фармацевтическом рынке спарфлоксацин продается под торговым названием Спарфло, а среди дженериков офлоксацина в последнее время все большую популярность завоевывает препарат Офлоцид.
Как и тетрациклины, фторхинолоны обладают фотосенсибилизирующим эффектом. Кроме того, препараты из группы фторхинолонов противопоказаны больным с нарушением функции печени и почек. Из побочных реакций после приема фторхинолонов могут наблюдаться диспептические расстройства, тошнота, рвота, головокружение, аллергические реакции, тендиниты.
Таким образом — на основании проведенного обзора литературы, — при лечении больных с уретритами, вызванными M. genitalium, следует отдавать предпочтение доксициклину, новейшим макролидам и фторхинолонам. При рецидивирующем течении инфекции рассматривается вопрос об удлинении сроков приема антибиотиков и применении иммунотропных препаратов.
М. А. Гомберг, доктор медицинских наук, профессор А. М. Соловьев, кандидат медицинских наук, доцент И. Н. Анискова В. П. Ковалык, кандидат медицинских наук ЦНИКВИ, МГМСУ, Москва
Анализы на микоплазму гениталиум: ПЦР, посев и идентификация урогенитальных микоплазм
Опубликовано: 05 ноя 2013, 11:26 Разновидность гениталиум является опаснейшим патогенном, способным колонизировать мочеполовую систему человека. Неэффективность лечения данного вируса и заболеваний, которые получают осложнения при его присутствии в организме, вызвана лишь тем, что проводится поздняя диагностика. Чтобы цервицит или уретрит был вылечен достаточно быстро, медики назначают анализы для обнаружения микоплазмы гениталиум методом ПЦР. Это самый современный и эффективный способ выявления вируса, хотя в некоторых лабораториях используется еще и посев на микоплазму гениталиум.
Разновидность гениталиум является опаснейшим патогенном, способным колонизировать мочеполовую систему человека. Неэффективность лечения данного вируса и заболеваний, которые получают осложнения при его присутствии в организме, вызвана лишь тем, что проводится поздняя диагностика. Чтобы цервицит или уретрит был вылечен достаточно быстро, медики назначают анализы для обнаружения микоплазмы гениталиум методом ПЦР. Это самый современный и эффективный способ выявления вируса, хотя в некоторых лабораториях используется еще и посев на микоплазму гениталиум.
Не каждый анализ, проведенный даже в стенах самой современной лаборатории, покажет наличие микоплазмоза, да и не обязательно наличие этих вирусов указывает на серьезное заболевание у пациента. Только врач, проведя различные диагностики, изучив их, может констатировать развитие болезни, требующей лечения. Наиболее точные результаты показывают посев на микоплазму гениталиум, ИФА и ПЦР. В редких случаях больным предлагают ПИФ или генетическое зондирование.
Метод ИФА – путь для обнаружения возбудителя
Материалом для иммуноферментного анализа служит кровь пациента. После того, как в организм во время контакта с больным человеком попали вирусы, в крови начинают образовываться антитела. Они принадлежат к различным классам - A, M, G, L. Каждая группа антител вырабатывается к конкретному возбудителю и на строго обозначенном сроке болезни. Некоторые группы антител к микоплазме гениталиум остаются даже после лечения, поэтому результат может оказаться ложноположительным после пройденного курса лечения. Метод ИФА не может дать точный ответ и на ранних сроках развития заболевания, когда в крови еще не успели появиться антитела. Использование данного метода для обнаружения микоплазмы гениталиум эффективно и надежно лишь в сочетании с ПЦР. Иногда требуется идентификация урогенитальных микоплазм и представление о точном количестве вируса, присутствующего на слизистых оболочках. Пациенту необходимо знать, что перед сдачей этого анализа нельзя есть, то есть венозная кровь для ИФА берется утром натощак.
ПЦР - точная диагностика
Врач назначает ПЦР на микоплазму гениталиум не при всех заболеваниях урогенитального тракта. Поводом для похода в лабораторию может стать несколько причин:
- Сомнительные результаты ИФА
- Невозможность забеременеть или выносить ребенка без видимых причин или угроз
- Урогенитальные инфекции с осложнениями
- Контроль над состоянием больного после проведенной терапии
В качестве исследуемого материала при проведении ПЦР на микоплазму гениталиум берется мазок из влагалища, сперма, выделения. Если у мужчин выявляется наличие микоплазмы в урогенитальном тракте, то анализ проводится в любой день. Желательно проводить его с утра, через 2 часа после посещения туалета. Женщинам нельзя сдавать анализ на микоплазму гениталиум непосредственно в критические дни. Желательно прийти в лабораторию не раньше, чем на 7 день менструального цикла.
Расшифровка анализа на микоплазму гениталиум
 Если пациент сдавал анализ на выявление патогенных вирусов в первый раз, то врач обращает внимание на количество антител или самого возбудителя (в зависимости от метода исследования). Положительный результат всегда определяет наличие микоплазменной инфекции. Однако ее присутствие опасно, когда в крови имеется данный вирус в большом количестве и результаты показывают присутствие антител IgM. Если их количество при последующем исследовании будет расти, значит, инфекция продолжает распространяться и требуется комплексное лечение.
Если пациент сдавал анализ на выявление патогенных вирусов в первый раз, то врач обращает внимание на количество антител или самого возбудителя (в зависимости от метода исследования). Положительный результат всегда определяет наличие микоплазменной инфекции. Однако ее присутствие опасно, когда в крови имеется данный вирус в большом количестве и результаты показывают присутствие антител IgM. Если их количество при последующем исследовании будет расти, значит, инфекция продолжает распространяться и требуется комплексное лечение.
загрузка...
загрузка...
загрузка...
Интересные материалы по этой теме!
04 ноя 2013, 22:46Микоплазмоз у собакМикоплазмоз у собак одно из самых распространенных заболеваний. Им болеют особи всех пород и всех возрастов. Причиной... 05 ноя 2013, 10:02Микоплазмоз у кошекМикоплазмоз кошек (фото) является широко распространенным заболеванием, встречаемым не только у бездомных животных, но и у домашних... 05 ноя 2013, 10:34Как передается микоплазма гениталиум?В организме даже здорового человека присутствуют маленькие жители семейства Mycоplasmataceae. Часть из них совершенно безвредные, но...загрузка...
загрузка...
загрузка...
загрузка...
Микоплазма Mycoplasma genitalium, полимеразная цепная реакция (ПЦР)
Микоплазмы – примитивные бактерии, которые могут обитать внутри клеток организма-хозяина, в том числе и человека. Существует много групп микоплазм, часть из которых могут вызывать заболевания мочеполовой системы у человека – микоплазмозы.
Микоплазмозы, наряду с хламидиозом, гонореей и трихомонозом, являются одними из наиболее распространённых инфекций, передающихся половым путём (ИППП). Источником инфекции является человек, больной микоплазмозом, или здоровый носитель микоплазм. При этом указанные инфекции часто сочетаются, усложняя лечение и диагностику заболевания. В конечном итоге, жизнедеятельность микоплазм в клетках человека может привести к воспалительным заболеваниям малого таза и мочеполовой системы (уретрит, простатит и вагинит) и стать причиной развития бесплодия как у женщин, так и у мужчин. Кроме того, среди последствий микоплазмоза отмечают патологии беременности и нарушения развития плода, спонтанные аборты и преждевременные роды.
Среди рода микоплазм отмечают Mycoplasma genitalium. В отличие от других видов микоплазм и уреаплазм, относительно микоплазмы Mycoplasma genitalium существует чёткая позиция специалистов: эта инфекция является безусловно патогенною. При выяснении причин бесплодия или воспалительных заболеваний малого таза исследование на наличие микоплазмы Mycoplasma genitalium проводится обязательно.
Выявление этого вида микоплазм проводится исключительно с помощью ПЦР – полимеразной цепной реакции, поскольку результаты определения антител ненадёжны. Суть метода ПЦР состоит в том, что с помощью специальной методики и реактивов генетическая информация микоплазмы (ДНК) многократно копируется в лабораторных условиях, увеличивая свою концентрацию в два раза на каждом цикле копирования. Это даёт возможность выявить вирус или бактерию даже в тех случаях, когда её содержание составляет лишь сотню на миллилитр крови. Второе уникальное преимущество метода ПЦР – это его чрезвычайная, практически 100% избирательность, по отношению к конкретному возбудителю заболевания. Если генетическая информация тестируемой бактерии или вируса в пробе отсутствует – то она не копируется и не определяется. Для проведения анализа на наличие микоплазмы методом полимеразной цепной реакции можно использовать различные биологические материалы – кровь, соскоб с уретры, сок простаты, сперму и т. д.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе