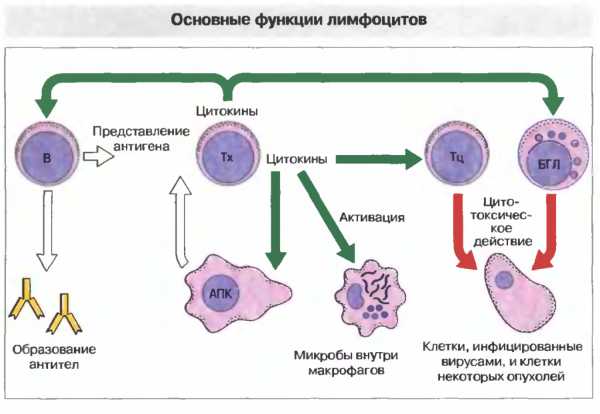
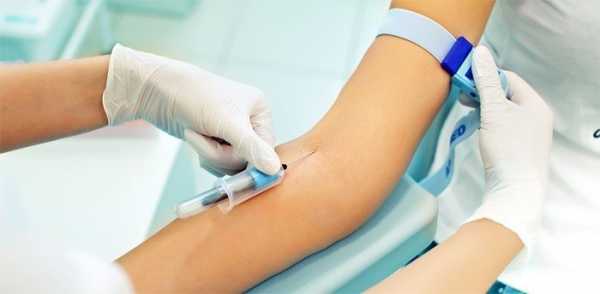
Кальцитонин и паратгормон
Механизм действия паратгормона и кальцитонина
| Паратгормон | Кальцитонин |
| в костях - стимулирует мобилизацию и выход в кровь Са + | в костях - стимулирует отложение Са2+ |
| в кишечнике - усиливает всасывание Са2+ в кровь | в кишечнике - тормозит всасывание Са2+ и фосфатов |
| в почках - усиливает реабсорбцию Са2+ и тормозит реабсорбцию фосфатных ионов | в почках - усиливает экскрецию Са2+ |
В щитовидной железе одновременно продуцируется тиреокальцитонин (антагонист паратгормона), который, напротив, способствует снижению кальциемии (гипокальциемический фактор). В норме паратгормон и тиреокальцитонин находятся в динамическом равновесии.
Наряду с регуляцией кальциевого метаболизма околощитовидные железы оказывают сильное влияние на обмен фосфора, снижая его концентрацию в крови.
Гипопаратиреоз. Заболевание развивается как следствие недостаточности функции околощитовидных желез. Уменьшение продукции паратгормона может обусловливаться удалением части околощитовидных желез, ослаблением их деятельности при инфекциях и интоксикациях.
Различают острую и хроническую паратиреоидную недостаточность.
Причиной возникновения острой паратиреоидной недостаточности (паратиреопривной тетании) чаще всего является случайное удаление околощитовидных желез при операциях на щитовидной железе или травматическое их повреждение. Уже в первые сутки развивается депрессивное состояние, возбудимость нервов и мышц возрастает, затем начинаются подергивания отдельных мышц головы и туловища, постепенно переходящие в тонические судороги.
Содержание кальция в крови во время тетанического припадка оказывается резко сниженным. При снижении концентрации кальция в крови нарушается равновесие между моновалентными и двухвалентными катионами (натрия и калия к кальцию и магнию), в результате чего и повышается нервно-мышечная возбудимость.
Содержание калия в крови больных гипопаратиреозом нередко повышено, содержание фосфора в крови во время приступа также значительно увеличивается. При тетании наблюдается сдвиг рН крови в кислую сторону. Удаление всех паращитовидных желез всегда заканчивается летальным исходом.
Хроническая форма околощитовидной недостаточности характеризуется подавлением аппетита, прогрессирующей кахексией и рядом трофических расстройств (гиперемия, кровоизлияния в области привратника желудка и двенадцатиперстной кишки с образованием язв, выпадение волос, в молодом возрасте - замедление роста).
Псевдогипопаратиреоз (болезнь Олбрайта). В отличие от истинного гипопаратиреоза, обусловленного первичной недостаточностью околощитовидных желез, является врожденным заболеванием. Характеризуется нанизмом (низким ростом), аномалиями в развитии скелета, дистрофическими изменениями зубов и костей и отставанием в интеллектуальном развитии. Наблюдаются снижение содержания кальция и повышение содержания фосфора в крови гипофосфатурия. В противоположность истинному гипопаратиреозу отмечается резистентность к паратгормону.
Гиперпаратиреоз (генерализованная фиброзная остеодистрофия, болезнь Реклингаузена). В 1876 году английский врач Педжет описал случай заболевания, проявившегося резкой деформацией костей. На секции кости оказались утолщенными и вместе с тем легкими, порозными и настолько мягкими, что их можно было резать ножом.
Гиперпаратиреоз - сложный и многообразный симптомокомплекс, клинические проявления которого обусловлены избыточной продукцией паратиреоидного гормона.
Патологические изменения при гиперпаратиреозе происходят, главным образом, в костях и почках. Костная ткань подвергается рассасыванию вследствие усиленной остеокластической реакции и деминерализации.
Нормальное пластинчатое костное вещество замещается свободной от извести молодой остеоидной тканью. Кости делаются мягкими, происходят разнообразные, иногда причудливые, деформации скелета.
Отмечаются резкие изменения в минеральном обмене. Паратиреоидный гормон понижает почечный порог в отношении фосфора, ослабляя его реабсорбцию в нефронах и усиливая экскрецию фосфатов с мочой.
При гиперпаратиреозе потеря фосфора приводит к мобилизации его неорганических соединений из костей. Поскольку эти соединения являются солями кальция, последний, освобождаясь из костей, в избытке поступает в кровь и развивается гиперкальциемия.
Кроме того, паратгормон стимулирует всасывание кальция из кишечника, функционально перекрываясь с витамином D, а также обратное всасывание кальция из клубочкового фильтрата.
Различают первичный и вторичный гиперпаратиреоз.
Первичный гиперпаратиреоз. Обусловлен развитием аденомы или гиперплазией околощитовидных желез.
Вторичный гиперпаратиреоз. Гиперплазия и гиперфункция околощитовидных желез развиваются в результате первичного изменения кальциево-фосфорного обмена (потери кальция и накопления фосфора в крови).
Вторичный гиперпаратиреоз имеет компенсаторный характер. Чаще всего он возникает при почечной остеодистрофии, когда нарушается экскреция фосфорнокислых солей в результате клубочковой недостаточности или же вследствие нарушения обмена ионов в дистальных канальцах.
Патофизиология нарушения гормональной регуляции артериального давления
Уровень артериального давления контролируется и поддерживается нейрогуморальными факторами при участии определенных вазомоторных центров, расположенных в продолговатом мозге.
В регуляции тонуса сосудов принимают участие и многие гормоны:
глюкокортикоидные гормоны коры надпочечников;
минералокортикоидные гормоны коры надпочечников (выработка и выделение альдостерона в норме стимулируются ионами калия и ангиотензином; минералокортикоиды увеличивают резорбцию натрия в дистальной части нефрона; если они присутствуют в избыточном или неконтролируемом количестве, повышение общего содержания натрия в организме ведет к увеличению объема жидкости, возрастанию объема крови и подъему артериального давления; кроме того, прямое воздействие минералокортикоидов на гладкие мышцы повышает сопротивление периферических сосудов);
катехоламины, вырабатываемые мозговым веществом надпочечников (оказывают разнообразное влияние на функцию сердечно-сосудистой системы и метаболизм, обеспечивая доставку крови и питательных веществ в условиях выраженного стресса);
ренин-ангиотензин;
вазопрессин.
Действие гормонов, вовлеченных в регуляцию артериального давления, наиболее отчетливо проявляется при их избытке или недостатке.
Избыточная продукция корой надпочечников гормона роста, глюкокортикоидных и особенно минералокортикоидных гормонов, катехоламинов, гипертиреоз, гиперпаратиреоз, повышенная продукция ренин-ангиотензина могут вызвать значительное повышение артериального давления.
Недостаточность надпочечников (болезнь Аддисона), гипотиреоз, автономная диабетическая нейропатия провоцируют возникновение гипотензии. При низком содержании кортизола в плазме нарушается реактивность гладких мышц сосудов, что вносит определенный вклад в развитие гипотензии. Механизм последнего при адреналовой недостаточности отчасти связан с уменьшением объема жидкости, обусловленным дефицитом альдостерона.
Артериальная гипертензия может быть проявлением гипертонической болезни (эссенциальная гипертензия, первичная артериальная гипертензия).
Термин «эссенциальная гипертензия» используется для описания состояния пациентов, у которых неизвестна причина повышения артериального давления. У большинства больных с гипертензией отсутствуют какие-либо симптомы, а данные лабораторных исследований остаются в пределах нормальных значений. При обследовании обычно выявляется высокое артериальное давление, а иногда и связанные с ним заболевания сердца, сосудов головного мозга, нарушение функции почек. У многих больных прослеживается отчетливая связь повышения артериального давления с генетическими факторами и образом жизни. Стресс, чрезмерное потреб ление алкоголя, ожирение и содержание в рационе большого количества соли коррелируют с развитием гипертензии.
Если эссенциальная гипертензия трудно контролируется или сочетается с гипокалиемией, необходимо исключить эндокринную причину ее возникновения.
Артериальная гипертензия - ведущий симптом многих эндокринных расстройств. Она развивается при поражении гипофиза (АКТГ-продуцирующая опухоль), адреналовых желез (феохромоцитома, первичный альдостеронизм).
Гипертензия адреналового происхождения (альдостероновая гипертензия) вызывается минералокортикоидными гормонами за счет увеличения объема плазмы либо внеклеточной жидкости.
Симптомы, связанные с артериальной гипертензией, могут отмечаться при первичном альдостеронизме (синдроме Конна) (см. выше).
Артериальная гипертензия, связанная с повышением уровня норадреналина, является ведущим физиологическим механизмом нарушений при феохромоцитоме - опухоли хромаффинной ткани, локализующейся в мозговом веществе надпочечников. Катехоламины (адреналин, норадреналин) оказывают выраженное и многостороннее действие на сердечно-сосудистую систему (увеличивают сердечный выброс, почечный кровоток, повышают систолическое артериальное давление, периферическое венозное давление).
Продукция катехоламинов при феохромоцитоме повышена в десятки раз. Огромные количества адреналина, которые постоянно выбрасываются в кровоток, провоцируют пароксизмальные повышения артериального давления, приступы тахикардии и одышку. Гипертонические кризы могут привести к серьезным мозговым осложнениям.
Феохромоцитома характеризуется также увеличением продукции вазопрессина, соматостатина, субстанции Р, кортикотропинрилизинг-фактора, адренокортикотропина, вазоактивного интестинального пептида и ряда других активных пептидов.
Эндокринная система и стресс
Эндокринная система принимает активное участие в ответе организма на воздействия факторов среды и процессах адаптации его к изменяющимся внешним условиям.
Термин «стресс» (англ. stress - давление, напряжение) был введен в медицинскую практику канадским патологом Гансом Селье. В своей жизни каждый человек постоянно испытывает физические и эмоциональные стрессы. «Стресс, - писал Селье, - аромат и вкус жизни». Однако избыточный стресс - дистресс - может стать патогенетической основой психических заболеваний, эндокринных расстройств, гипертонической болезни, ишемической болезни сердца, язвенной болезни желудка. Стресс снижает иммунную противоопухолевую защиту организма.
В целом стресс можно определить как состояние организма человека и животных, всегда возникающее при действии на него различных экстремальных факторов (холод, гипоксия, физическая нагрузка и т.п.). Сами же раздражители называются стрессорами.
Стрессорами могут служить самые разнообразные внешние и внутренние факторы, воздействующие на организм: травмы, ожоги, инфекции, интоксикации, наркоз, кровопотеря, действие высоких и низких температур, электротравма, действие ионизирующей радиации, эмоциональные воздействия.
Системы противодействия организма чрезвычайным раздражителям обеспечивают сохранение гомеостаза. В ответ на стрессорное воздействие человек или животное либо избегает его, либо приспосабливается (адаптируется) к новым условиям среды. При первичном действии стрессора возникает стресс-реакция (так называемая срочная, аварийная адаптация). Она дает организму возможность осуществлять жизнедеятельность в новых условиях - в условиях действия стрессора.
Однако эта реакция несовершенна и не обеспечивает эффективного устойчивого приспособления к стрессорному воздействию. Устойчивая долговременная адаптация, характеризующаяся высокой резистентностью к стрессору, может сформироваться лишь в результате повторных воздействий данного стрессора, если интенсивность и длительность его влияния умеренны. Если же они чрезмерны, то адаптация не развивается, а возникают повреждения, которые приводят к развитию болезни или гибели.
Общий адаптационный синдром (Селье) - это совокупность защитных реакций организма, возникающих в ответ на действие стрессорных агентов.
В настоящее время доказано участие в формировании стресс-реакции не только гормонов гипофиза и надпочечников, но и нейропептидов, опиоидных пептидов и многих других биологически активных веществ.
Все большее внимание врачей привлекает проблема стресса как патогенетической основы болезней.
Патогенетические механизмы стресса. Включение гипофизарно-надпочечниковой системы в ответ на стрессорные стимулы можно представить следующим образом. Стрессор воздействует на экстеро- и (или) интерорецепторы, возможно, и на различные анализаторы (не исключено также сочетанное действие стрессора на эти образования). Через систему моноаминоергических нейронов головного мозга активируются нейросекреторые клетки гипоталамуса, находящиеся под контролем пептидергических волокон. Усиливается секреция гипоталамического кортикотропинлиберирующего фактора (КРФ), являющегося стимулятором для АКТГ-продуцирующих клеток гипофиза. В свою очередь, АКТГ усиливает секрецию глюкокортикоидов корой надпочечников.
Роль пускового механизма активации гипофизарно-надпочечниковой системы играет возбуждение симпатической нервной системы и мозгового вещества надпочечников (катехоламины высвобождаются из мозговой ткани надпочечников под влиянием симпатических стимулов).
Стресс-лимитирующие системы и их роль в развитии стресса. Бурный ответ организма, направленный на ограничение действия стрессора и борьбу с теми неблагоприятными последствиями, которые он может вызвать, несет в себе потенциальную опасность. Она связана также с возможным истощением запасов адаптивных гормонов глюкокортикоидов и формированием в связи с этим острой надпочечниковой недостаточности.
Классической стресс-лимитирующей системой является опиоидергическая система организма (нейроны в гипоталамусе, пропиомеланокортин гипофиза, Р-эндорфин, энкефалины).
ГАМК-ергическая и серотонинергическая системы оказывают тормозящее влияние на реакции ЦНС при стрессе.
На уровне органов и тканей ограничение стресса связывают с деятельностью системы локальной регуляции адениннуклеотидов, простагландинов, антиоксидантов, сдерживающих разрушительные процессы в тканях.
NO-ергическая система (NO-нейроны стриатума, среднего мозга, гипоталамуса, гипофиза, чувствительные к оксиду азота) ограничивает активацию симпато-адреналовой системы и периферических звеньев, ответственных за развитие стресс-реакции.
Роль стресса в патогенезе некоторых заболеваний. В настоящее время в медицинской теории и практике используются термины «острый стресс» и «хронический стресс». Последний является одним из важнейших причинных факторов возникновения и развития многих болезней человека.
Психологический (эмоциональный) стресс, связанный с неразрешимостью жизненных ситуаций, может провоцировать возникновение не только психических болезней (в этом случае врачи говорят о большой вероятности преморбида - готовности к болезни), но и психосоматических заболеваний (ИБС, гипертоническая болезнь, язвенная болезнь желудка и двенадцатиперстной кишки). Описаны случаи аффективных эндокринных расстройств: нарушение функции щитовидной железы, нарушения лактации, течения беременности и климакса у женщин.
Роль стресса в патогенезе гипертонической болезни. Длительно действующие эмоциональные стрессоры имеют первостепенное значение в патогенезе гипертонической болезни в связи с нарушением саморегуляции АД. Можно выделить следующие факторы, ведущие к гипертензии и закрепляющие ее.
Сосудосуживающий эффект катехоламинов.
Закрепление симпатической активности при повторяемости ее стимуляции.
Развитие тенденции барорецепторов каротидного синуса и аорты к «перенастройке» на более высокий уровень артериального давления. В норме благодаря депрессорным влияниям с этих зон подъем артериального давления сдерживается. Но если они «перенастроены» на более высокий уровень, то для их включения в работу будут требоваться все более высокие величины АД. Следовательно, артериальное давление будет иметь тенденцию к повышению после очередных гипертензивных состояний.
Большие дозы глюкокортикоидов вызывают минералокор- тикоидный эффект задержки натрия, обусловливающей су- жение артериол как за счет набухания стенки, так и за счет потенцирования катехоламиновых влияний.
Активация ренин-ангиотензин-альдостероновой системы через симпатические влияния.
Под влиянием стрессора активируется симпато-адреналовая система, повышается тонус сосудов. Избыток глкжокортикоидов ведет к повышению тонуса сосудодвигательного центра и увеличению содержания натрия в крови, что повышает чувствительность рецепторов сосудов к катехоламинам. Все это способствует поддержанию АД на повышенном уровне и развитию гипертензии.
Роль стресса в патогенезе ишемической болезни сердца и инфаркта. Когда идет речь об этиологии ишемической болезни сердца, принято говорить о так называемых факторах риска этой болезни. Среди них важнейшими являются наследственные факторы, по всей вероятности, связанные с особенностями обмена холестерола, а также потребление пищи, богатой холестерином, адинамия, курение, иногда потребление алкоголя и, наконец, стрессовые ситуации.
Можно выделить несколько механизмов развития ИБС.
Длительная, частая стимуляция симпатической нервной системы ведет к поражению миокарда. В данном случае важную роль отводят повышению внутриклеточного содержания кальция. Кальциевые механизмы повреждения принято рассматривать в соответствии со следующими феноменами: активация фосфолипаз, увеличение активности ПОЛ, ослабление мощности саркоплазматического ретикулума (СПР) и контрактура миофибрилл, ухудшение работы митоходрий в силу их перегрузки кальцием. Все эти нарушения механизмов сократительной функции миокарда неизбежно ведут к нарушениям фаз сердечного цикла систолы и диастолы.
Адренергический компонент стресс-реакции может вызвать стойкий спазм гладкой мускулатуры коронарных артерий, ведущий к ишемическому повреждению миокарда.
Катехоламины, обладая способностью активировать процессы свертывания крови, могут вызвать развитие тромбоза коронарных артерий, потенцируя ишемическое повреждение миокарда.
Перераспределение крови во время стресса (ее централизация) может вызвать неадекватное кровоснабжение сердца, что способствует его ишемизации.
Снижению коронарного кровотока может способствовать возникающая во время стресса гипервентиляция легких, которая ведет к увеличению напряжения кислорода в крови с последующим развитием гипокапнического алкалоза, что, в свою очередь, повышает тонус коронарных артерий.
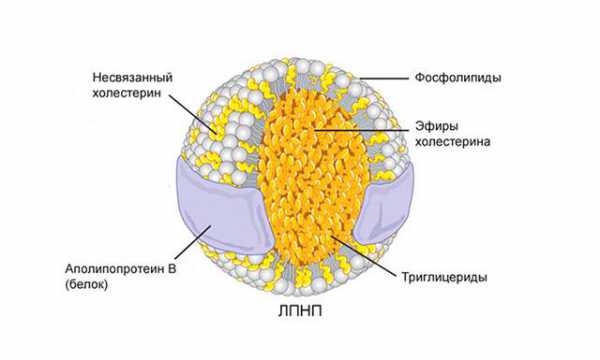
Ухудшению коронарного кровотока способствует характерная для стресса гиперлипидемия, вызываемая чрезмерным усилением адаптивного липотропного эффекта стресса. Стрессор, повышая активность симпатической нервной системы, усиливает мобилизацию жира из жировой ткани. Этому способствуют и гормональные сдвиги (повышение в крови уровней адреналина и норадреналина, АКТГ, СТГ, ТТГ). В крови повышается содержание НЭЖК, а затем - триглицеридов, ресинтезируемых в печени из НЭЖК. Увеличиваются продукция и содержание в крови |3-липопротеидов, в состав которых входит холестерин. Развивается атеросклероз коронарных артерий.
Роль стресса в патогенезе желудочно-кишечных заболева- ний. Стрессу и возникающим в ходе его развития нарушениям нейрогуморальной регуляции придается немаловажное значение в формировании патологии желудочно-кишечного тракта, прежде всего язвенной болезни желудка и двенадцатиперстной кишки и неспецифического язвенного колита.
При агрессии стрессовая реакция активирует симпато-адреналовую систему, тогда как при депрессии и аутизации (уход в себя) активируется система «передний гипофиз - кора надпочечников». Когда человек испытывает эмоции, связанные с гневом, яростью и т.п., возрастает содержание пепсина и соляной кислоты в желудке, при депрессии продукция их снижается. И то и другое ведет к дис- балансу секреторной функции желудка.
Хорошо известно, что язвы тела желудка редко сопровождаются повышенной кислотностью, но агрессивные свойства желудочного сока при них особенно ярко выражены. Эти нарушения связаны с активацией парасимпатической нервной системы. Повышение же симпатической активности влечет за собой расстройство кровоснабжения желудка в форме ишемизации и ишемического повреждения; нарушается процесс репарации слизистой желудка.
Фактором, связанным с нарушением функции вегетативной нервной системы при стрессе, можно считать и нарушение моторики желудка в форме заброса дуоденального содержимого в его пилорическую часть. На этом фоне избыточная продукция глюкокортикоидов рассматривается как фактор, способствующий развитию язвенного процесса. Глюкокортикоиды снижают местную продукцию простагландинов (что ведет к нарушению кровотока и уменьшению продукции слизи), уплотняют стенку микроциркуляторных сосудов, снижая активность процессов выделения и образования медиаторов, поддерживающих гистогематический барьер слизистой на должном уровне. Наконец, глюкокортикоиды тормозят репарацию клеток слизистой оболочки желудка, неизбежно подвергающихся как естественной гибели, так и процессам повреждения.
Роль стресса в патогенезе психических расстройств. Известно, что высокий уровень симпатической активности часто обусловливает тревожные реакции. Такая тревога может быть вызвана усиленной симпатической и проприоцептивной импульсацией в кору головного мозга. Проприоцептивные импульсы обнаруживаются в условиях высокого напряжения скелетной мускулатуры. С учетом всего этого становится понятным положительный эффект релаксации (снижения мышечного напряжения) при стрессе. Можно предположить, что чрезмерное нервное возбуждение через восходящую активирующую ретикулярную формацию приводит к возникновению неорганизованной и нефункциональной нервной импульсации, проявляющейся нарушением сна, беспричинной тревогой, а иногда и маниакальным поведением.
Депрессивные реакции рассматриваются как одно из психологических проявлений дистресса у больных. Нередко он предшествует депрессивной реакции. В трудных жизненных ситуациях у больного могут возникать мысли о том, что все предпринимаемые им усилия бесполезны, что он находится в безвыходном положении, следствием чего, как правило, и является депрессия. Доказано, что у больных во время депрессивных эпизодов повышена активность оси «передний гипофиз - кора надпочечников».
Предполагается, что стресс может иметь отношение к развитию или обострению некоторых форм шизофрении. Считается, что при этой патологии нарушен адаптивный механизм избегания при столкновении с провоцирующей тревогу ситуацией.
Совместимость Паратгормона и Кальцитонина
Паратгормон и кальцитонин вырабатываются паращитовидными железами и входят в состав некоторых лекарственных средств. В эндокринологии данные гормоны регулируют работу многих органов и систем.
Паратгормон и кальцитонин вырабатываются паращитовидными железами и входят в состав некоторых лекарственных средств.
Действие паратгормона
Паратгормон оказывает влияние на уровень кальция в крови, способствуя его повышению. Стимулирует активацию витамина D, который необходим для нормального функционирования костной системы. Гормон, поступающий в организм в нормальных количествах, улучшает состояние суставов.
Действие кальцитонина
Гормон оказывает влияние на уровень фосфора в крови, а также способен задерживать ионы кальция в костях, предотвращая их разрушение при воздействии ряда неблагоприятных факторов.
Оба гормона можно обнаружить в большинстве препаратов, предназначенных для лечения заболеваний щитовидной железы, а также в продуктах питания.
Препараты
Препараты, в которых содержатся указанные вещества:
- Паратиреоидин — применяют при недостаточной выработки паратгормона паращитовидными железами; способствует повышению кальция в крови и устранению судорог;
- Паратирин — регулирует уровень кальция и фосфора в крови; применяется при остеопорозе, связанном с гиперпаратиреозом;
- Сибакальцин — представляет собой синтетический кальцитонин; избавляет от боли и препятствует деструкции костной ткани;
- Кальцитрин — применяют при гиперкальциемии, остеопорозе и фантомных болях.
Продукты
Для регуляции уровня паратгормона следует употреблять в пищу:
- сельдерей;
- сельдь;
- льняное масло;
- крапиву;
- белокочанную капусту.
Для поддержания необходимой концентрации кальцитонина следует включить в рацион:
- морепродукты;
- морскую капусту;
- кисломолочные продукты;
- яйца;
- творог.
Показания для одновременного применения 2 гормонов:
- болезнь Педжета;
- остеопороз;
- медленное срастание костной ткани;
- остеомиелит;
- пародонтоз;
- профилактика переломов;
- болезнь Олбрайта;
- большое количество стрессов.
Совместный эффект паратгормона и кальцитонина
Нормальное содержание паратгормона и кальцитонина в крови способствует поддержанию здоровья костной и эндокринной систем.
Противопоказания
Противопоказания:
- повышенное артериальное давление;
- заболевания надпочечников;
- гиперчувствительность;
- беременность и кормление грудью;
- аллергия.
Как принимать паратгормон и кальцитонин
Для лучшего действия паратгормон в виде раствора вводится подкожно по 20 мг. Дозировку в каждом случае определяет врач. Количество препарата и курс лечения зависят от клинической картины и степени разрушения костной ткани. Кальцитонин также вводится подкожно, но в некоторых случаях и внутривенно.
Побочные действия
При лечении гормонами могут возникать аллергические реакции: зуд, жжение, отеки.
В начале терапии могут ощущаться приливы крови к лицу. Реже меняется уровень артериального давления.
В некоторых случаях отмечаются головные боли, тошнота, нарушения стула, неприятный привкус во рту.
В месте введения инъекции может возникать зуд, реже — болезненные ощущения.
Во время лечения может снижаться аппетит, появляться головокружение.
Не следует исключать возникновение анафилактических реакций, сопровождающихся отеком гортани и бронхоспазмом.
В редких случаях на фоне введения гормонов усиливаются боли в суставах, присутствует слабость и носовые кровотечения.
При несоблюдении пропорции повышается риск возникновения побочных реакций. Был зафиксирован случай летального исхода при введении кальцитонина, поэтому при гиперчувствительности лучше перестраховаться и начинать лечение с минимальной дозировки.
Ольга Владимировна (ортопед), 47 лет, Красноярск
Кальцитонин совместно с паратгормоном назначаю с осторожностью, так как повышается риск возникновения побочных эффектов. Препараты на основе данных гормонов помогают при тяжелой форме остеопороза.
Александр Алексеевич (эндокринолог), 51 год, Якутск
Гормоны паращитовидной и щитовидной желез могут вызвать негативные реакции со стороны организма, поэтому лечение должно осуществляться под контролем состояния больного. Подобное сочетание может привести к последствиям.
Отзывы пациентов
Геннадий, 38 лет, Свердловск
Кальцитонин и паратгормон назначили при нарушении работы паращитовидных желез. Хотя эти гормоны имеют противоположное друг другу действие (как объяснил мне врач), в некоторых случаях их совместный прием просто необходим для лечения. Во время терапии не наблюдалось каких-либо неприятных симптомов.
Светлана, 46 лет, Уфа
Гормоны паращитовидных желез пришлось принимать после сильного стресса, который и привел к сбою в эндокринной системе. Стала отмечать боли в костях, но к концу лечения состояние нормализовалось.
Как связаны паратгормон и кальцитонин
[содержание]
Гормоны в организме человека – это такие биологически активные вещества, которые продуцируются специальными железами. Уровень гормонов должен быть стабильный. Любые отклонения способны спровоцировать серьёзнейшие последствия, вплоть до летального исхода. Существуют такие гормоны-антагонисты, как паратгормон и кальцитонин. Они тесно взаимосвязаны, каждый из них влияет на содержание кальция в организме и его усвояемость. Но направлено влияние каждого из гормонов на разные механизмы.
Паратгормон
Паратгормон – это гормон человека, который вырабатывают паращитовидные (околощитовидные) железы. Продуцирование данного гормона увеличивается, если происходит снижение уровня ионизированного кальция в организме. Клетки паращитовидных желез имеют рецепторы, которые определяют понижение уровня кальция в крови. В соответствии с показателями происходит более активная выработка паратгормона или менее.
Паратгормон является полипептидным гормоном (состоит из аминокислот), повышающим уровень ионизированного кальция в крови за счёт трёх моментов. Он через кальцитриол (гормоноподобное вещество, образующееся из витамина D) стимулирует всасывание кальция из кишечника, в результате чего кальций из пищи попадает в кровь в большем количестве. При этом необходимо много витамина D.
Вторым моментом является всасывание кальция из первичной мочи в почечных канальцах, а третий момент – это усиление активности остеокластов (разрушители костных тканей). Остеокласты забирают кальций из костей, что повышает риск возникновения переломов.
Кальцитонин
Кальцитонин – это один из трёх главных гормонов щитовидной железы. В отличие от двух других гормонов кальцитонин не является йодозависимым. Щитовидная железа продуцирует гормон кальцитонин в довольно незначительных количествах. В крови его содержание обычно невысокое. В совсем маленьких количествах кальцитонин вырабатывается и в кишечнике. Кальцитонин принимает участие в регуляции обмена кальция, являясь антагонистом паратгормона. Но он имеет также и другое значение.
Кальцитонин является онкомаркером – веществом, по концентрации которого в крови человека определяется развитие медуллярного рака щитовидной железы. Медуллярный рак является очень агрессивной формой онкологии, которая нередко развивается как наследственная патология. Кальцитонин позволяет выявить формирование этого рака щитовидки даже на самых ранних стадиях.
Взаимосвязь гормонов
Паратгормон и кальцитонин регулируют содержание кальция в крови. Но помимо этих гормонов на его содержание влияют и другие факторы. Например, уровень витамина D имеет огромное значение.
Паратгормон и кальцитонин находятся в двойной обратной связи. Снижение уровня кальция в крови провоцирует повышенное выделение паратгормона для повышения кальция. Если же его уровень становится высоким, то рецепторы паращитовидных желез улавливают изменения и прекращают выработку гормона.
Кальцитонин, наоборот, снижает уровень кальция и стимулирует выработку новой костной ткани. Достаточное количество кальцитонина необходимо для повышения плотности костей.
Гормоны противоположны друг другу по действию, но зависимы друг от друга. К примеру, при формировании опухоли у пациента она может вырабатывать оба этих гормона.
Оценка статьи:
(голосов: 2, средняя оценка: 5,00 из 5) Loading...Гормональные регуляторы минерального гомеостаза (кальцитонин и паратгормон)
Уровень кальция в крови является критическим фактором функционирования многих тканей, включая мышечную сократимость, свертывание крови, головной мозг, сердце. Главным депо кальция в организме служит костная ткань. Он откладывается в белковом матриксе костей в виде кристаллов гидроксиапатитов, что придает им прочность. Кальций находится в плазме крови частично связанной с белками плазмы (неактивной) фракции, частично – в свободной (активной) фракции. Кальций плазмы крови находится в динамическом равновесии с кальцием кишечника, костей и почечных канальцев.
Количественные показатели свободной фракции кальция регулируются, главным образом, паратиреоидным гормоном и витамином Д. В значительно меньшей степени в этой регуляции участуюи также кальцитонин, глюкокортикоиды и эстрогены.
Характерные особенности кальцитонина и паратгормона
| Гормон | Влияние на обмен кальция | Показания к применению | |
| кровь | костная ткань | ||
| Кальцитонин (препарат кальцитрин) Побочные эффекты: аллергические реакции, тошнота, воспаление в зоне введения | ↓ Са++ | ↑ Са++ | Остеопороз (при длительной иммобилизации в старческом возрасте), при длительном при-менении кортикостероидов. |
| Паратгормон (препарат паратиреоидин) Побочные эффекты: головокружение, гиперкальциемия, гиперурекемия | ↑ Са++ | ↓ Са++ | Хронический гипопаратиреоз, спазмофилия. |
| Форма выпуска (состав), количество препарата в упаковке | Форма выпуска (состав), количество препарата в упаковке | Способ назначения, средние терапевтические дозы |
| Паратиреоидин Parathyreoidinum (Б) | Ампулы по 1 мл (20 ЕД) | По 1 мл ежедневно или через сутки под кожу (в мышцу) |
| Кальцитрин Calcitrin | Ампулы по 1 мл (1 мл – 50 МЕ) | Под кожу, в мышцу, в вену капельно (доза определяется заболеванием) |
Препараты инсулина и синтетические гипогликемические средства
Поджелудочная железа выполняет экзокринную и эндокринную функции.
Эндокринная функция (выполняет островки Лангерганса):
синтез инсулина
синтез глюкагона
синтез соматостатина и панкреатического полипептида
Главные функции инсулина:
Транспорт глюкозы в клетку.
Синтез гликогена из глюкозы в печени и мышцах (активирует фермент гликогенсинететазу).
Активирует аэробный гликолиз.
Сахарный диабет – это заболевание, при котором наблюдается абсолютный или относительный дефицит инсулина.
Абсолютный дефицит инсулина – ↓ секреция инсулина β-клетками поджелудочной железы→ ↓ количество инсулина в крови.
Относительный дефицит инсулина – толерантность периферических тканей к инсулину или неадекватная секреция инсулина в ответ на стимуляцию пищи.
Сахарный диабет I типа:
чаще в молодом возрасте (до 40 лет);
генетическая предрасположенность;
провоцирующие факторы – аутоиммунные заболевания, вирусные инфекции
Сахарный диабет II типа:
возраст старше 40 лет;
генетическая предрасположенность;
провоцирующие факторы – избыточная масса тела (главный фактор), гиподинамия, нерациональное питание
Симптомы сахарного диабета
Снижение массы тела ( при СД Iтипа).
Увеличение массы тела (при СД IIтипа).
Гипергликемия.
Глюкозурия (в норме глюкоза в моче отсутствует).
Полиурия (глюкоза является осмолярным веществом и выводит из организма воду).
Полидипсия (жажда в ответ на ↑ диуреза.
Полифагия (↑ аппетита).
Лечение сахарного диабета
При сахарном диабете Iтипа – препараты инсулина.
При сахарном диабете IIтипа – пероральные (негормональные) гипогликемические средства.
 Диагностическая лаборатория в Уфе
Диагностическая лаборатория в Уфе