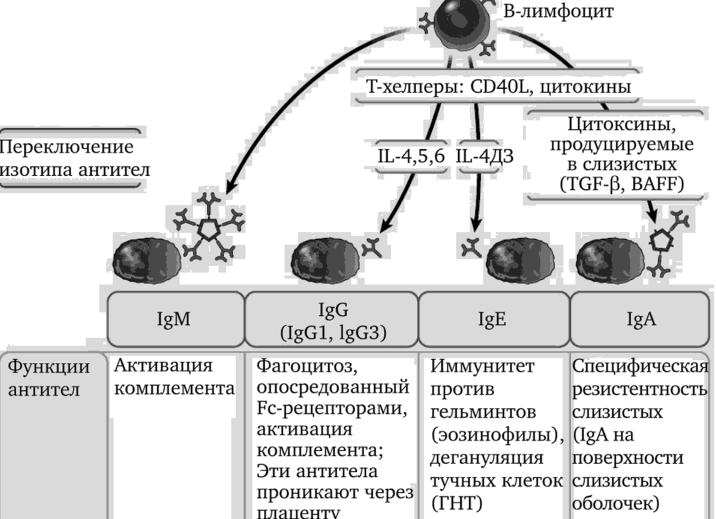
 [Антитела выполняют функции]
[Антитела выполняют функции]
Основные функции антител.
1. Опсонизация (иммунный фагоцитоз).
2. Антитоксический эффект.
3. Активация комплемента.
4. Нейтрализация.
5. Циркулирующие комплексы (связанные растворимые Аг образуют комплесы с Ат, которые выводятся из организма с желчью и мочой).
6. Антителозависимая цитотоксичность.
Динамика антителообразования.
Серологические реакции в лабораторной диагностике инфекционных заболеваний.
В защите организма от чужеродных антигенов решающую роль играют иммунологические механизмы, осуществляющиеся антителами и иммунокомпетентными клетками. Основа иммунологических механизмов – специфическая реакция между антителами или лимфоцитами (образовавшихся под воздействием попавшего в организм антигена) и антигена. Главная функция антител – связывание антигена и его дальнейшее выведение из организма.
Однако такие реакции между антителами и антигенами могут происходить и вне организма (in vitro) в присутствии электролита и возможны лишь при наличии комплементарности (структурного сходства, сродства) антигена и антитела.
Имея специфические антитела против определенного антигена можно распознать и выявить его среди других антигенов, а в сыворотке крови антитела против известного антигена.
Реакция антиген-антитело in vitro сопровождается возникновением определенного феномена – агглютинации, преципитации, лизиса.
Таким образом все серологические реакции используются с двумя целями:
-
выявление антител в сыворотке больного с помощью стандартных антигенов-диагностикумов (для серологической диагностики инфекционных болезней);
-
для выявления неизвестных антигенов по известным стандартным сывороткам, содержащим антитела определенной специфичности (для серологической идентификации возбудителей).
Например, если сыворотка больного реагирует с конкретным микробным антигеном – значит в сыворотке больного есть антитела против данного микроорганизма.
Серологическая диагностика – берут стандартный антиген (диагностикум), представляющий собой инактивированные или живые бактерии, вирусы или же их антигены (компоненты) в изотоническом растворе.
Серологическая идентификация – используют стандартные иммунные сыворотки, которые получают от иммунизированных животных (в крови животных в результате многократной иммунизации возбудителем появляется большое количество антител).
Агглютинация.
Агглютинация – серологическая реакция между антителами (агглютининами) и антигенами (агглютининогенами), размещенными на поверхности бактериальной клетки, а в результате образуется комплекс антиген-антитело (агглютинат).
Механизм агглютинации – под влиянием ионов электролита уменьшается негативный поверхностный заряд бактериальной клетки и следовательно они могут сблизиться на такое расстояние при котором возникает склеивание бактерий.
Макро- и микроскопический вид агглютината:
-
О-агглютинация (соматическая) – мелкозернистая, при микроскопии – бактерии склеиваются полюсами клеток, образуя сеть.
-
Vi-агглютинация (капсульная) – мелкозернистая, при микроскопии — склеивание бактерий происходит всей поверхностью клетки.
-
Н-агглютинация (жгутиковая) – агглютинины взаимодействуют с жгутиками обездвиживая бактерии, при микроскопии – крупнохлопчатая, склеивание бактериальных клеток в области жгутиков.
Реакция агглютинации используется для определения антител в сыворотке крови больных, например, при бруцеллезе (реакции Райта, Хеддельсона), брюшном тифе и паратифах (реакция Видаля) других инфекционных болезнях, а также при определении возбудителя, выделенного от больного. Эту же реакцию применяют для определения групп крови с использованием моноклональных антител против аллоантигенов эритроцитов.
Применяются различные варианты реакции агглютинации: развернутая, ориентировочная, непрямая и др.
Для определения у больного антител ставят развернутую реакцию агглютинации: к разведениям сыворотки крови больного добавляют взвесь убитых микробов (диагностикум) и через несколько часов инкубации при 37°С отмечают наибольше разведение (титр) сыворотки, при котором произошла агглютинация, т.е. образовался осадок.
Характер и скорость агглютинации зависят от вида антигена и антител.
Если необходимо определить возбудитель, выделенный от больного, ставят ориентировочную реакцию агглютинации, применяя диагностические антитела, т.е. проводят серотипирование возбудителя. Ориентировочную реакцию проводят на предметном стекле. К 1 капле диагностической иммунной сыворотки в разведении 1:10 или 1:20 добавляют чистую культуру возбудителя, выделенного от больного. Если появляется хлопьевидный осадок, то реакцию проводят в пробирках с увеличивающимися разведениями диагностической сыворотки, добавлял в каждую дозу сыворотки 2—З капли взвеси возбудителя. Реакцию считают положительной, если агглютинация отмечается в разведении, близком к титру диагностической сыворотки. В контролях (сыворотка, разведенная изотоническим раствором хлорида натрия, или взвесь микробов в том же растворе) осадок в виде хлопьев должен отсутствовать.
Разные родственные бактерии могут агглютинироваться одной и той же диагностической агглютинирующей сывороткой, что затрудняет их идентификацию. Поэтому пользуются адсорбированными агглютинирующими сыворотками, из которых удалены перекрестно реагирующие антитела путем адсорбции их родственными бактериями. В таких сыворотках сохраняются антитела, специфичные только к данной бактерии. Получение таким способом монорецепторных диагностических агглютинирующих сывороток было предложено А.Кастелляни (1902). Реакция непрямой (пассивной) гемагглютинации (РНГА) основана на использовании эритроцитов (или латекса) с адсорбированными на их поверхности антигенами или антителами, взаимодействие которых с соответствующими антителами или антигенами сыворотки крови больных вызывает склеивание и выпадение эритроцитов на дно пробирки или ячейки в виде фестончатого осадка. РНГА применяют для диагностики инфекционных болезней, определения гонадотропного гормона в моче при установлении беременности, для выявления повышенной чувствительности к лекарственным препаратам и гормонам и в некоторых других случаях. Реакция торможения гемагглютинации (РТГА) основана на блокаде, подавлении вирусов антителами иммунной сыворотки, в результате чего вирусы теряют свойство агглютинировать эритроциты. РТГА применяют для диагностики многих вирусных болезней, возбудители которых (вирусы гриппа, кори, краснухи, клещевого энцефалита и др.) могут агглютинировать эритроциты различных животных. Реакцию агглютинации для определения групп крови применяют для установления системы АВО с помощью РА эритроцитов, используя антитела к группам крови А(II), В(III). Контролем служит сыворотка, не содержащая антител, т.е. АВ(IV) группы крови, антигены, содержащиеся в эритроцитах групп А(II), В(III); отрицательный контроль не содержит антигенов, т.е. используют эритроциты группы 0 (I). В реакции агглютинации для определения резус-фактора используют антирезусные сыворотки (не менее двух различных серий). При наличии на мембране исследуемых эритроцитов резус-антигена происходит агглютинация этих клеток. Контролем служат стандартные резус-положительные и резус-отрицательные эритроциты всех групп крови.
Реакцию агглютинации для определения антирезусных антител (непрямую реакцию Кумбса) применяют у больных при внутрисосудистом гемолизе. У некоторых таких больных обнаруживают антирезусные антитела, которые являются неполными. Они специфически взаимодействуют с резус-положительными эритроцитами, но не вызывают их агглютинации. Наличие таких неполных антител определяют в непрямой реакции Кумбса. Для этого в систему антирезусные антитела + резус-положительные эритроциты добавляют антиглобулиновую сыворотку (антитела против иммуноглобулинов человека), что вызывает агглютинацию эритроцитов. С помощью реакции Кумбса диагностируют: патологические состояния, связанные с внутрисосудистым лизисом эритроцитов иммунного генеза, например гемолитическую болезнь новорожденных: эритроциты резус-положительного плода соединяются с циркулирующими в крови неполными антителами к резус-фактору, которые перешли через плаценту от резус-отрицательной матери.
Реакция коагглютинации — разновидность РА: клетки возбудителя определяют с помощью стафилококков, предварительно обработанных иммунной диагностической сывороткой. Стафилококки, содержащие белокА, имеющий сродство к иммуноглобулинам, неспецифически адсорбируют антимикробные антитела, которые затем взаимодействуют активными центрами с соответствующими микробами, выделенными от больных. В результате коагглютинации образуются хлопья, состоящие из стафилококков, антител диагностической сыворотки и определяемого микроба.
Схема постановки реакции агглютинации.
|
Компоненты |
Пробирки |
||||||
|
1 |
2 |
3 |
4 |
5 |
6 КС |
7 КД |
|
|
Изотонический раствор NaCl (физиологический раствор) |
0,5 |
— |
|||||
|
Сыворотка больного в разведении 1:5 (стартовое разведение) |
|||||||
|
Разведение |
1:10 |
1:20 |
1:40 |
1:80 |
1:160 |
1:100 |
|
|
Диагностикум, капли |
КС – контроль сыворотки; КД – контроль диагностикума
Титр сыворотки — наибольше разведение сыворотки, при котором произошло образование агглютината, т.е. образовался осадок. Фактически – это разведение сыворотки в последней пробирке, где произошло образование агглютината.
17. Антитела (иммуноглобулины), структура, классы, функции. Понятие о моноклональных антителах. Гибридомы, получение, применение.
Антитела (иммуноглобулины, ИГ, Ig) — особый класс гликопротеинов, присутствующих на поверхности B-лимфоцитов в виде мембраносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворимых молекул, и обладающих способностью очень избирательно связываться с конкретными видами молекул, которые в связи с этим называютантигенами. Антитела являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов. Антитела выполняют две функции: антиген-связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
Антитела синтезируются плазматическими клетками, которыми становятся некоторые В-лимфоциты, в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.
Антитела представляют собой белки глобулиновой природы (иммуноглобулины) образующиеся в организме под воздействием антигена и обладающие способностью избирательно связываться с ним. Существуют пять разновидностей молекул (классов) иммуноглобулинов с молекулярной массой от 150 до 900 тыс. дальтон: IgM, lgG, IgA, IgE, IgD. Молекулы иммуноглобулинов состоят из двух легких (L) и двух тяжелых (Н) полипептидных цепей, соединенных между собой дисульфидными связями . Оба типа цепей, соединенных между собой, обладают антигенностью. У тяжелых цепей она специфична для каждого класса иммуноглобулинов и соответственно классам Н-цепи обозначаются m , g , a , e , s . Легкие цепи в антигенном отношении делятся на две разновидности — X и l , одинаковые для, разных классов. Антигенные различия тяжелых цепей используют для получения антисывороток, позволяющих выявить наличие в исследуемом материале иммуноглобулинов того или иного класса. Легкие цепи IgG состоят из двух участков (доменов): вариабельных (VL) и константных (CL). Тяжелые цепи включают в себя один вариабельный ( V Н) и 3 константных участка (CH 1 , CH 2 , СН 3 ). Вариабельные участки легких и тяжелых цепей формируют активные центры антител (VL -VH). Участок CL — CH 1 определяет небольшие различия в последовательности расположения аминокислот у индивидуумов одного и того же вида (аллоантигенные различия молекул IgM). Область CH 2 -CH 2 участвует в фиксации и активации комплемента, а область СН 3 -СН 3 — в фиксации антитела к клеткам (лимфоцитам, макрофагам, тучным клеткам). Данный тип строения молекулы характерен и для всех остальных классов иммуноглобулинов, различия заключаются в дополнительной организации этой основной единицы. Так, Н-цепь IgM состоит не из 4, а из 5 доменов, а вся молекула IgM представляет собой пентамер молекулы IgG, соединенный дополнительными полипептидными J-цепями. IgA может быть в форме мономеров, димеров и секреторного IgA. Последние две формы имеют дополнительные (димеры) J или J и S цепи (секреторный). Другие свойства антител представлены в таблице 5.
Таблица 5.
Основные характеристики иммуноглобулинов человека
|
© п/п |
Показатели |
IgM |
IgG |
IgA |
IgE |
IgD |
|
1. |
Молекулярная масса |
900т. |
150т. |
170т. и 300т. |
190т. |
180т. |
|
2. |
Уровень в крови в г/л |
0,5 — 1,8 |
6 -16 |
1 — 5 |
0,00002 |
0,03 — 0,04 |
|
3. |
Тип тяжелых цепей |
m 1 — m 2 |
g 1 — g 4 |
a 1 — a 2 |
e |
s |
|
4. |
Формула |
5 H5L |
2h3L |
4h5L |
||
|
5. |
Фиксация С |
++++ |
++ |
+ S |
||
|
6. |
Нейтрализация токсинов |
+ |
||||
|
7. |
Агглютинация |
|||||
|
8. |
Бактериолиз |
? |
||||
|
9. |
Прохождение плаценты |
Молекула антитела связывается с детерминантой антигена не целиком, а лишь определенной своей частью, называемой активным центром. Активный центр представляет собой полость или щель, соответствующую пространственной конфигурации детерминантной группы антигена. Один из активных центров по разным причинам может быть функционально инертным. Такие антитела называются неполными. Их появлению обычно предшествует образование полных, т. е. антител с двумя (IgG) активными центрами. Неполные антитела встречаются у разных классов иммуноглобулинов. Основная масса антител образуется в клетках плазмоцитарного ряда (плазмобласт, проплазмоцит, плазмоцит). Каждая из них продуцирует антитела только одной специфичности, т. е. к одной антигенной детерминанте. Территориально эти клетки располагаются в селезенке, лимфоузлах, костном мозге, лимфоидных образованиях слизистых оболочек. При первичном контакте организма с антигеном и антителообразовании различают индуктивную и продуктивные фазы. Продолжительность первой фазы составляет около 2 суток. В этот период происходит пролиферация и дифференцировка лимфоидных клеток, развитие плазмобластической реакции. Вслед за индуктивной наступает продуктивная фаза. В сыворотке крови антитела начинают определяться с З-го дня после контакта с антигеном. Эти антитела относятся к классу IgM. С 5-7 дня происходит постепенная смена синтеза IgM на синтез IgG той же специфичности. Обычно к 12-15 дню кривая антителообразования достигает максимума, далее уровень антител начинает снижаться, но определенное их количество можно обнаружить и через много месяцев, а иногда и лет. При повторном контакте организма с тем же антигеном индуктивная фаза занимает лишь несколько часов. Продуктивная фаза протекает быстрее и интенсивнее, осуществляется синтез преимущественно IgG.
Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типараспознает и связывает антиген, а затем усиливает киллинг и/или удаление иммунных комплексов, сформированных в результате активации эффекторных механизмов.
Одна область молекулы антител (Fab) определяет её антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C1q) системы комплемента для инициации классического пути каскада комплемента.
-
IgG является основным иммуноглобулином сыворотки здорового человека (составляет 70-75 % всей фракции иммуноглобулинов), наиболее активен во вторичном иммунном ответеи антитоксическом иммунитете. Благодаря малым размерам (коэффициент седиментации 7S, молекулярная масса 146 кДа) является единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивающей иммунитет плода и новорожденного. В составе IgG 2-3 % углеводов; два антигенсвязывающих Fab-фрагмента и один FC-фрагмент. Fab-фрагмент (50-52 кДа) состоит из целой L-цепи и N-концевой половины H-цепи, соединённых между собой дисульфидной связью, тогда как FC-фрагмент (48 кДа) образован C-концевыми половинами H-цепей. Всего в молекуле IgG 12 доменов (участки, сформированные из β-структуры и α-спиралей полипептидных цепей Ig в виде неупорядоченных образований, связанных между собой дисульфидными мостиками аминокислотных остатков внутри каждой цепи): по 4 на тяжёлых и по 2 на лёгких цепях.
-
IgM представляют собой пентамер основной четырёхцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J-цепью (20 кДа), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Появляются при первичном иммунном ответе B-лимфоцитами на неизвестный антиген, составляют до 10 % фракции иммуноглобулинов. Являются наиболее крупными иммуноглобулинами (970 кДа). Содержат 10-12 % углеводов. Образование IgM происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μ-цепями, в результате образуются функционально активные IgM, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген распознающего рецептора; с этого момента клетки пре-B-лимфоцитов становятся зрелыми и способны участвовать в иммунном ответе.
-
IgA сывороточный IgA составляет 15-20 % всей фракции иммуноглобулинов, при этом 80 % молекул IgA представлено в мономерной форме у человека. Основной функцией IgA является защита слизистых оболочек дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекций. Секреторный IgA представлен в димерной форме в комплексесекреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Содержит 10-12 % углеводов, молекулярная масса 500 кДа.
-
IgD составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, ещё не представлявшихся антигену. Молекулярная масса 175 кДа.
-
IgE в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многиеаллергические реакции. Механизм действия IgE проявляется через связывание с высоким сродством (10−10М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления), на чем основано применение аллергических диагностических проб. Молекулярная масса 200 кДа.
Классификация по антигенам
-
антиинфекционные или антипаразитарные антитела, вызывающие непосредственную гибель или нарушение жизнедеятельности возбудителя инфекции либо паразита
-
антитоксические антитела, не вызывающие гибели самого возбудителя или паразита, но обезвреживающие вырабатываемые им токсины.
-
так называемые «антитела-свидетели заболевания», наличие которых в организме сигнализирует о знакомстве иммунной системы с данным возбудителем в прошлом или о текущем инфицировании этим возбудителем, но которые не играют существенной роли в борьбе организма с возбудителем (не обезвреживают ни самого возбудителя, ни его токсины, а связываются со второстепенными белками возбудителя).
-
аутоагрессивные антитела, или аутологичные антитела, аутоантитела — антитела, вызывающие разрушение или повреждение нормальных, здоровых тканей самого организмахозяина и запускающие механизм развития аутоиммунных заболеваний.
-
аллореактивные антитела, или гомологичные антитела, аллоантитела — антитела против антигенов тканей или клеток других организмов того же биологического вида. Аллоантитела играют важную роль в процессах отторжения аллотрансплантантов, например, при пересадке почки, печени, костного мозга, и в реакциях на переливание несовместимой крови.
-
гетерологичные антитела, или изоантитела — антитела против антигенов тканей или клеток организмов других биологических видов. Изоантитела являются причиной невозможности осуществления ксенотрансплантации даже между эволюционно близкими видами (например, невозможна пересадка печени шимпанзе человеку) или видами, имеющими близкие иммунологические и антигенные характеристики (невозможна пересадка органов свиньи человеку).
-
антиидиотипические антитела — антитела против антител, вырабатываемых самим же организмом. Причём это антитела не «вообще» против молекулы данного антитела, а именно против рабочего, «распознающего» участка антитела, так называемого идиотипа. Антиидиотипические антитела играют важную роль в связывании и обезвреживании избытка антител, в иммунной регуляции выработки антител. Кроме того, антиидиотипическое «антитело против антитела» зеркально повторяет пространственную конфигурацию исходного антигена, против которого было выработано исходное антитело. И тем самым антиидиотипическое антитело служит для организма фактором иммунологической памяти, аналогом исходного антигена, который остаётся в организме и после уничтожения исходных антигенов. В свою очередь, против антиидиотипических антител могут вырабатыватьсяанти-антиидиотипические антитела и т. д.
-
Моноклональные антитела — антитела, вырабатываемые иммунными клетками, принадлежащими к одному клеточному клону, то есть произошедшими из одной плазматической клетки-предшественницы. Моноклональные антитела могут быть выработаны против почти любого природного антигена (в основном белки и полисахариды), который антитело будет специфически связывать. Они могут быть далее использованы для детекции (обнаружения) этого вещества или его очистки.
-
Гибридома — гибридная клетка, искусственно полученная на основе слияния продуцирующей антитела В-лимфоцита с раковой клеткой, придающей этой гибридной клетке способность неограниченного размножения при культивировании in vitro, которая осуществляет синтез специфических иммуноглобулинов одного изотипа — моноклональных антител.Гибридомы, продуцирующие моноклональные антитела, размножают или в аппаратах, приспособленных для выращивания культур клеток или же вводя их внутрибрюшинно особой линии (асцитным) мышам. В последнем случае моноклональные антитела накапливаются в асцитной жидкости, в которой размножаются гибридомы. Полученные как тем, так и другим способом моноклональные антитела подвергают очистке, стандартизации и используют для создания на их основе диагностических препаратов. Гибридомные моноклональные антитела нашли широкое применение при создании диагностических и лечебных иммунобиологических препаратов.
Антитела
Антитела (иммуноглобулины, ИГ, Ig) — это особый класс гликопротеинов, присутствующих на поверхности В-клеток в виде мембраносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворимых молекул. Они являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов. Антитела выполняют две функции: антиген-связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
Антитела синтезируются плазматическими клетками, которыми становятся В-лимфоциты в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.
Антитела состоят из двух лёгких цепей и двух тяжелых цепей. У млекопитающих выделяют пять классов антител (иммуноглобулинов) — IgG, IgA, IgM, IgD, IgE, различающихся между собой по строению и аминокислотному составу тяжёлых цепей и по выполняемым эффекторным функциям.
История изучения
Самое первое антитело было обнаружено Берингом и Китазато в 1890 году, однако в это время о природе обнаруженного столбнячного антитоксина, кроме его специфичности и его присутствия в сыворотке иммунного животного, ничего определенного сказать было нельзя. Только с 1937 года — исследований Тизелиуса и Кабата, начинается изучение молекулярной природы антител. Авторы использовали метод электрофореза белков и продемонстрировали увеличение гамма-глобулиновой фракции сыворотки крови иммунизированных животных. Адсорбция сыворотки антигеном, который был взят для иммунизации, снижала количество белка в данной фракции до уровня интактных животных.
Строение антител
Общий план строения иммуноглобулинов: 1) Fab; 2) Fc; 3) тяжелая цепь; 4) легкая цепь; 5) антиген-связывающийся участок; 6) шарнирный участок
Антитела являются относительно крупными (~150 кДа — IgG) гликопротеинами, имеющими сложное строение. Состоят из двух идентичныхтяжелых цепей (H-цепи, в свою очередь состоящие из VH, Ch2, шарнира, Ch3 и Ch4 доменов) и из двух идентичных лёгких цепей (L-цепей, состоящих из VL и CL доменов). К тяжелым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина антитела можно расщепить на два Fab (англ. fragment antigen binding — антиген-связывающий фрагмент) и один Fc (англ. fragment crystallizable — фрагмент, способный к кристаллизации). В зависимости от класса и исполняемых функций антитела могут существовать как в мономерной форме (IgG, IgD, IgE, сывороточный IgA) так и в олигомерной форме (димер-секреторный IgA, пентамер — IgM). Всего различают пять типов тяжелых цепей (α-, γ-, δ-, ε-и μ- цепи) и два типа легких цепей (κ-цепь и λ-цепь).
Классификация по тяжелым цепям
Различают пять классов (изотипов) иммуноглобулинов, различающихся:
-
величиной
-
зарядом
-
последовательностью аминокислот
-
содержанием углеводов
Класс IgG классифицируют на четыре подкласса (IgG1, IgG2, IgG3, IgG4), класс IgA — на два подкласса (IgA1, IgA2). Все классы и подклассы составляют девять изотипов, которые присутствуют в норме у всех индивидов. Каждый изотип определяется последовательностью аминокислот константной области тяжелой цепи.
Функции антител
Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типа
-
распознает и связывает антиген, а затем
-
усиливает киллинг и/или удаление иммунных комплексов, сформированных в результате активации эффекторных механизмов.
Одна область молекулы антител (Fab) определяет ее антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C1q) системы комплемента для инициации классического пути каскада комплемента.
-
IgM представляют собой пентамер основной четырехцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J-цепью (20 кДа), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Появляются при первичном иммунном ответе B-лимфоцитами на неизвестный антиген, составляют до 10 % фракции иммуноглобулинов. Являются наиболее крупными иммуноглобулинами (970 кДа). Содержат 10-12 % углеводов. Образование IgM происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μ-цепями, в результате образуются функционально активные IgM, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген распознающего рецептора; с этого момента клетки пре-B-лимфоцитов становятся зрелыми и способны участвовать в иммунном ответе.
-
IgA сывороточный IgA составляет 15-20 % всей фракции иммуноглобулинов, при этом 80 % молекул IgA представлено в мономерной форме у человека. Секреторный IgA представлен в димерной форме в комплексе секреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Содержит 10-12 % углеводов, молекулярная масса 500 кДа.
-
IgD составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, еще не представлявшихся антигену. Молекулярная масса 175 кДа.
-
IgE в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многиеаллергические реакции. Механизм действия IgE проявляется через связывание с высоким сродством (10−10М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления). 200 кДа.
-
антиидиотипические антитела — антитела против антител, вырабатываемых самим же организмом. Причём это антитела не «вообще» против молекулы данного антитела, а именно против рабочего, «распознающего» участка антитела, так называемого идиотипа. Антиидиотипические антитела играют важную роль в связывании и обезвреживании избытка антител, в иммунной регуляции выработки антител. Кроме того, антиидиотипическое «антитело против антитела» зеркально повторяет пространственную конфигурацию исходного антигена, против которого было выработано исходное антитело. И тем самым антиидиотипическое антитело служит для организма фактором иммунологической памяти, аналогом исходного антигена, который остаётся в организме и после уничтожения исходных антигенов. В свою очередь, против антиидиотипических антител могут вырабатываться анти-антиидиотипические антитела и т. д.
Специфичность антител
Клонально-селекционная теория имеет в виду то, что каждый лимфоцит синтезирует антитела только одной определенной специфичности. И эти антитела располагаются на поверхности этого лимфоцита в качестве рецепторов.
Как показывают опыты, все поверхностные иммуноглобулины клетки имеют одинаковый идиотип: когда растворимый антиген, похожий на полимеризованный флагеллин, связывается со специфической клеткой, то все иммуноглобулины клеточной поверхности связываются с данным антигеном и они имеют одинаковую специфичность то есть одинаковый идиотип.
Антиген связывается с рецепторами, затем избирательно активирует клетку с образованием большого количества антител. И так как клетка синтезирует антитела только одной специфичности, то эта специфичность должна совпадать со специфичностью начального поверхностного рецептора.
Специфичность взаимодействия антител с антигенами не абсолютна, они могут в разной степени перекрестно реагировать с другими антигенами. Антисыворотка, полученная к одному антигену, может реагировать с родственным антигеном, несущим одну или несколько одинаковых или похожих детерминант . Поэтому каждое антитело может реагировать не только с антигеном, который вызвал его образование, но и с другими, иногда совершенно неродственными молекулами. Специфичность антител определяется аминокислотной последовательностью их вариабельных областей.
Клонально-селекционная теория:
-
Антитела и лимфоциты с нужной специфичностью уже существуют в организме до первого контакта с антигеном.
-
Лимфоциты, которые участвуют в иммунном ответе, имеют антигенспецифические рецепторы на поверхности своей мембраны. У B-лимфоцитов рецепторы- молекулы той же специфичности, что и антитела, которые лимфоциты впоследствии продуцируют и секретируют.
-
Любой лимфоцит несет на своей поверхности рецепторы только одной специфичности.
-
Лимфоциты, имеющие антиген, проходят стадию пролиферации и формируют большой клон плазматических клеток . Плазматические клетки синтезируют антитела только той специфичности, на которую был запрограммирован лимфоцит-предшественник. Сигналами к пролиферации служат цитокины, которые выделяются другими клетками. Лимфоциты могут сами выделять цитокины.
Вариабельность антител
Антитела являются чрезвычайно вариабельными (в организме одного человека может существовать до 108 вариантов антител). Все разнообразие антител проистекает из вариабельности как тяжёлых цепей, так и лёгких цепей. У антител, вырабатываемых тем или иным организмом в ответ на те или иные антигены, выделяют:
-
Изотипическая вариабельность — проявляется в наличии классов антител (изотипов), различающихся по строению тяжёлых цепей и олигомерностью, вырабатываемых всеми организмами данного вида;
-
Аллотипическая вариабельность — проявляется на индивидуальном уровне в пределах данного вида в виде вариабельности аллелей иммуноглобулинов — является генетически детерминированным отличием данного организма от другого;
-
Идиотипическая вариабельность — проявляется в различии аминокислотного состава антиген-связывающего участка. Это касается вариабельных и гипервариабельных доменов тяжёлой и лёгкой цепей, непосредственно контактирующих с антигеном.
Контроль пролиферации
Наиболее эффективный контролирующий механизм заключается в том, что продукт реакции одновременно служит ее ингибитором. Этот тип отрицательной обратной связи имеет место при образовании антител. Действие антител нельзя объяснить просто нейтрализацией антигена, потому что целые молекулы IgG подавляют синтез антител намного эффективнее, чем F(ab’)2 -фрагменты. Предполагают, что блокада продуктивной фазы T-зависимого B-клеточного ответа возникает в результате образования перекрестных связей между антигеном, IgG и Fc — рецепторами на поверхности B-клеток. Инъекция IgM, усиливает иммунный ответ. Так как антитела именно этого изотипа появляются первыми после введения антигена, то на ранней стадии иммунного ответа им приписывается усиливающая роль.
Иммунология и биохимия
Антитела — это белки, которые синтезируются иммунной системой организма в ответ на проникновение чужого, антигенов. Их задача – опознать и специфически связать антиген. Антигены — это бактерии, грибы, паразиты, простейшие и вирусы. В иммунной системе антитела называют гуморальными факторами адаптивного или приобретенного иммунитета. По своим свойствам антитела относятся к глобулинам. Глобулины, имеющие свойства антител, называют иммуноглобулинами.
В организме человека антитела находятся в двух физических формах – растворимой (кровь, тканевая жидкость, секреты) и связанной с наружной мембраной В-лимфоцитов. На мембране В лимфоцитов антитела выполняют функцию В клеточного рецептора, потому их называют рецепторные иммуноглобулины.
Рецепторные иммуноглобулины дают возможность В клеткам
- обнаруживать и связывать антигены в попавшие в организм
- этот тип иммуноглобулинов обеспечивает связь внеклеточного пространства с внутриклеточными сигнальными путями, управляющими пролиферацией и дифференцировкой В клеток в секретирующие антитела плазматические клетки.
Растворимые антитела — продукт секреции плазматических клеток и выполняют следующие функции:
- нейтрализуют антиген,
- мобилизуют эффекторные клетки иммунной системы — клетки уничтожения чужого,
- связывают и активируют систему комплемента — систему белков врожденного иммунитета.
Иммуноглобулины — это бифункциональные белки. С одной стороны они взаимодействуют с небольшим количеством специализированные молекул — с Fc-рецепторами на клетках иммунной системы, белками комплемента и молекулами, инициирующими внутриклеточную сигнализацию. С другой стороны, они распознают бесконечное множество антигенных структур (детерминант).
Молекулы как рецепторных, так и растворимых иммуноглобулинов, имеют общую основную структуру, которая имеет форму Y (рис.1). Эту структуру молекулы антител образуют две идентичные тяжелые цепи и две идентичные легкие цепи. N-концы легких и тяжелых цепей образуют вариабельную (предельно разную) область антител, F(ab)2 фрагмент — красные структуры на рис.1. образуют антиген связывающий сайт. Эта часть молекулы уникальна и называется детерминанта идиотипа (идиотип — класс иммуноглобулинов). У каждого человека 103 вариантов N-конца тяжелых и легких цепей образуют 106-107 вариантов антиген связующих сайтов. Особенности строения этой области обеспечивает распознавание бесконечного множества антигенных детерминант образования иммунных комплексов антиген-антитело (АГ-АТ).
Остальная часть легких и тяжелых цепей образуют константную область, Fc — фрагмент (синие структуры на рис.1). Эта область антител взаимодействует с ограниченным числом специализированных молекул на клетках иммунной системы, только с теми, которые имеют рецептор к Fc -фрагменту соответствующего класса иммуноглобулинов, и мобилизует их на уничтожение и удаление антигена.
F(ab)2 область антител выполняет:
- обнаружение антигена,
- осаждение антигена,
- блокирование активных центров токсинов или патоген-ассоциированных молекул;
- блокирование взаимодействия между молекулами клеток хозяина и патоген-ассоциированными молекулами возбудителя.
Но F(ab)2 не может:
- обеспечить ассоциированные с клетками воспалительные и эффекторные функции,
- обеспечить воспалительные и эффекторные функции комплемента,
- вовлечь антигены на путь процессинга. Эту функцию, она называется эффекторной, выполняет Fc- фрагмент антител..
Различают всего два варианта строения легких цепей иммуноглобулинов: каппа (κ) и лямбда (λ). В состав молекулы иммуноглобулинов входят либо лямбда, либо каппа. Структура тяжелых цепей антител имеет пять вариантов: µ,γ,α, ε и δ. В соответствии со структурой тяжелой цепи различают 5 классов иммуноглобулинов: IgM, IgG, IgA, IgE и IgD.
Классы иммуноглобулинов и их функция
Молекула IgM является старейшим классом иммуноглобулинов. Это большая молекула, состоящий из пяти основных единиц вместе J-цепью. Основная роль IgM — внутрисосудистая нейтрализация организмов, особенно вирусов. Эта важная физиологическая роль определяется тем, что IgM содержит пять сайтов связывания комплемента, что приводит к мощной активации системы комплемента.Эта активация (опсонизация) обеспечивает удаление комплексов антиген-антитело путем фагоцитоза через рецепторы комплемента на фагоцитирующих клетках или комплементарный лизис патогенов. Однако, в отличие от молекулы IgG, IgM имеет относительно низкуюсвязь со специфическим антигеном. Во-вторых, из-за его размера он обычно не проникают в ткани.
Напротив, IgG представляет собой меньшую молекулу, которая легко проникает в ткани. IgG представлены четырьмя основными подклассами: IgG1 и IgG3 активирует комплемент и эффективно удаляют большинство белковых антигенов, включая удаление микроорганизмов фагоцитирующими клетками. Напротив, IgG2 и IgG4 реагируют в основном с углеводными антигенами и относительно слабые опсонины. IgG — единственная молекула, которая пересекает плаценту и обеспечивает специфическую иммунную защиту новорожденных (защитные антитела).
Основной иммуноглобулинов слизистой оболочки IgA, состоит из двух базовых единиц, соединенных J цепь. Добавление секреторной молекулы предотвращает переваривание IgA2 (sIgA) ферментами в слизистой и в кишечнике. Таким образом, IgA2 является основной молекулой IgA в секретах и весьма эффективен в нейтрализации антигенов,которые проникают через эти слизистые пути. IgA1, основная молекула IgA в сыворотке, однако, подвержена инактивации сывороточными протеазами и, следовательно, менее активна для защита. В настоящее время функция IgA1 неясна.
IgD синтезируется антиген-чувствительным B-клетками и участвует в активации этих клеток антигеном. IgE продуцируются плазматическими клетками, они связывается со специфическими IgE-рецепторами на большинстве клеток и базофилов. Эта молекула играет чрезвычайно важную роль в аллергических реакциях и изгнании кишечных паразитов, что достигается за счет увеличения сосудистой проницаемости и индуцирования факторов хемотаксиса после дегрануляции тучных клеток. Исключительная способность генерировать большое количество молекул антител, иммунная система распознает все патогены, включая прошлые, настоящие и будущие.
Антигенсвязывающие сайты мембранных иммуноглобулинов В-клеток (рецепторы В-клеток) распознают не весь антиген, а определенные участки молекулы антигена, эпитопы или антигенные детерминанты с помощью конкретного домена вариабельных участков тяжелых (VH) и легких (VL) цепей. В -клетка активируется и подвергается пролиферации и дифференцировке. Последующее потомство этой В-клетки будет производить тот же домен VH или VL. Последовательность событий выглядит следующим образом: изначально B-клетка производит внутриклеточный антиген специфический IgM, который связан с поверхностью клетки. В-клетка теперь реагирует с антигеном и подвергается воздействию данного антигена. В-клетка начинает продуцировать изотип или класс иммуноглобулинов и начинает делиться, и все потомство (клон) будет производить идентичные молекулы иммуноглобулина, специфически связывающиеся со своим антигеном. Эти В-клетки позже созревают либо в плазматические клетки, либо в В-клетки.долговременной памяти. Таким образом, антиген структура его поверхностных доменов (эпитопов) отбирает В-лимфоциты с комплементарными рецепторами, которые в конечном счете будут синтезировать антиген-специфические антитела, антитела к тому или иному патогену, белки которого индуцировали иммунный ответ. При первичной встрече с антигеном первыми синтезируются антиген-специфические IgM, через 7 -10 дней в сыворотке определяются антиген специфические IgG. При повторном инфицировании тотчас включаются В-клетки памяти и синтезируются антиген-специфические IgG.