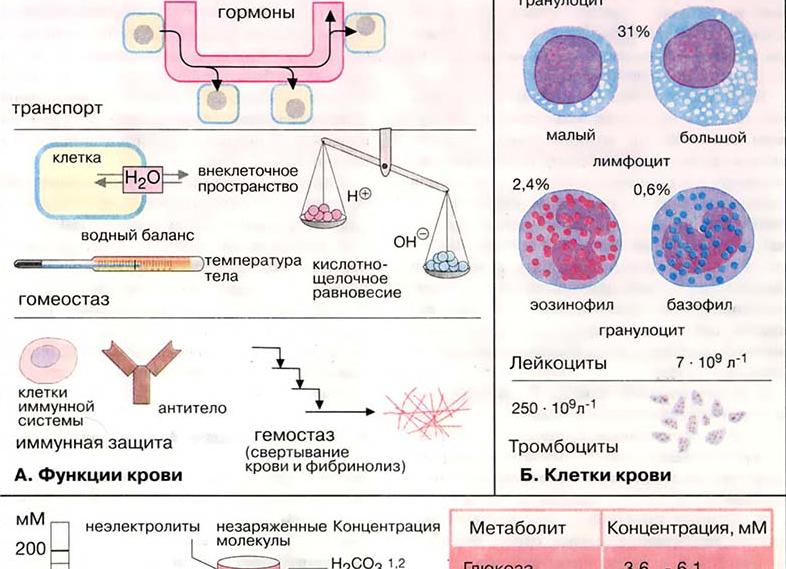
43. Электролитный состав плазмы крови. Осмотическое давление плазмы крови. Функциональная система, обеспечивающая постоянство осмотического давления крови.
-
Электролитами, т. е. анионами и катионами, являются неорганические вещества. Они выполняют ряд функций:
-
регулируют осмотическое давление;
-
поддерживают pH крови;
-
участвуют в возбуждении клеточной мембраны.
-
У каждого элемента имеются свои функции:
-
йод необходим для синтеза гормонов щитовидной железы;
-
железо входит в состав гемоглобина;
-
медь катализирует эритропоэз.
-
Осмотическое давление крови обеспечивается за счет концентрации в крови осмотически активных веществ, т. е. это разность давлений между электролитами и неэлектролитами.
-
Осмотическое давление относится к жестким константам, его величина 7,3–8,1 атм. Электролиты создают до 90–96 % всей величины осмотического давления, из них 60 % – хлорид натрия, так как электролиты имеют низкую молекулярную массу и создают высокую молекулярную концентрацию. Неэлектролиты составляют 4—10 % величины осмотического давления и обладают высокой молекулярной массой, поэтому создают низкую осмотическую концентрацию. К ним относятся глюкоза, липиды, белки плазмы крови. Осмотическое давление, создаваемое белками, называется онкотическим. С его помощью форменные элементы поддерживаются во взвешенном состоянии в кровеносном русле. Для поддержания нормальной жизнедеятельности необходимо, чтобы величина осмотического давления всегда была в пределах допустимой нормы.
-
Постоянство рН поддерживается:
-
буферными системами (сглаживают резкие колебания рН при внезапном увеличении содержания кислых либо щелочных продуктов в крови, н не выводят эти продукты из организма)
-
выделительными системами – легкими и почками (выводят кислые и щелочные продукты из организма)
-
Бикарбонатный буфер – это главный буфер плазмы; содержание его компонентов непосредственно регулируется системами выделения: почки выводят бикарбонат, легкие – углекислый газ, образующийся при распаде угольной кислоты.
-
Образован угольной кислотой и ее натриевой солью – бикарбонатом натрия.
-
При добавлении кислоты протоны связываются бикарбонатом и вместо сильной кислоты образуется слабая угольная кислота, и рН меняется мало.
-
При добавлении основания протоны высвобождаются угольной кислотой и нейтрализуют гидроксил, вместо основания образуется соль, и рН также меняется мало.
-
Фосфатный буфер – это важнейший буфер мочи, один из внутриклеточных буферов. В плазме его роль не велика.
-
Образован одно- и двузамещенными солями фосфорной кислоты.
-
При добавлении к фосфатному буферу кислоты протоны связываются с однозамещенной солью.
-
При добавлении основания протоны высвобождаются двузамещенной солью и нейтрализуют гидроксил.
-
Белковый буфер – главный внутриклеточный буфер.
-
Буферные свойства белков обусловлены наличием у аминокислот групп, способных обратимо связывать протоны.
-
Определенную буферную роль играют и белки плазмы крови.
-
Гемоглобиновый буфер – самый мощный буфер организма, единственный буфер эритроцитов.
-
Его буферная емкость зависит от того, в какой мере гемоглобин насыщен кислородом.
-
Буферные свойства гемоглобина обусловлены его белковой частью (глобином), в которой имеются группы, способные обратимо связывать протоны.
-
Задача выделительных систем:
-
Удалять кислые и щелочные вещества с такой же скоростью, с какой они поступают в кровь.
-
Подавляющая часть кислых веществ – СО2. Это летучее соединение, удаляется легкими.
-
Небольшое количество нелетучих кислот образуется в процессе метаболизма (продукты окисления серосодержащих и фосфорсодержащих аминокислот — серная и фосфорная кислоты, продукт распада нуклеиновых кислот — мочевая кислота, в определенных условиях — молочная кислота, кетоновые тела), часть их поступает из ЖКТ. Все нелетучие кислоты сначала реагируют в крови с бикарбонатом; затем удаляются почками, а концентрация бикарбоната в крови при этом восстанавливается.
-
Нарушения КЩР могут быть вызваны:
-
нарушениями метаболизма;
-
нарушениями функции ЖКТ или поступлением в ЖКТ больших количеств кислых или щелочных соединений;
-
нарушениями дыхания;
-
нарушениями функции почек.
Электролитный состав плазмы крови физиология — Все про гипертонию
- Описание исследования и показания
- Показатели белкового обмена
- Исследование ферментного состава крови
- Показатели липидного обмена
- Оценка обмена билирубина
- Электролитный состав крови
Тяжело себе представить современную медицину без лабораторных исследований. Биохимический анализ крови – один из самых востребованных и часто назначаемых врачами, методов. Комплекс показателей, входящих в его состав, самый широкий и дает информацию о функционировании любой из систем органов и организма в целом. Главное, уметь правильно оценить полученные результаты анализа.
Описание исследования и показания
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день…
Читать далее »
Биохимическое исследование крови предполагает определение концентрации различных продуктов каждого из видов метаболических процессов (обмена веществ) в человеческом организме. Для этого производится забор венозной крови из периферической вены (до 20 мл). Это обязательно должна быть кровь, взятая у исследуемого в утреннее время натощак. После забора ее отстаивают, центрифугируют, так как для непосредственного анализа нужна только ее жидкая прозрачная часть – плазма (сыворотка).
В исследуемой плазме определяются такие основные показатели:
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию. Подробнее здесь…
- Белковый обмен: общий белок и его фракции (альбумины и различные типы глобулинов), креатинин, остаточный азот, мочевина;
- Ферменты плазмы: аланинаминотрансфераза (АлАТ), аспартатаминотрансфераза (АсАТ), альфа-амилаза, щелочная фосфатаза;
- Пигментный обмен: билирубин общий и его фракции (прямой, непрямой);
- Липидный обмен: холестерин, липопротеиды высокой и низкой плотности, триглицериды;
- Электролиты крови: калий, натрий, хлор, кальций, магний.
Исследуемый комплекс биохимии в крови не обязательно должен включать в себя все возможные показатели. Целесообразность конкретных из них устанавливает врач в зависимости от патологии пациента. Это сократит стоимость исследования без снижения его информативности.
Показатели белкового обмена
Белковые молекулы в организме выполняют крайне важную роль, так как входят в состав любой клеточной мембраны, являются главным транспортировщиком питательных веществ и базовой основой иммуноглобулинов и антител в плазме крови. Расшифровка показателей белкового обмена приведена в таблице.
| Показатель белкового обмена | Норма | Патологические изменения |
| Общий белок | 70-90 г/л | Гипопротеинемия (состояние, при котором уровень белка ниже нормальных величин);
Гиперпротеинемия (состояние, при котором общий белок плазмы выше нормы); Диспротеинемия (нарушение нормального соотношения между альбуминами и глобулинами). |
| Альбумины | 56,5-66,5% | Гопоальбуминемия (полученный показатель альбумина ниже нормы);
Гиперальбуминемия (полученный показатель альбумина выше нормы). |
| Глобулины | 33,5-43,5% | Гопоглобулинемия или гиперглобулинемия (соответственно, снижение или повышение полученного показателя относительно нормального). Может быть представлена, как изменением общего уровня глобулинов, так и определенных их видов. |
| Креатинин | 50-115 мкмоль/л | Практический интерес представляет повышение уровня этих показателей в крови (гиперазотемия). |
| Мочевина | 4,2-8,3 ммоль/л |
Снижение уровня общего белка и альбумина. Обычно, характеризуются одними и теми же механизмами и причинами появления. Это могут быть:
- Плохое питание;
- Избыточное употребление жидкости или нарушение ее выведения из организма при почечной патологии;
- Ускоренный распад белка (опухоли, истощение, тяжелые травмы, болезни и операции, инфекции, воспалительно-деструктивные и аутоиммунные процессы);
- Нарушение синтеза белков печенью при ее заболеваниях. Гиипоальбуминемия относится к одному из критериев печеночной недостаточности при циррозе печени;
- Гипопротеинемия, обусловленная снижением функции щитовидной железы (гипотиреоз).
Анализ крайне редко определяет гиперпротеинемию и гиперальбуминемию, так как в большинстве случаев они носят относительный характер и обусловлены снижением количества жидкости в сосудистом пространстве при обезвоживании любого происхождения (недостаточное употребление жидкости или ускоренные потери с потом, испарением, поносом, рвотой).
Снижение и повышение уровня глобулинов
Большая часть глобулинов в крови человека представлена иммуноглобулинами. Повышение их абсолютного числа или относительного (по сравнению с альбуминами, которых должно быть больше половины общего уровня белка) является свидетельством активного иммунного процесса при любой инфекционно-воспалительной патологии. Если при этих заболеваниях регистрируется гипоглобулинемия, это говорит об иммунодефиците и неспособности организма противостоять патогенным микроорганизмам.
Повышение уровня креатинина, мочевины и остаточного азота
Такое возможно либо от ускоренного разрушения белка в организме при распаде тканей, либо от нарушения функции почек в отношении выведения токсических продуктов из организма при почечной недостаточности (гломерулонефрит, мочекаменная болезнь, интоксикации). В некоторых случаях повышение данных показателей крови закономерно возникает у пожилых людей и не свидетельствует о патологии. В этом отношении крайне важна степень повышения креатинина и мочевины. Чем больше они выражены, тем больше это говорит о почечном происхождении. Крайняя степень их повышения (в несколько раз) называется уремией.
Исследование ферментного состава крови
Ферменты в человеческом организме выполняют роль катализаторов, ускоряя течение обменных процессов. Каждый из них имеет определенную среду и орган, в которой он должен проявлять свою основную активность. Если имеет место поражение конкретного органа, происходит повышенный выход соответствующих ферментов в системный кровоток, что и определяется в ходе биохимического анализа.
| Показатель | Норма |
| АлАТ | 0,1-068 мкмоль/(ч*мл) |
| АсАТ | 0,1-0,45мкмоль/(ч*мл) |
| Альфа-амилаза | 12-32 мг/(ч*мл) |
| Щелочная фосфатаза | Нормативных величин очень много, что зависит от способа определения фермента. Норму указывает лаборатория. |
АлАТ (аланинаминотрансфераза)
Повышение уровня данного фермент является специфическим показателем разрушения печеночных клеток (печеночный цитолиз). Это возможно при токсических поражениях печени, гепатите, инфекционных заболеваниях, циррозе. По степени повышения АлАТ можно судить об активности и масштабах поражения печени.
АсАТ (аспартатаминотрансфераза)
Этот фермент больше всего проявляет свою активность в сердечной мышце и печени. Обнаружение его повышенного содержания в плазме крови говорит о патологии этих органов. Если возникает изолированное повышение АсАТ, это говорит об инфаркте миокарда. Синхронное повышение уровня фермента с АлАТ является свидетельством печеночного цитолиза при поражении этого органа.
Альфа-амилаза
Относится к специфическим показателям ферментативной активности поджелудочной железы. Практический интерес представляет, как повышение, так и снижение ее уровня при биохимическом анализе крови. В первом случае, это говорит о воспалительном процессе при остром и хроническом панкреатите, панкреонекрозе (разрушении ткани поджелудочной железы), нарушении оттока панкреатического сока при камнях желчных протоков или опухолевой трансформации органа. Снижение уровня альфа-амилазы характерно больных после тотального или субтотального панкреонекроза и операций по удалению всей или большей части поджелудочной железы.
Щелочная фосфатаза
Многие лаборатории автоматически включают этот фермент в биохимический анализ. С практической точки зрения может вызвать интерес исключительно повышение активности этого фермента в крови. Это является свидетельством либо внутрипеченочного застоя желчи в мелких желчных протоках, что бывает при механической и паренхиматозной желтухе, либо прогрессирующего остеопороза или разрушения костной ткани (миеломная болезнь, старение организма).
Показатели липидного обмена
На практике актуальными являются лишь некоторые из параметров обмена жиров. Они связаны с холестериновым обменом, что очень актуально для диагностики и определения динамики атеросклероза сосудов. Поскольку, это заболевание является фоном для развития ишемической болезни сердца, инфаркта, ишемического инсульта, облитерирующих заболеваний сосудов нижних конечностей и ветвей аорты, то мониторинг механизмов его развития крайне важен для медиков. Расшифровка основных показателей липидного обмена приведена в таблице.
| Показатель | Норма | Варианты отклонения от нормы |
| Холестерин | Менее 5,2 ммоль/л | Повышение показателя в крови говорит о нарушении липидного обмена, которое может быть следствием метаболического синдрома, ожирения, сахарного диабета и способно стать причиной прогрессирования атеросклероза сосудов. Снижение показателя холестерина также опасно и грозит нарушением синтеза стероидных и половых гормонов в организме. |
| Липопротеины низкой плотности | Менее 2,2 ммоль/л | Повышение данного показателя способствует распространению атеросклеротического поражения сосудов, так как ЛПНП транспортируют холестерин из печени в сосуды. |
| Липопротеины высокой плотности | 0,9-1,9 моль/л | Эти соединения ответственны за перенос холестерина из сосудов в печень и ткани. С практической точки зрения интересует снижение их уровня при анализе плазмы на биохимию. Если таковое выявляется, это говорит о возможности атеросклеротического процесса в сосудистых стенках. |
Оценка обмена билирубина
Главным показателем пигментного обмена в организме является билирубин. Его обмен очень сложный, что обуславливает наличие нескольких видов этого соединения. Он образуется в селезенке при распаде эритроцитов и попадает в печень через портальную систему вен. Здесь происходит его обезвреживание печеночными клетками путем связывания и глюкуроновой кислотой, что делает его нетоксичным для тканей организма. Это и лежит в основе определения билирубина и его разных видов при биохимическом исследовании. Та его часть, которая обезврежена после связывания, выделяется по желчным протокам и называется прямым билирубином. Оставшаяся часть, которая не успевает соединиться с глюкуроновой кислотой, попадаете в кровоток, и называется непрямым билирубином. Расшифровка показателей билирубинового обмена приведена в таблице.
| Показатель | Норма анализа | В каких случаях бывает повышен |
| Общий билирубин | 8-20,5 мкмоль/л | Во всех случаях повышения прямого и непрямого |
| Прямой | 0-5,1 мкмоль/л | Возникает при нарушении оттока желчи:
|
| Непрямой | До 16,5 мкмоль/л | Возникает при повышении продукции билирубина селезенкой или невозможности печени связать его:
|
Билирубин очень токсичный для тканей головного мозга. Повышение его уровня обязательно сочетается с желтушностью кожи, а в тяжелых случаях и нарушениями памяти и интеллекта.
Электролитный состав крови
Ни одна клетка организма не сможет существовать и функционировать без участия электролитов и ионов кальция, калия, магния, натрия и хлора. Получение результатов биохимического электролитного анализа крови может помочь определить состояние клеток и возможные угрозы, связанные с этим. Варианты нормы, их отклонения и расшифровка приведены в таблице.
| Показатель | Норма | Патология |
| Калий | 3,3-5,5 ммоль/л | Относятся к внутриклеточным ионам. Повышение их уровня (гиперкалиемия, гипермагниемия) является показателем почечной недостаточности или массивного распада мышечной ткани при травмах, глубоких ожогах, панкреонекрозе. Избыток опасен нарушениями сердечного ритма, остановкой сердца в диастоле. Снижение этих электролитов крови (гипокалиемия, гипомагниемия) наблюдаются при остром перитоните, кишечной непроходимости, инфекционных диареях и рвоте, обезвоживании организма, передозировке мочегонных средств. Опасности такие же, как и в случае с повышением их концентрации. |
| Магний | 0,7-1,2 ммоль/л | |
| Натрий | 135-152 ммоль/л | Являются внеклеточными ионами и ответственны за осмотическое давление в клетке и межклеточном пространстве. Снижение их уровня связано с обезвоживанием и нарушением водно-электролитного баланса на фоне любых тяжелых заболеваний. Опасность состояния в нарушении возбудимости нервных тканей и сердца, что может привести к его остановке в систолу. |
| Хлор | 95-110 ммоль/л | |
| Кальций | 2,2-2,75 ммоль/л | Является главным ионом, ответственным за мышечное сокращение, стабилизацию клеточных мембран и крепость костной ткани. Снижение его уровня бывает при рахите, гипотиреозе и недостаточном поступлении с продуктами питания. Это грозит возникновением мышечной слабости, аритмиями, остеопорозом. Повышение кальция характерно для гиперфункции паращитовидных желез и панкреонекроза. |
Видео о методике забора крови для биохимического анализа:
Биохимическое исследование крови – это прекрасный диагностический комплекс, дающий исчерпывающую информацию о функциональных возможностях организма и помогающий в решении лечебно-тактических вопросов.
Электролитный состав плазмы крови. Осмотическое давление.
Состав плазмы крови.
Плазма представляет собой жидкую часть крови желтоватого цвета, слегка опалесцирующую, в состав которой входят различные соли (электролиты), белки, липиды, углеводы, продукты обмена, гормоны, ферменты, витамины и растворенные в ней газы.
Электролитный состав плазмы важен для поддержания ее осмотического давления, кислотно-щелочного состояния, функций клеточных элементов крови и сосудистой стенки, активности ферментов, процессов свертывания крови и фибринолиза. Поскольку плазма крови постоянно обменивается электролитами с микросредой клеток, содержание в ней электролитов в значительной мере определяет и фундаментальные свойства клеточных элементов органов — возбудимость и сократимость, секреторную активность и проницаемость мембран, биоэнергетические процессы.
Содержание натрия и калия в плазме и эритроцитах отличается также, как и в других клетках и внеклеточной среде, и, соответственно, обусловлено различиями проницаемости мембран и работой К- Na- насосов клеток. Часть катионов плазмы связана с анионами органических кислот и белков, что играет роль в поддержании кислотно-щелочного состояния и необходимо для реализации функций белков.
Отличается в плазме и эритроцитах содержание и ряда анионов, прежде всего хлора и бикарбоната. Эти различия обусловлены обменом этих анионов между эритроцитами и плазмой в капиллярах легких и тканей при дыхании.
Содержание натрия и калия в плазме крови — жесткие гомеостатические константы, зависящие от баланса процессов поступления и выведения ионов, а также их перераспределения между клетками и внеклеточной средой. Регуляция гомеостазиса этих катионов осуществляется изменениями поведения (большее или меньшее потребление соли) и системами гуморальной регуляции, среди которых основное значение имеют ренин-ангиотензин-альдостероновая система и натриуретический гормон предсердий. Жесткой гомеостатической константой является и концентрация кальция в плазме крови. Кальций содержится в двух формах: связанной (с белками, в комплексных соединениях, малорастворимых солях) и свободной, ионизированной (Са++). Основные биологические эффекты кальция обусловлены его ионизированной формой. В цитозоле клеток ионизированного кальция содержится мало, но его количество чрезвычайно тонко регулируется, поскольку этот катион является важнейшим регулятором обменных процессов и функций клеток. Поступление кальция в клетки из внеклеточной среды связано с его уровнем в микросреде и плазме крови, хотя в большей степени зависит от специальных транспортных мембранных механизмов (каналов, насосов, переносчиков). В клеточном цитозоле ионизированный кальций связывается с белками, а также удаляется с помощью специальных Са-насосов во внутриклеточные депо (митохондрии, цитоплазматический ретикулум) и наружу в микросреду клеток. Содержащийся в плазме крови ионизированный кальций помимо того, что является источником для транспорта внутрь клеток, необходим для обеспечения физико-химических свойств плазменных белков, активности ферментов, например, для реализации механизмов свертывания крови. Регуляция уровня ионизированного кальция в плазме крови осуществляется специальной гуморальной системой, включающей ряд кальций-регулирующих гормонов: околощитовидных желез (паратирин), щитовидной железы (кальцитонин и его аналоги), почек (кальцитриол).
В плазме крови содержится и большое число различных микроэлементов. Как минимум 15 микроэлементов, содержащихся в плазме крови, например, медь, кобальт, марганец, цинк, хром, стронций и др., играют важную роль в процессах метаболизма клеток и обеспечении их функций, поскольку входят в состав ферментов, катализируют их действие, участвуют в процессах образования клеток крови и гемоглобина (гемопоэзе) и др.
Осмотическое давление крови. Осмотическим давлением называется сила, которая заставляет переходить растворитель (для крови это вода) через полупроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом с помощью определения депрессии (точки замерзания), которая для крови составляет 0,56—0,58°С.
Осмотическое давление крови зависит в основном от растворенных в ней низкомолекулярных соединений, главным образом солей. Около 60% этого давления создается NaCl. Осмотическое давление в крови, лимфе, тканевой жидкости, тканях приблизительно одинаково и отличается постоянством. Даже в случаях, когда в кровь поступает значительное количество воды или соли, осмотическое давление не претерпевает существенных изменений. При избыточном поступлении в кровь вода быстро выводится почками и переходит в ткани и клетки, что восстанавливает исходную величину осмотического давления. Если же в крови повышается концентрация солей, то в сосудистое русло переходит вода из тканевой жидкости, а почки начинают усиленно выводить соли. Продукты переваривания белков, жиров и углеводов, всасывающиеся в кровь и лимфу, а также низкомолекулярные продукты клеточного метаболизма могут изменять осмотическое давление в небольших пределах.
Open Library — открытая библиотека учебной информации
Безазотистые органические компоненты крови
В группу безазотистых органических веществ крови входят углеводы, жиры, липиды, органические кислоты и некоторые другие вещества. Все эти соединœения являются либо продуктами промежуточного обмена углеводов и жиров, либо играют роль питательных веществ. Основные данные, характеризующие содержание в крови различных безазотистых органических веществ, представлены в табл. 17.1. В клинике большое значение придают количественному определœению этих компонентов крови.
Известно, что общее содержание воды в организме человека составляет 60–65% от массы тела, ᴛ.ᴇ. приблизительно 40–45 л (если масса тела 70 кг); 2/3 общего количества воды приходится на внутриклеточную жидкость, 1/3 – нa внеклеточную. Часть внеклеточной воды находится в сосудистом русле (5% от массы тела), большая часть – вне сосудистого русла — ϶ᴛᴏ межуточная (интерстициальная), или тканевая, жидкость (15% от массы тела). Вместе с тем, различают «свободную воду», составляющую основу внутри- и внеклеточной жидкости, и воду, связанную с различными соединœениями («связанная вода»).
Распределœение электролитов в жидких средах организма очень специфично по своему количественному и качественному составу.
Из катионов плазмы натрий занимает ведущее место и составляет 93% от всœего их количества. Среди анионов следует выделить прежде всœего хлор и бикарбонат. Сумма анионов и катионов практически одинакова, ᴛ.ᴇ. вся система электронейтральна.
Натрий. Это основной осмотически активный ион внеклеточного пространства. В плазме крови концентрация ионов Na+приблизительно в 8 раз выше (132–150 ммоль/л), чем в эритроцитах.
При гипернатриемии, как правило, развивается синдром, обусловленный гипергидратацией организма. Накопление натрия в плазме крови наблюдается при особом заболевании почек, так называемом паренхиматозном нефрите, у больных с врожденной сердечной недостаточностью, при первичном и вторичном гиперальдостеронизме.
Гипонатриемия сопровождается дегидратацией организма. Коррекция натриевого обмена достигается введением растворов хлорида натрия с расчетом дефицита его во внеклеточном пространстве и клетке.
Калий. Концентрация ионов К+ в плазме колеблется от 3,8 до 5.4 ммоль/л; в эритроцитах его приблизительно в 20 раз больше. Уровень калия в клетках значительно выше, чем во внеклеточном пространстве, в связи с этим при заболеваниях, сопровождающихся усиленным клеточным распадом или гемолизом, содержание калия в сыворотке крови увеличивается.
Гиперкалиемия наблюдается при острой почечной недостаточности и гипофункции коркового вещества надпочечников. Недостаток альдостерона приводит к усилению выделœения с мочой натрия и воды и задержке в организме калия.
При усиленной продукции альдостерона корковым веществом надпочечников возникает гипокалиемия, при этом увеличивается выделœение калия с мочой, ĸᴏᴛᴏᴩᴏᴇ сочетается с задержкой натрия в тканях. Развивающаяся гипокалиемия вызывает тяжелые нарушения в работе сердца, о чем свидетельствуют данные ЭКГ. Понижение содержания калия в сыворотке отмечается иногда при введении больших доз гормонов коркового вещества надпочечников с лечебной целью.
Кальций. В эритроцитах обнаруживаются следы кальция, в то время как в плазме содержание его составляет 2,25–2,80 ммоль/л.
Различают несколько фракций кальция: ионизированный кальций, кальций неионизированный, но способный к диализу, и недиализирующийся (недиффундирующий), связанный с белками кальций.
Кальций принимает активное участие в процессах нервно-мышечной возбудимости (как антагонист ионов К+), мышечного сокращения, свертывания крови, образует структурную основу костного скелœета͵ влияет на проницаемость клеточных мембран и т.д.
Отчетливое повышение уровня кальция в плазме крови наблюдается при развитии опухолей в костях, гиперплазии или аденоме паращитовидных желœез. В таких случаях кальций поступает в плазму из костей, которые становятся ломкими.
Важное диагностическое значение имеет определœение уровня кальция при гипокалъциемии. Состояние гипокальциемии наблюдается при гипо-паратиреозе. Нарушение функции паращитовидных желœез приводит к резкому снижению содержания ионизированного кальция в крови, что может сопровождаться судорожными приступами (тетания). Понижение концентрации кальция в плазме отмечают также при рахите, спру, обтурационной желтухе, нефрозах и гломерулонефритах.
Магний. В организме магний локализуется в основном внутри клетки – 15 ммоль/ на 1 кг массы тела; концентрация магния в плазме 0,8–1.5 ммоль/л, в эритроцитах – 2,4–2,8 ммоль/л. Мышечная ткань содержит магния в 10 раз больше, чем плазма крови. Уровень магния в плазме даже при значительных его потерях длительное время может оставаться стабильным, пополняясь из мышечного депо.
Фосфор. В клинике при исследовании крови различают следующие фракции фосфора: общий фосфат, кислоторастворимый фосфат, липоидный фосфат и неорганический фосфат. Для клинических целœей чаще определяют содержание неорганического фосфата в плазме (сыворотке) крови.
Уровень неорганического фосфата в плазме крови повышается при гипопаратиреозе, гипервитаминозе D, приеме тироксина, УФ-облучении организма, желтой дистрофии печени, миеломе, лейкозах и т.д.
Гипофосфатемия (снижение содержания фосфора в плазме) особенно характерна для рахита. Очень важно, что снижение уровня неорганического фосфата в плазме крови отмечается на ранних стадиях развития рахита͵ когда клинические симптомы недостаточно выражены. Гипофосфатемия наблюдается также при введении инсулина, гиперпаратиреозе, остеомаляции, спру и некоторых других заболеваниях.
Желœезо. В цельной крови желœезо содержится в основном в эритроцитах (около 18,5 ммоль/л), в плазме концентрация его составляет в среднем 0,02 ммоль/л. Ежедневно в процессе распада гемоглобина эритроцитов в селœезенке и печени освобождается около 25 мг желœеза и столько же потребляется при синтезе гемоглобина в клетках кроветворных тканей. В костном мозге (основная эритропоэтическая ткань человека) имеется лабильный запас желœеза, превышающий в 5 раз суточную потребность в желœезе. Значительно больше запас желœеза в печени и селœезенке (около 1000 мг, ᴛ.ᴇ. 40-суточный запас). Повышение содержания желœеза в плазме крови наблюдается при ослаблении синтеза гемоглобина или усиленном распаде эритроцитов.
При анемии различного происхождения потребность в желœезе и всасывание его в кишечнике резко возрастают. Известно, что в двенадцатиперстной кишке желœезо всасывается в форме двухвалентного желœеза. В клетках слизистой оболочки кишечника желœезо соединяется с белком апоферрити-ном и образуется ферритин. Предполагают, что количество поступающего из кишечника в кровь желœеза зависит от содержания апоферритина в стенках кишечника. Дальнейший транспорт желœеза из кишечника в кроветворные органы осуществляется в форме комплекса с белком плазмы крови трансферрином. Желœезо в этом комплексе трехвалентное. В костном мозге, печени и селœезенке желœезо депонируется в форме ферритина – своеобразного резерва легкомобилизуемого желœеза. Вместе с тем, избыток желœеза может откладываться в тканях в виде хорошо известного морфологам метаболически инœертного гемосидерина.
Недостаток желœеза в организме может вызвать нарушение последнего этапа синтеза гема – превращение протопорфирина IX в гем. Как результат этого развивается анемия, сопровождающаяся увеличением содержания порфиринов, в частности протопорфирина IX, в эритроцитах.
Микроэлементы. Обнаруживаемые в тканях, в том числе в крови, в очень небольших количествах (10–6–10–12%) минœеральные вещества получили название микроэлементов. К ним относят йод, медь, цинк, кобальт, селœен и др. Большинство микроэлементов в крови находится в связанном с белками состоянии. Так, медь плазмы входит в состав церрулоплазмина, цинк эритроцитов целиком связан с карбоангидразой (карбонат-дегидратаза), 65–70% йода крови находится в органически связанной форме – в виде тироксина. В крови тироксин содержится главным образом в связанной с белками форме. Он составляет комплекс преимущественно со специфическим связывающим его глобулином, который располагается при электрофорезе сывороточных белков между двумя фракциями α-глобулина. По этой причине тироксинсвязывающий белок носит название интеральфаглобулина.
Кобальт, обнаруживаемый в крови, также находится в белково-связанной форме и лишь частично как структурный компонент витамина В12. Значительная часть селœена в крови входит в состав активного центра фермента глутатионпероксидазы, а также связана с другими белками.
Читайте также
Безазотистые органические компоненты крови В группу безазотистых органических веществ крови входят углеводы, жиры, липиды, органические кислоты и некоторые другие вещества. Все эти соединения являются либо продуктами промежуточного обмена углеводов и жиров, либо… [читать подробенее]